J IMMUNOTHER CANCER:易普利姆玛和纳武单抗治疗转移性或不可切除的血管肉瘤的多中心II期试验(SWOG S1609,队列51):罕见肿瘤(DART)中双重抗CTLA-4和抗PD-1阻断的子研究
血管肉瘤是一种侵袭性癌症,难以治疗且死亡率高,由于是极罕见的肿瘤,在美国每年只有大约400例新病例,转移性疾病患者的治疗选择有限。本文研究者报告了用易普利姆玛和纳武单抗治疗血管肉瘤的结果,作为正在进行的罕见癌症研究的队列。
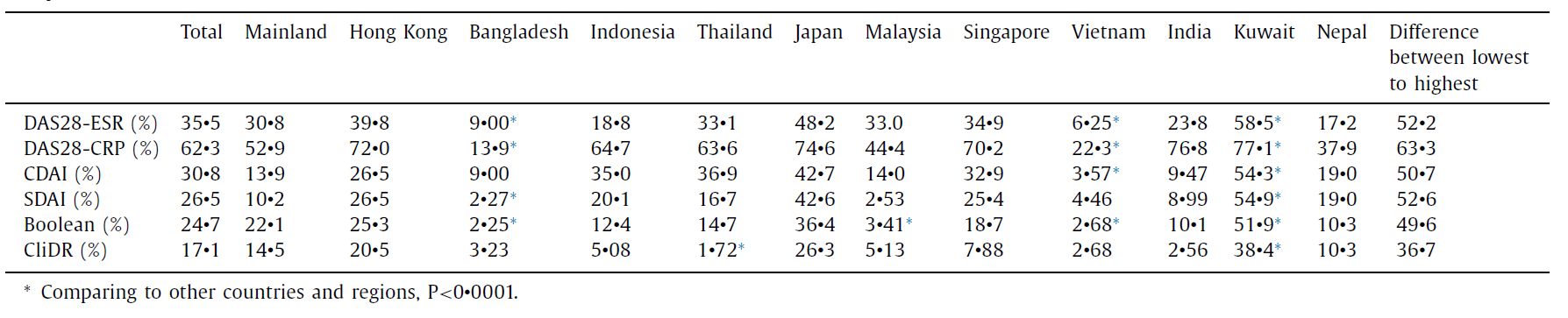
Lancet子刊在线发表类风湿关节炎治疗大样本多中心研究成果
Lancet杂志子刊The Lancet Regional Health(WP)在线发表了题为“亚太地区类风湿关节炎临床缓解的多中心真实世界研究结果”(Clinical remission of rheumatoid arthritis in a multicenter real-world study in Asia-Pacific region)的文章。
中山大学肿瘤防治中心徐瑞华教授发布特瑞普利单抗联合化疗一线治疗复发或转移性鼻咽癌III期研究成果
由中山大学肿瘤防治中心主任、院长徐瑞华教授为通讯作者(中山大学肿瘤防治中心麦海强教授和陈秋燕教授为文章共同第一作者)在顶级医学期刊Nature Medicine上发表文章特瑞普利单抗或安慰剂联合化疗一线治疗晚期鼻咽癌的多中心随机III期临床研究,公开了本土创新药特瑞普利单抗联合化疗一线治疗复发或转移性鼻咽癌III期研究(JUPITER-02研究)成果。今年6
国家有关部门发布关于开展第五批国家临床医学研究中心申报工作的通知
近日,科技部办公厅、 国家卫生健康委办公厅 、军委后勤保障部办公厅、 药监局综合发布了关于开展第五批国家临床医学研究中心申报工作的通知,全文如下;各有关单位:按照《国家临床医学研究中心五年(2017-2021年)发展规划》(国科发社〔2017〕204号)的总体部署和《国家临床医学研究中心管理办法(2017年修订)》的要求,
全球最大样本量的子宫内膜菌群检测 (EMMA/ALICE) 中心随机对照临床研究项目正式启动
2021 年 5 月 31 日 晚,由北京大学第三医院发起,中山大学孙逸仙纪念医院、中信湘雅生殖与遗传专科医院共同参与的“比较基于EMMA/ALICE检测经治疗后的胚胎移植与常规的冷冻胚胎移植(FET)用于不孕妇女首次IVF/ICSI周期的随机对照试验(RCT)(国际注册号:NCT04686357,以下简称为
美国疾控中心(CDC)最大规模COVID-19疫苗在医疗工作者中有效性研究:mRNA疫苗有效率94%!
在接种第二剂mRNA疫苗后≥7天的医疗工作者中,COVID-19疾病减少94%。
新冠DNA疫苗首个全球多中心III期临床研究计划启动
新冠DNA疫苗的研发进程一直受到业内的密切关注。近日,美国Inovio制药宣布,新冠DNA疫苗的美国II期临床已接近尾声,计划基于II期安全性和免疫原性的评价结果,启动全球多中心III期临床研究。Inovio制药将联合新冠DNA疫苗的合作伙伴苏州艾棣维欣生物制药(Advaccine),以及国际疫苗研究院(IVI)等机构共同开展该III期临床研究。III期临床
分子植物科学卓越创新中心发现HYL1蛋白调控miRNA介导的翻译抑制过程
中国科学院分子植物科学卓越创新中心/植物生理生态研究所研究员何玉科研究组在The Plant Cell上,发表了题为Cytoplasmic HYL1 modulates miRNA-mediated translational repression的研究论文。该研究组发现,HYL1蛋白除了介导microRNA (miRNA)的转录后调
Nature Communications:北医三院国家妇产疾病临床医学研究中心两项重要研究成果
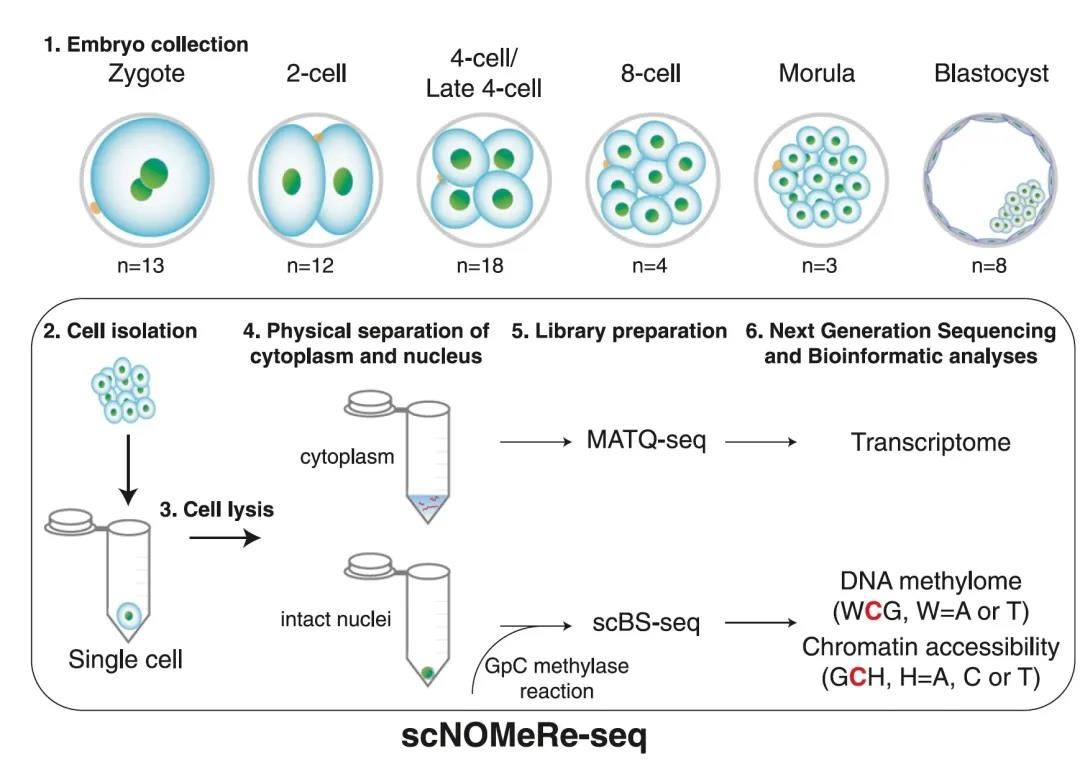
北京大学第三医院(北医三院)李默课题组卵巢癌发生相关研究成果和乔杰闫丽盈课题组关于早期胚胎发育机制方面的研究成果,同时在国际学术期刊《自然通讯》(Nature Communications)上在线发表。卵巢癌是妇科致死率最高的恶性肿瘤,严重危害女性生命健康及生育能力。由于其异质性强及转移率高,该疾病的早期诊断与治疗一直是肿瘤领域研究的重点与难点。李默课题组主
国家药监局药审中心发布皮肤外用化学仿制药研究技术指导原则
3月16日,国家药品监督管理局药审中心为指导我国皮肤外用化学仿制药研发,提供可参考的技术标准,组织制定了《皮肤外用化学仿制药研究技术指导原则(试行)》。经国家药品监督管理局审查同意,现予发布,自发布之日起施行。原文如下:国家药监局药审中心关于发布《皮肤外用化学仿制药研究技术指导原则(试行)》的通告(2021年第23号)发布日期:202