亚洲芒苞草属和非洲黑炭木属植物叶绿体基因组比较与系统定位研究取得进展
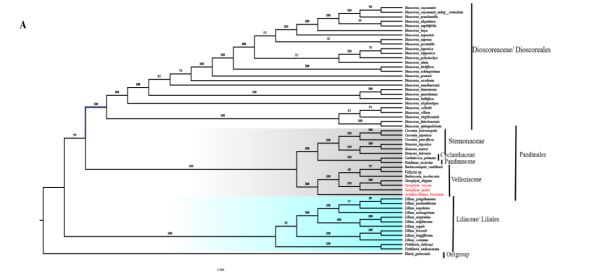
翡若翠科(Velloziaceae)由5属约250个物种组成的单子叶植物科,在非洲、马达加斯加、阿拉伯半岛、中国和南美洲间断分布。该科植物多为耐旱的复苏植物,花的特征较为相似,而叶形、植株大小和生活型等形态特征又具变异,因而该科植物的分类比较困难,成员之间的亲缘关系尚不清楚。中国科学院武汉植物园东非植物区系与分类学科组对采自我国横断山
新研究表明转基因草可用于清除含有军用炸药残留有毒污染物的土壤
英国约克大学网站发布消息,一项由约克大学领导的研究表明,转基因柳枝稷草(Panicum virgatum)可用于清除炸弹训练场、弹药场和雷场使用的军用炸药RDX(黑索金)的残留物,这些弹药残留在地面的有毒化学物质对人类健康有危害。自第二次世界大战以来,RDX一直是弹药的主要组成部分,至今仍在军事训练场上广泛使用,这导致了地下水的广泛污
甘李药业在研产品GLR2007获欧盟委员会孤儿药资格认定
4月6日,甘李药业发布公告称,近日收到欧盟委员会(简称“EC”)的正式书面回函,授予本公司在研创新药细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂(以下简称“GLR2007”)孤儿药资格认定,用于治疗胶质瘤。GLR2007是一款细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂,为本公司自主研发的创新型小分子化学药物,拟用于包括脑
研究人员利用环境DNA检测草花粉水平
草花粉是一种主要的室外过敏原,导致了广泛的呼吸道疾病,包括过敏性哮喘和鼻炎。3月12日,研究人员在Cell Press细胞出版社旗下期刊Current Biology(《当代生物学》)上报告称,环境DNA可以帮助人们更好地了解哪些草类是最严重的“致敏者”。“这些发现改善了我们对花粉和人群健康之间复杂关系的理解。”英国埃克塞特大学的Be
甘李药业每周1次长效 GLP-1受体激动剂申报临床
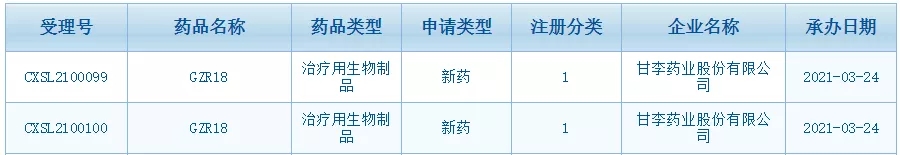
3月24日,CDE官网显示,甘李药业每周注射1次的胰高血糖素样肽 1(GLP-1)受体激动剂 GZR18 的临床申请已获得国家药监局受理(受理号:CXSL2100099 国、CXSL2100100 国),本次申请的临床试验适应症为 II 型糖尿病、肥胖及超重。在中国糖尿病人群中大约 90%-95%为 II 型糖尿病。据一项全国范围内的调查结果显示
三叶草生物与Dynavax宣布新冠候选疫苗全球II/III期临床试验“SPECTRA” 完成首批志愿者接种
专注于针对世界严重疾病研发创新型生物疗法和疫苗的全球临床阶段生物制药公司 — 三叶草生物制药有限公司(以下简称“三叶草生物”)和专注于开发和商业化新型疫苗的生物制药公司 — Dynavax Technologies Corporation公司(以下简称“Dynavax”)宣布三叶草生物的新冠候选疫苗全球II/III期临床试验项目“SP
齐鲁「唑来膦酸注射液」通过一致性评价
国家药监局官网显示,齐鲁唑来膦酸注射用浓溶液(5ml:4mg)通过一致性评价,成为该规格首家过评企业。此规格对应适应症为:①与标准抗肿瘤药物治疗合用,治疗实体肿瘤骨转移患者和多发性骨髓癌患者的骨骼损害。②治疗恶性肿瘤引起的高钙血症。唑来膦酸为第三代双膦酸盐,与第一、二代相比,具有抗骨吸收作用更强、 降低骨相关事件发生率疗效更优的临床优
甘莱NASH候选药物ASC42获美国FDA快速通道资格认定
12月14日,歌礼制药有限公司旗下全资子公司甘莱宣布,美国FDA授予其NASH候选药物ASC42快速通道资格。美国FDA的快速通道项目旨在加速针对严重疾病的药物开发和快速审查,以解决未获满足的医疗需求。目前,尚无获得美国FDA批准的NASH药物。ASC42能顺利获得快速通道资格认定,表明美国FDA认可其有解决NASH患者未被满足的医疗
三叶草生物发布“S-三聚体”新冠候选疫苗I期积极结果
I期临床研究数据表明,三叶草生物的“S-三聚体”重组亚单位新冠候选疫苗分别在与GSK预防疾病大流行的疫苗佐剂系统或Dynavax的CpG 1018加铝佐剂系统联合使用下,在150 名成年和老年受试者中诱导出强烈的中和免疫应答。三叶草生物的新冠候选疫苗被证实具有良好的安全性和耐受性,在2-8摄氏度下具有长期稳定性,适合在全球范围内分发。由流行病预防