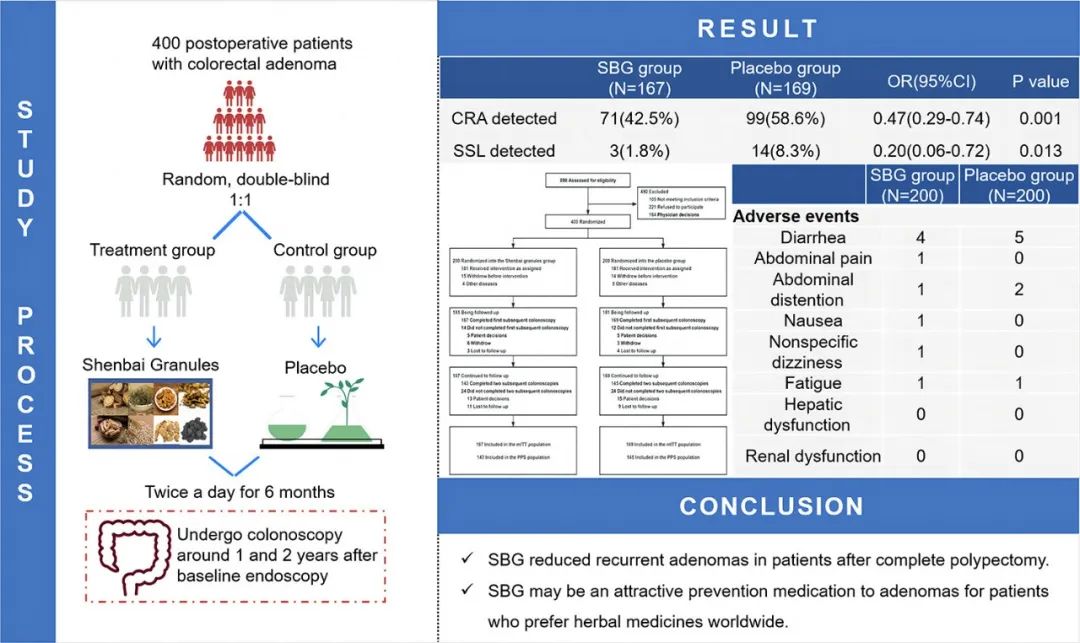
中国首个国际注册中药复方临床研究,证实参白颗粒显著降低结直肠腺瘤术后复发率
结果表明,参白颗粒在预防CRA复发方面表现出色,相较于过去的化学预防药物,其疗效显著(减少CRA复发率16.07%),安全性高,采用天然植物炮制,避免了化学药物的潜在副作用。
2024-04-11
广生堂一类创新药泰中定—超级3CL抑制剂的注册临床研究数据将发表于国际权威医学期刊柳叶刀《eClinicalMedicine》
泰中定的注册临床研究数据将发表于国际权威医学期刊《柳叶刀》旗下子刊《eClinicalMedicine》。
2024-03-22
【注册倒计时】内含参会须知!2023(第六届)单细胞多组学研究与应用研讨会,9月14日开幕在即!
2023第六届单细胞多组学研究与应用研讨会,2023年9月14-15日,上海北虹桥绿地铂骊酒店
2023-09-06
饶毅创建的华毅乐健再迎重要里程碑 |血友病AAV基因疗法完成注册临床I期首例受试者入组
2023年8月22日,中国苏州,苏州华毅乐健生物科技有限公司(以下简称“华毅乐健),一家致力于基因治疗创新药开发的生物技术公司,今日宣布其自主研发的基因治疗血友病A GS1191-0445
2023-08-22
Moderna在上海落地公司,注册资本为1亿美元,计划更多参与中国市场
根据路透社报道,近日“mRNA 疫苗三巨头”之一 Moderna(NASDAQ: MRNA)已在中国上海注册了实体公司,并计划在中国寻求更多机会。
2023-06-02
邦耀生物CAR-T细胞(BRL-201)治疗启动注册临床试验
2023年3月16日,邦耀生物宣布称在研CAR-T细胞产品(BRL-201)注册临床试验的启动会在中国医学科学院血液病医院召开,标志着这款CAR-T细胞临床试验正式启动。
2023-03-20
中国国家药品监督管理局正式受理新可来®重度嗜酸粒细胞性哮喘适应症注册申请
美泊利珠单抗通过与IL-5结合,阻断IL-5与嗜酸粒细胞表面受体的结合,从而使血液中嗜酸粒细胞的数量降低并维持在正常水平。
2023-03-14
全球首个斑马鱼PDX临床研究注册项目携手类器官技术,限量开启抗肿瘤药物研发单位合作申请
环特生物联合国内知名三甲医院共同发起“基于胃癌的斑马鱼PDX与类器官抗肿瘤药效评价的科研项目”,通过构建胃癌的精准医疗生物样本库,致力于为广大药企的抗肿瘤药物提供药效评价的科研服务。
2023-02-02