剑指罗氏王牌生物制剂Avastin(安维汀)!迈兰/百康MYL-1402(贝伐单抗生物仿制药)在美国进入审查
来源:本站原创 2020-03-12 14:16
2020年03月12日/生物谷BIOON/--迈兰(Mylan)与合作伙伴印度生物制药公司百康(Bicon)近日联合宣布,美国食品和药物管理局(FDA)已受理迈兰提交的贝伐单抗生物仿制药MYL-1402O的生物制品许可申请(BLA)。该申请将通过351(k)途径进行审查,生物仿制药用户收费法(BsUFA)目标日期为2020年12月27日。MYL-1402O是

2020年03月12日/生物谷BIOON/--迈兰(Mylan)与合作伙伴印度生物制药公司百康(Bicon)近日联合宣布,美国食品和药物管理局(FDA)已受理迈兰提交的贝伐单抗生物仿制药MYL-1402O的生物制品许可申请(BLA)。该申请将通过351(k)途径进行审查,生物仿制药用户收费法(BsUFA)目标日期为2020年12月27日。
MYL-1402O是罗氏王牌生物制剂Avastin(安维汀,通用名:bevacizumab,贝伐单抗)的生物仿制药。此次BLA,寻求批准MYL-1402O用于:(1)联合氟尿嘧啶化疗一线和二线治疗转移性结直肠癌;(2)一线治疗非鳞状非小细胞肺癌(NSCLC);(3)复发性胶质母细胞瘤;(4)联合干扰素α治疗转移性肾细胞癌(RCC);(5)治疗持续性、复发性、转移性宫颈癌。
如果获得批准,MYL-1402O将成为迈兰和百康合作产品组合中在美国获得批准治疗癌症的第三个生物仿制药,该产品现在已在印度和其他发展中市场上市。
此次BLA基于一项全球性随机、双盲III期临床试验的数据。该研究共入组了671例诊断为IV期非鳞状非小细胞肺癌(NSCLC)的患者。研究中,符合资格的患者随机接受MYL-1402O或Avastin,并联用卡铂和紫杉醇治疗6个疗程(18周)。之后,患者继续接受MYL-1402O或Avastin单药治疗直至第42周。
结果显示,在第18周,研究达到了主要终点:最佳客观缓解率(ORR)比率的90%置信区间在预先指定的等效范围内,包括免疫原性在内的安全性与Avastin相似。
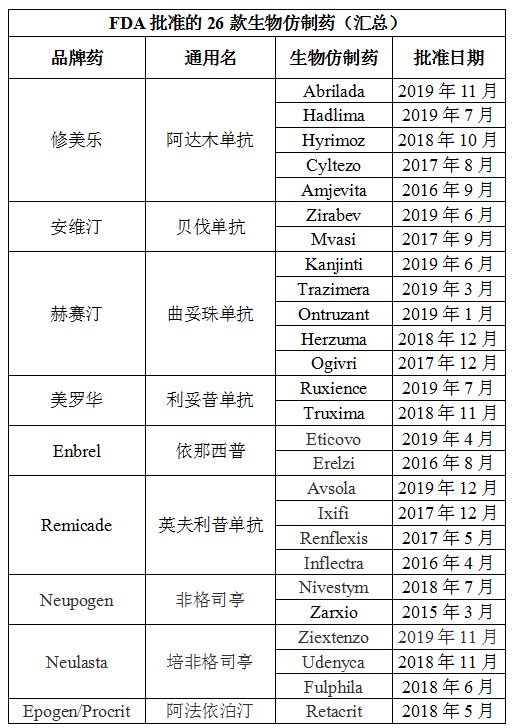
目前,迈兰和百康正在为全球市场共同开发多达11种生物产品。在美国,双方推出的首个生物仿制药是Fulphila(pegfilgrastim-jmdb,培非格司亭),该药于2018年6月获得批准,是安进重磅“升白”药物Neulasta(pegfilgrastim,培非格司亭)的首个生物仿制药。
2019年12月,双方在美国推出Ogivri(trastuzumab-dkst,曲妥珠单抗),该药是罗氏另一款王牌生物制剂Herceptin(赫赛汀,通用名:trastuzumab,曲妥珠单抗)的生物仿制药。Ogivri于2017年12月获得美国FDA批准,是该机构批准的首个曲妥珠单抗生物仿制药,被批准用于Herceptin的全部适应症,包括治疗HER2过表达的乳腺癌和转移性胃癌(胃或胃食管交界腺癌)。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


