宫颈癌一线免疫治疗!默沙东Keytruda+铂类化疗3期临床成功:显著延长总生存期(OS)和无进展生存期(PFS)!
来源:本站原创 2021-06-23 03:31
Keytruda是第一个被批准治疗晚期宫颈癌的抗PD-1疗法,用于二线治疗复发或转移性患者。
2021年06月22日讯 /生物谷BIOON/ --默沙东(Merck & Co)近日公布了评估抗PD-1疗法Keytruda(可瑞达®,通用名:pembrolizumab,帕博利珠单抗)一线治疗宫颈癌关键3期KEYNOTE-826试验(NCT03635567)的结果。该试验在617例在先前没有接受过系统化疗、也不再适合根治性治疗(如手术和/或放疗)的持续性、复发性或转移性宫颈癌(包括鳞状细胞癌、腺鳞状癌、腺癌)成人患者中开展,正在评估Keytruda对比安慰剂,联合铂类化疗(紫杉醇+顺铂,或紫杉醇+卡铂)加用或不加用贝伐单抗(bevacizumab)用于一线治疗的疗效和安全性。研究主要终点是总生存期(OS)和无进展生存期(PFS)。次要终点包括:总缓解率(ORR)、缓解持续时间(DOR)、安全性。
结果显示,该试验达到了OS和PFS主要终点。根据独立数据监测委员会(IDMC)开展的一项中期分析,无论患者肿瘤PD-L1状态如何,与对照方案(安慰剂+铂类化疗方案,加用或不加用贝伐单抗),Keytruda方案(Keytruda+相同的铂类化疗方案,加用或不加用贝伐单抗)显示OS和PFS方面有统计学显著和临床意义的改善。
根据该试验结果,Keytruda是第一个证明这一点的抗PD-1/PD-L1疗法。该试验中,Keytruda的安全性与先前研究报道的一致。试验结果将在即将召开的医学会议上公布,并将提交给监管机构。
默沙东研究实验室首席医疗官、高级副总裁兼全球临床开发负责人Roy Baynes博士表示:“尽管在预防和筛查方面取得了进展,但宫颈癌仍然是一个重大的健康问题,往往影响青中年女性。确诊为转移性宫颈癌的女性预后特别差,迫切需要新的治疗方案。KEYNOTE-826是第一个在一线持续性、复发性或转移性宫颈癌中显示免疫治疗阳性结果的研究,我们期待在即将召开的大会上分享这些发现,并与监管机构讨论。我们感谢患者、他们的护理人员和研究人员参与这项重要的研究。”
3期KEYNOTE-826试验也是目前加速批准Keytruda治疗宫颈癌的验证性试验。2018年6月,Keytruda获得美国FDA加速批准,用于二线治疗复发或转移性宫颈癌患者,具体为:化疗期间或化疗后疾病进展、经FDA批准的检测方法证实肿瘤表达PD-L1(合并阳性评分[CPS]≥1)的复发性或转移性宫颈癌女性。
根据这项加速批准,Keytruda成为第一个获批治疗晚期宫颈癌的PD-1免疫疗法。此次批准也标志着Keytruda在妇科癌症领域的首个适应症。来自II期KEYNOTE-158队列E的数据显示,在PD-L1阳性(CPS≥1)患者中,Keytruda治疗的总缓解率(ORR)为14.3%,而在PD-L1阴性(CPS<1)的患者中没有观察到治疗反应。
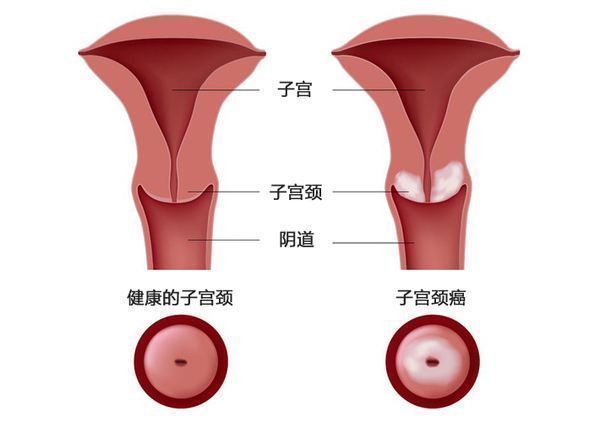
宫颈癌是全世界女性癌症死亡的第四大原因,尽管宫颈癌可能出现在任何年龄的女性身上,但最常见于35-44岁女性人群。几乎所有的病例都是由人类乳头瘤病毒(HPV)感染引起的,大约80%被归类为鳞状细胞癌(SCC,起源于宫颈底部的细胞),其余大部分是腺癌(起源于宫颈上部的腺细胞)。
尽管在常规医学筛查和预防(HPV疫苗)方面已取得了进展,但宫颈癌仍然普遍存在。据估计,全世界每年新诊断的宫颈癌病例超过60万,死亡人数超过34万。宫颈癌在早期发现和有效治疗时通常是可以治愈的,但晚期、复发性或转移性宫颈癌的治疗方案有限,生存率很低。在美国,对于诊断为已扩散到身体较远部位的宫颈癌患者,5年生存率估计约为17%。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


