2022年HIV研究进展第4期
来源:生物谷原创 2022-08-30 11:01
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。
人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴细胞,进而阻断细胞免疫和体液免疫过程,导致免疫系统瘫痪,从而致使各种疾病在人体内蔓延,最终导致艾滋病。由于HIV的变异极其迅速,难以生产特异性疫苗,至今无有效治疗方法,对人类健康造成极大威胁。
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
生物谷小编梳理了一下近期生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Science子刊:揭示广泛中和抗体VRC07的IgG亚型影响它预防HIV传播的能力
doi:10.1126/scitranslmed.abn9662
在HIV大流行的40多年后,科学家们对如何防御这种病毒有了新的认识,这些发现最终可能会导致产生一种中和抗体,从而在HIV成为破坏免疫力的威胁之前阻止它。
在一项新的研究中,来自美国拉根研究所、哈佛医学院和达特茅斯学院的研究人员破译了一种广泛保护性抗HIV抗体亚型是如何抵御HIV感染的。这一发现有朝一日可能为用基于抗体的疗法治疗或预防HIV传播的努力提供参考。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“Antibody-mediated prevention of vaginal HIV transmission is dictated by IgG subclass in humanized mice”。
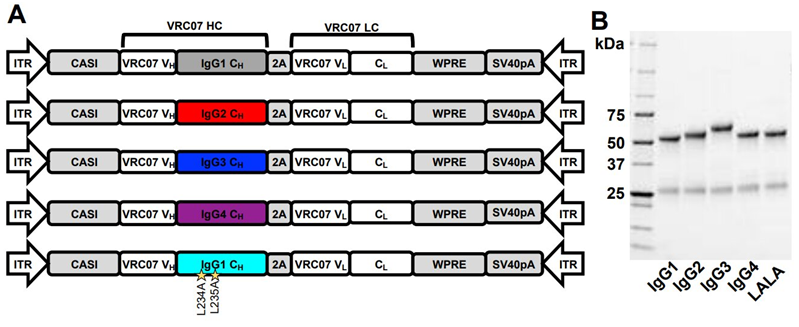
VRC07 IgG亚型的表达和纯化。图片来自Science Translational Medicine, 2022, doi:10.1126/scitranslmed.abn9662。
这些作者指出,一种IgG亚型抗体积极地靶向HIV包膜蛋白的保守区域。这使得这些抗体能够阻止这种病毒进入并驱动针对受感染细胞的免疫反应。
论文第一作者、拉根研究所的Jacqueline M. Brady博士及其同事们写道,“HIV广泛中和抗体既能阻断病毒进入,又能驱动针对遭受HIV感染的细胞的先天免疫反应。”他们强调这种IgG抗体亚型触发了先天免疫系统的爆炸性活动。
2.Nat Med:一种新确定的生物标志物有望加快预防HIV-1感染的疫苗开发
doi:10.1038/s41591-022-01953-6
广泛中和抗体(bnAb)的定义是它们能够中和多种遗传上不同的病毒毒株。在一项新的研究中,来自美国华盛顿大学和弗雷德-哈钦森癌症中心等研究机构的研究人员确定了一种新的生物标志物,它似乎可以有效地作为替代终点,可靠地预测广泛中和单克隆抗体防止HIV-1(导致艾滋病的最常见病毒类型)感染的能力。相关研究结果于2022年8月22日在线发表在Nature Medicine期刊上,论文标题为“Neutralization titer biomarker for antibody-mediated prevention of HIV-1 acquisition”。
这项新研究的结果建立在2021年3月发表的概念验证性抗体介导预防(Antibody Mediated Prevention, AMP)临床试验的基础上,该临床试验显示一种名为VRC01的bnAb能有效防止某些---但不是所有--HIV毒株的感染。在进行研究的地区---撒哈拉以南非洲、美国和南美---流行的70%的HIV毒株对VRC01有抵抗力,而且最初的报告还已指出,在整体预防HIV感染方面,VRC01组和安慰剂组之间没有统计学差异。
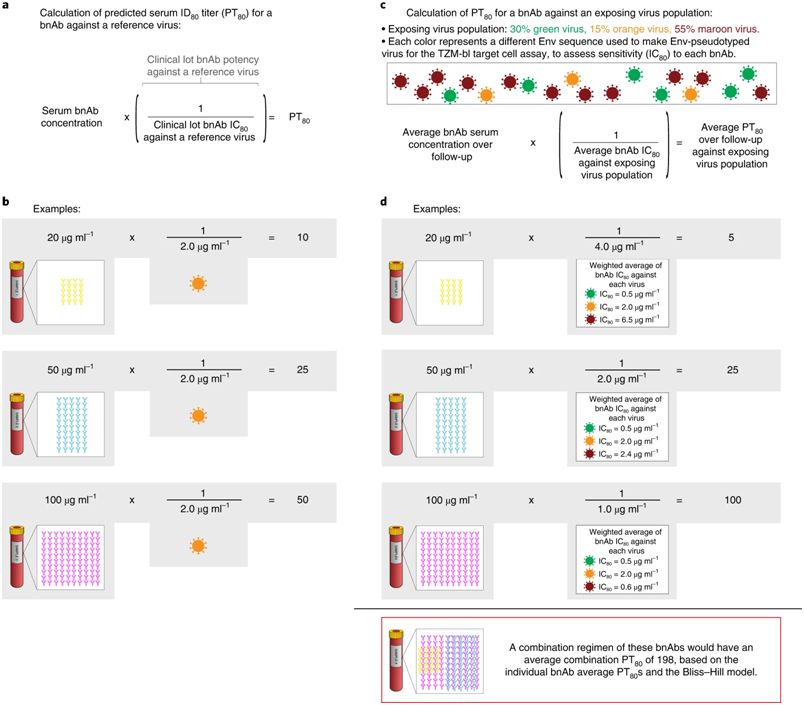
图片来自Nature Medicine, 2022, doi:10.1038/s41591-022-01953-6。
论文通讯作者兼论文共同第一作者、弗雷德-哈钦森癌症中心的Peter Gilbert博士说,“单一的HIV-1广泛中和单克隆抗体,如VRC01,将不足以提供对HIV-1感染的高度保护,因为许多HIV-1毒株具有抵抗性。因此,将需要bnAb混合物,尽管这些抗体有丰富的开发渠道,但我们首先需要一种生物标志物,使我们能够比较不同的bnAb混合物,并选择最佳候选混合物进行疗效试验。”
Gilbert说,一种有用的生物标志物也必须被验证为替代终点,以可靠地预测HIV-1 bnAb混合物的预防功效水平。这将允许加快批准不同的HIV-1 bnAb混合物,而不需要长期和昂贵的疗效临床试验。根据这项新研究的结果,这种新确定的生物标志物---PT80---似乎符合这些要求,它可以预测bnAb受者的血液样品在特定时间对特定病毒的80%中和抗体滴度。
3.eLife:新型广泛中和抗体联合使用有望阻止HIV病毒逃逸和反弹
doi:10.7554/eLife.76004
在一项新的研究中,来自德国马克斯-普朗克动力学与自组织研究所、科隆大学和美国华盛顿大学的研究人员发现精心设计的广泛中和抗体(bNAb)混合物可能能够帮助治疗HIV感染,同时将这种病毒逃避治疗的风险降到最低。相关研究结果于2022年7月19日在线发表在eLife期刊上,论文标题为“Design of an optimal combination therapy with broadly neutralizing antibodies to suppress HIV-1”。

论文第一作者、马克斯-普朗克动力学与自组织研究所研究员Colin LaMont说,“在我们的研究中,我们提出使用一种计算方法来预测基于HIV遗传学的bNAb组合的有效性。”
LaMont及其同事们使用高通量测序技术分析了10年来从11名未经治疗的HIV患者身上收集的HIV病毒的遗传学特征。他们利用这些数据预测哪些HIV毒株可能能够逃避不同bNAb的治疗,以及逃避bNAb治疗是否与生存成本有关。接下来,利用计算方法,他们将获得的知识用于预测三项真实的bNAb临床试验中的病毒反弹。
最后,这些作者利用他们的计算方法找到了最不可能让任何病毒逃避的bNAb组合。他们还发现,一些bNAb(比如10-1074)能更好地对抗不同的病毒群体,因为允许病毒逃逸的突变也使这种病毒不太可能生存。其他的bNAb(包括PGT121)对不那么多样化的病毒群体更有效,因为能够让病毒逃逸的突变很罕见。总的来说,这些研究结果表明,最佳组合包括三种bNAb:PG9、PGT151和VRC01。
4.Mol Cell:揭示机体免疫系统利用两步法机制来抵御HIV-1感染的新型分子机制
doi:10.1016/j.molcel.2022.06.010
HIV-1因其能躲避宿主机体免疫系统的攻击而闻名。近日,一篇发表在国际杂志Molecular Cell上题为“Recognition of HIV-1 capsid by PQBP1 licenses an innate immune sensing of nascent HIV-1 DNA”的研究报告中,来自Scripps研究所等机构的科学家们通过研究揭示了机体先天性免疫系统检测HIV-1的分子机制(即使当病毒量较少时),先天性免疫系统是机体抵御外来入侵者的第一道防线。
先天性免疫系统会在适应性免疫系统之前被激活,后者是机体的第二道防线,其涉及多种专门的功能,比如产生抗体等,先天性免疫系统的一个主要职责就是识别自我和外来病原体(比如细菌和病毒等),环状GMP-AMP合成酶(cGAS)是先天性免疫系统中重要的信号蛋白,其能感知细胞中漂浮的DNA,如果cGAS检测到了外来病原体的存在,其就会激活分子途径来抵御入侵者。然而,由于HIV-1是一种RNA病毒,其会产生微量的DNA,实际上,科学家们目前并不理解cGAS以及先天性免疫系统如何对其进行监测以及如何将其与机体自身的DNA进行区分的。
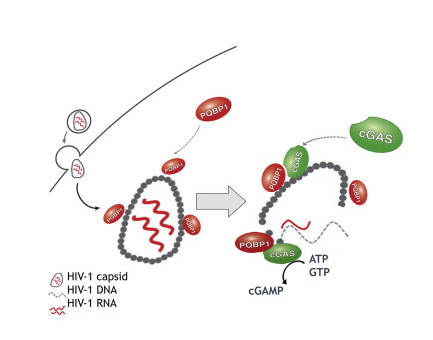
揭示机体免疫系统利用两步法机制来抵御HIV-1感染的新型分子机制。图片来源:Molecular Cell (2022). DOI: 10.1016/j.molcel.2022.06.010。
这篇研究报告中,研究人员发现,先天性免疫系统需要两步安全检查来激活抵御HIV-1的能力,第一步主要涉及一种名为PQBP1(polyglutamine binding protein 1,多聚谷氨酰胺结合蛋白1)的必要蛋白,其能在HIV-1进入细胞后开始复制之前就识别出病毒的外壳,随后PQBP1就会包裹并装饰病毒,并作为一种警惕信号来召唤cGAS,一旦病毒外壳开始分解,cGAS就会激活额外的免疫相关通路来抵御病毒。最初研究人员惊讶地发现能帮助先天性免疫激活来抵御HIV-1的两个关键步骤,因为大多数其他DNA编码的病毒仅会在一个步骤中激活cGAS,这是一种类似于使用双因子认证技术的概念,比如要求用户输入密码,随后回复确认邮件。
这种两步法机制或能为科学家们开发新型疫苗策略提供思路,其能在病毒在宿主细胞内开始复制之前,在PQBP1对分子进行装饰之后开始宿主机体的免疫级联反应。研究者Sunnie Yoh认为,尽管适应性免疫系统一直是HIV研究和疫苗开发的重点,但本文研究清楚地揭示了先天性免疫反应在检测病毒上所扮演的关键角色,在调节这个两步过程的窗口中,或许研究人员有望开发出抵御HIV-1的新型佐剂疫苗策略,即在PQBP1装饰病毒衣壳后,病毒将其自身整合到宿主基因组并开始复制之前。
5.PNAS:首次解析出HIV-1基质的原子视图,有助于揭示这种病毒组装和包膜蛋白整合机制
doi:10.1073/pnas.2200794119
导致艾滋病的HIV-1的组装发生在受感染细胞的内质膜层上,这是一个几何构建过程,在病毒蛋白Gag的N端基质结构域(matrix domain, MA)的引导下,从病毒Gag蛋白的三聚体中产生六聚体。然而,四十年来一直缺乏这种病毒颗粒组装的某些细节。在一项新的研究中,阿拉巴马大学伯明翰分校微生物学教授Jamil Saad博士及其同事们提供了HIV-1基质晶格的首个原子视图,以2.1埃的分辨率显示了它的分子细节,这一发现推进了对病毒组装和病毒包膜蛋白(Env)整合的关键机制的理解。相关研究结果发表在2022年6月3日的PNAS期刊上,论文标题为“Atomic view of the HIV-1 matrix lattice; implications on virus assembly and envelope incorporation”。
在Saad及其同事们描述的HIV-1基质晶格结构中,myrMA的豆蔻酸基团在稳定这种晶格结构方面起着关键作用,因此形成myrMA晶体的能力很重要。他们通过从长132个氨基酸的myrMA末端去除20个氨基酸来完成这一难以捉摸的技术挑战。众所周知,在质膜上形成Gag晶格对于未成熟的HIV-1的组装和Env的整合是必需的。

图片来自Structure, 2017, doi:10.1016/j.str.2017.09.010。
Saad及其同事报告说,他们的myrMA晶格被排列为带有中心孔的三聚体晶格的六聚体,被认为是为了容纳Env的细胞质尾巴以促进Env整合到病毒颗粒中。他们的myrMA晶体使他们能够观察myrMA晶格中附着的豆蔻酸基团。他们发现,myrMA的一个亚基上的豆蔻酸基团穿过二倍轴插入到这个亚基的疏水腔中,实现了“豆蔻酸基团交换(myr swapping)”,而且他们还报告了三聚体之间的其他分子相互作用。他们描述了有助于稳定三聚体晶格的六聚体的额外分子细节。
doi:10.1016/j.isci.2022.104488
在一项新的研究中,来自美国加州大学洛杉矶分校的研究人员发现HIV对感染者的衰老有“早期和实质性”的影响,在感染后短短两到三年内就会加速身体中与正常衰老有关的生物变化。这一发现表明,相对于未感染者,HIV感染可能会使一个人的寿命缩短近5年。相关研究结果于2022年6月30日在线发表在iScience期刊上,论文标题为“Accelerated aging with HIV begins at the time of initial HIV infection”。
这些作者分析了100名男性在感染HIV前6个月或更短时间内收集的储存血液样品,并在感染后2至3年再次收集血液样品。他们将这些样本与同一时期来自100名未受HIV感染的男性的匹配样本进行了比较。所有这些人都是多中心艾滋病队列研究(Multicenter AIDS Cohort Study)的参与者,多中心艾滋病队列研究是一项从1984年到2019年为期35年的全国性研究。这些作者说这项研究是第一项以这种方式匹配感染者和非感染者的研究。
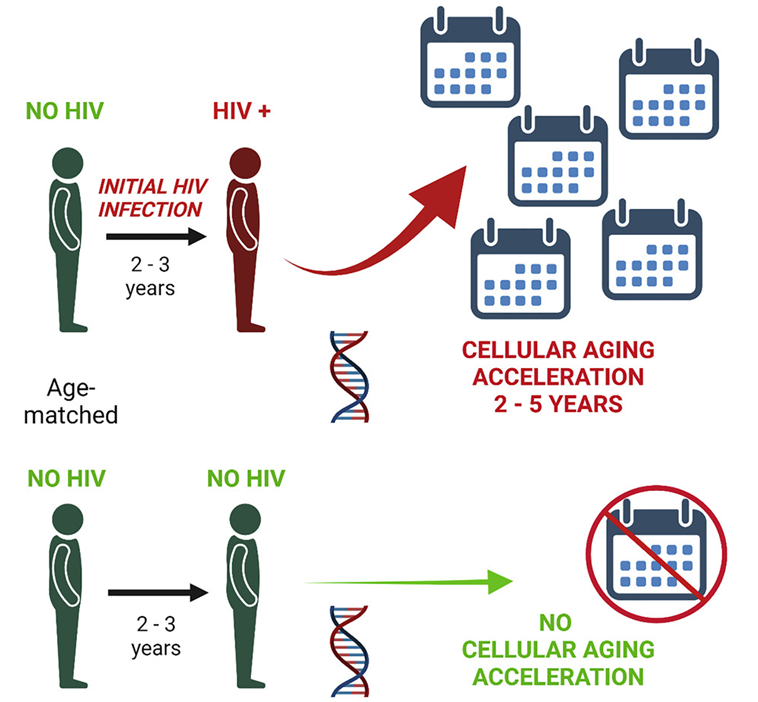
图片来自iScience, 2022, doi:10.1016/j.isci.2022.104488。
这些作者专注于HIV如何影响表观遗传学的DNA甲基化,这是细胞在正常生理变化过程中用来开启或关闭基因的过程。表观遗传学变化是那些对环境、人们的行为或其他外部因素---比如疾病---的影响所做出的反应,这会影响基因的行为方式,而不改变基因本身。
这些作者研究了关于衰老的五种表观遗传指标。其中的4种是所谓的表观遗传“时钟”,每一种表观遗传时钟都使用了稍微不同的方法来估计以年份为单位的生物年龄加速(相对于生理年龄而言)。第五种表观遗传指标评估了端粒的长度,端粒是染色体的保护性帽状末端。随着年龄的增长,端粒在每次细胞分裂时会逐渐变短,直到它们变得如此之短,以至于分裂不再可能。
HIV感染者在四种表观遗传时钟中的每一种都显示出明显的年龄加速---从1.9岁到4.8岁不等---以及在没有高度活跃的抗逆转录病毒治疗的情况下,从感染前开始到感染后两到三年的时间里,端粒变短。在相同的时间间隔内,在未感染的参与者中没有看到类似的年龄加速。
doi:10.1073/pnas.2117781119
德克萨斯大学奥斯汀分校德克萨斯高级计算中心的Frontera超级计算机进一步加深了科学家们对HIV-1病毒如何感染的理解,并协助生成了第一个关于它的衣壳的现实模拟,包括它蛋白、水、遗传物质和最近发现的一种叫做IP6的关键辅助因子,该辅助因子稳定和帮助形成这种衣壳。
芝加哥大学杰出服务教授Gregory Voth说,“这些非常大的模拟和我们所做的分析揭示了HIV-1病毒衣壳盔甲的漏洞。”Voth是近期发表在PNAS期刊上的一篇标题为“Strain and rupture of HIV-1 capsids during uncoating”的论文的通讯作者。
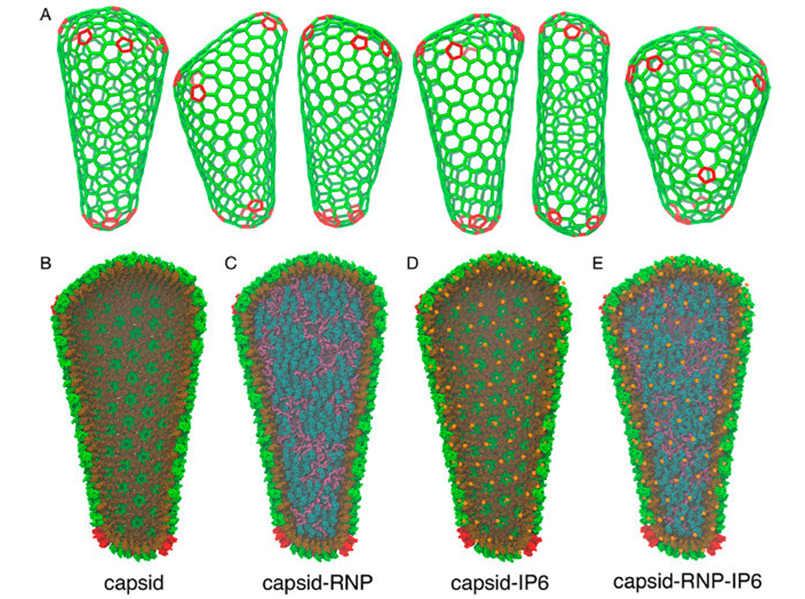
成熟的HIV-1衣壳在大小和形状上有明显的变化,图片来自PNAS, 2022, doi:10.1073/pnas.2117781119。
Voth及其同事们利用从马克斯-普朗克生物化学研究所细胞与病毒结构系的John Brigg博士的实验室获得的实际病毒的低温电子断层扫描数据开始研究。利用这些实验数据,他们开发了一种HIV-1病毒衣壳的全原子分子动力学模拟,接近1亿个原子。
这项新研究中的模拟图片显示了这种病毒衣壳上的条纹,这表明存在应力-应变(stress-strain)。它们准确地指出了这种衣壳上的蛋白晶格发生压缩或膨胀的位置,并且在经历痛苦的应变,这告诉科学家们这种应力-应变并不是完美分布的。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


