2020年6月Science期刊不得不看的亮点研究
来源:本站原创 2020-06-30 23:59
2020年6月30日讯/生物谷BIOON/---2020年6月份即将结束了,6月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
2020年6月30日讯/生物谷BIOON/---2020年6月份即将结束了,6月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:神奇的动物竟能让失去的眼睛重新长出!新研究揭示其中的奥秘
doi:10.1126/science.aba3203; doi:10.1126/science.abc8066
如果在淡水中生活的小型真涡虫地中海圆头涡虫(Schmidtea mediterranea)的眼睛发生了什么意外,它们可以在几天内把眼睛长回来。它们是如何做到这一点的,这是一个科学难题---美国怀特黑德研究所的Peter Reddien实验室多年来一直在研究这个问题。
该实验室的最新项目提供了一些启示:在一项新的研究中,Reddien实验室的研究人员鉴定出一类新的细胞,在这种真涡虫完成重建它的神经回路的困难任务时,这些细胞可能作为一种路标(guidepost),帮助将它的轴突从眼睛引导到大脑中。相关研究结果发表在2020年6月26日的Science期刊上,论文标题为“Muscle and neuronal guidepost-like cells facilitate planarian visual system regeneration”。

真涡虫是研究再生的流行模型,它们可以重新长出身体的几乎任何部分;眼睛是一个有趣的研究部分,这是因为再生视觉系统需要真涡虫重新连接它们的神经元以连接到大脑。
当神经系统在胚胎中发育时,第一批神经纤维,称为先锋轴突(pioneer axon),蜿蜒穿过组织,形成感知和解释外部刺激所需的神经回路。轴突沿途得到称为路标细胞(guidepost cell)的特殊细胞的帮助。这些特殊细胞被安置在选择点--轴突的路径可能会在不同的方向发生分叉的地方。
2.Science:揭示梅斯纳小体感知轻微触觉机制
doi:10.1126/science.abb2751; doi:10.1126/science.abc7610
梅斯纳小体(Meissner corpuscle, 也称为触觉小体)是密集分布在哺乳动物无毛皮肤上的机械感觉末梢器官。梅斯纳小体的基本解剖结构和支配它的Aβ(较大的胞体直径和快速动作电位传导)机械感觉神经元已被广泛描述。然而,人们对梅斯纳小体以及支配它的Aβ 机械感觉神经元在触觉相关行为、感觉运动能力和触觉感知方面的要求却知之甚少。
缺乏脑源性神经营养因子(BDNF)或其受体TrkB的小鼠具有一系列发育障碍,包括缺乏梅斯纳小体。来自美国哈佛医学院和斯坦福大学的研究人员推断,将TrkB操纵限制在感觉神经元与选择性遗传标记方法相结合,将允许他们研究梅斯纳小体的发育组装及其在躯体感觉 中的功能。在研究梅斯纳小体发育时,他们发现有两种类型的Aβ机械感觉神经元支配梅斯纳小体。他们评估了梅斯纳小体对触觉敏感度和精细感觉运动控制的要求,以及支配该机械感觉末端器官的两种Aβ机械感觉神经元的解剖学、生理学和超微结构特性。相关研究结 果发表在2020年6月19日的Science期刊上,论文标题为“Meissner corpuscles and their spatially intermingled afferents underlie gentle touch perception”。
感觉神经元特异性敲除TrkB导致梅斯纳小体完全丧失,而不影响小鼠无毛皮肤的其他机械感觉末端器官,包括Aβ机械感觉神经元-梅克尔细胞复合物和帕西尼小体(Pacinian corpuscle,也称为环层小体)。行为测量表明,缺乏梅斯纳小体的小鼠在感知、对作用于无毛 皮肤的最轻微的可检测力作出的反应和精细的感觉运动控制方面存在缺陷。
遗传标记实验显示,梅斯纳小体由两种类型分子上不同的Aβ感觉神经元支配:一种表达TrkB,另一种表达酪氨酸激酶Ret。尽管支配着同一个末端器官,但是这两种Aβ神经元类型对触觉刺激的反应是不同的:TrkB阳性(TrkB+)的梅斯纳小体传入更敏感,在无毛皮肤的 梯形压痕的起始和偏移时都作出反应,而Ret+ 梅斯纳小体传入则不太敏感,很少在梯形压痕偏移时作出反应。一些Ret+神经元甚至在静态压痕刺激时有持续反应。此外,这两种Aβ机械感觉神经元类型的轴突末端被发现是同型平铺,但异型偏移。计算建模表明,这种解 剖学安排最大限度地提高了编码敏锐度的可用信息,同时确保使用有限数量的神经元完全覆盖皮肤。最后,使用电子显微镜的超微结构分析显示,更敏感的TrkB+梅斯纳小体传入的轴突末梢比不太敏感的Ret+梅斯纳小体传入的轴突末梢具有更多数量的片状细胞包裹。
3.Science:新研究表明通用流感疫苗的设计可能比预期的更具挑战性
doi:10.1126/science.aaz5143
在一项新的研究中,来自美国斯克里普斯研究所、弗雷德-哈金森癌症研究中心、华盛顿大学和中国香港大学的研究人员发现一些常见的流感病毒毒株有可能发生突变来逃避由通用流感疫苗引起的广效抗体。这些研究结果突显了设计这类疫苗面临的挑战,应当有助于指导 疫苗开发。相关研究结果发表在2020年6月19日的Science期刊上,论文标题为“Different genetic barriers for resistance to HA stem antibodies in influenza H3 and H1 viruses”。论文第一作者为斯克里普斯研究所的博士后研究员Nicholas Wu博士和斯克里普 斯研究所的研究员Andrew Thompson博士。
在这项研究中,这些研究人员发现有证据表明,作为最常见的流感病毒亚型之一,H3N2可以相对容易地发生突变,以逃避两种被认为可以阻断几乎所有流感病毒毒株的抗体。不过,他们发现,对另一种常见亚型H1N1来说,要逃脱同样具有广泛中和作用的抗体要困难得多 。
4.Science:新研究首次确定麻疹病毒的起源,从而为探究COVID-19起源提供信息
doi:10.1126/science.aba9411; doi:10.1126/science.abc5746
在一项新的研究中,来自德国、比利时、美国和法国的研究人员解决了麻疹首次出现的时间这个有争议的问题,发现它可能与大城市的崛起有关。他们对来自1912年的一种麻疹病毒毒株的基因组进行了测序,并反向评估了这种病毒可能在人类群体中出现的时间,并将它 确定在公元前6世纪左右。相关研究结果发表在2020年6月19日的Science期刊上,论文标题为“Measles virus and rinderpest virus divergence dated to the sixth century BCE”。
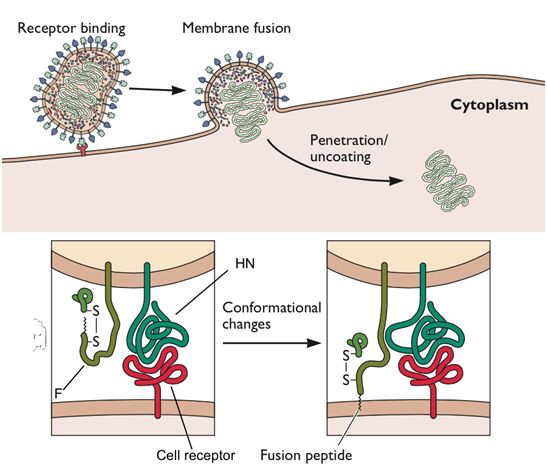
在针对这项研究发表的一篇评论类型文章中,澳大利亚悉尼大学的Simon Ho博士和墨尔本大学的Sebastián Duchêne博士提出类似地完善关于COVID-19和其他人畜共患疾病何时出现的研究将有助于理解这类病原体如何从动物跳跃到人类身上。Ho说,这项研究可能有助于帮 助确定麻疹在人类中出现的时间的努力。
5.Science:我国科学家发现人中和抗体结合SARS-CoV-2刺突蛋白的N端结构域
doi:10.1126/science.abc6952
三聚体刺突蛋白(S蛋白)装饰着冠状病毒的表面,在病毒进入过程中起着关键作用。在感染过程中,S蛋白被宿主蛋白酶(比如TMPRSS2)切割成N端的S1亚基和C端的S2亚基,并从融合前状态转变为融合后状态。S1和S2由胞外结构域(ECD,1-1208个氨基酸)和单个跨膜螺旋组成,分别介导受体结合和膜融合。S1由N端结构域(NTD)和受体结合结构域(RBD)组成,对决定组织嗜性和宿主范围至关重要。RBD负责与ACE2结合,而NTD的功能尚不十分清楚。在一些冠状病毒中,NTD可能在初始附着时识别特定的糖基团,并可能在S蛋白从融合前状态到融合后状态的转变中发挥重要作用。MERS-CoV S蛋白的NTD可以作为中和抗体的关键表位。
具有强效中和活性的靶向SARS-CoV-2 S蛋白的单克隆抗体(mAb)是开发COVID-19治疗干预的一个重点。许多研究报道了靶向RBD和抑制S蛋白与ACE2之间结合的SARS-CoV-2中和抗体的功能和结构。使用单一的RBD靶向抗体可能会诱发冠状病毒产生抵抗性突变。靶向非RBD表位的抗体可能被添加到针对SARS-CoV-2的抗体组合疗法中。
不仅位于S蛋白的RBD上的表位分布,而且位于整个S蛋白上的表位分布都可用来指导开发靶向SARS-CoV-2的治疗性药物。在一项新的研究中,来自中国军事医学科学院、西湖大学和清华大学的研究人员从10名康复期COVID-19患者中分离并描述了mAb。相关研究结果于2020年6月22日在线发表在Science期刊上,论文标题为“A neutralizing human antibody binds to the N-terminal domain of the Spike protein of SARS-CoV-2”。
他们分离出的三种mAb显示出对真正的SARS-CoV-2的中和活性。一种名为4A8的mAb对真正的SARS-CoV-2和SARS-CoV-2假病毒都有较高的中和效力,但并不结合RBD。他们解析出4A8与S蛋白结合在一起时的总体分辨率为3.1埃的低温电镜结构和针对4A8-NTD界面的局部分辨率为3.3埃的低温电镜结构,从而确定4A8的表位为S蛋白的NTD。这表明NTD是针对COVID-19的治疗性mAb的一个有希望的靶点。
6.Science:靶向SARS-CoV-2刺突蛋白的抗体组合可阻止单一抗体治疗时快速产生的逃逸突变
doi:10.1126/science.abd0831
科学家们最近利用基因人源化的小鼠和来自恢复期患者的B细胞,产生了一个非常大的靶向SARS-CoV-2 S蛋白的受体结合结构域(RBD)的高强效全人中和抗体的集合。产生这个非常大的集合的预期目标是筛选成对可以同时结合S蛋白的RBD的高强效抗体,因此它们可能构成治疗性的抗体混合物,不仅可以成为一种有效的治疗,而且也可能防止为了应对单一抗体治疗的选择性压力而产生的病毒逃逸突变体引起的抗体抵抗性。
在一项新的研究中,为了评估再生元制药公司(Regeneron Pharmaceuticals)近期描述的抗病毒抗体对截至2020年3月底已确定的可公开获得的SARS-CoV-2序列(代表超过7000个独特的基因组)所代表的一系列S蛋白RBD突变体的有效性,该公司的研究人员使用了表达这些SARS-CoV-2 S蛋白突变体的VSV假颗粒系统。他们的前八种中和抗体都可有效地抵抗所有测试的突变体,从而展示了对在人类中传播的SARS-CoV-2的广泛覆盖。相关研究结果于2020年6月15日在线发表在Science期刊上,论文标题为“Antibody cocktail to SARS-CoV-2 spike protein prevents rapid mutational escape seen with individual antibodies”。
这项研究描述的数据有力地支持了这样一个概念,即抗体组合疗法可能提供一个强大的方法,以最大限度地减少SARS-CoV-2的突变逃逸;特别是,这些研究人员的研究指出了抗体组合治疗---选择两种结合独特的非重叠的病毒靶标区域(就这项研究而言,S蛋白的RBD),因而需要在两个不同的遗传位点同时发生不太可能发生的突变以便病毒逃逸---的潜在价值。临床候选广效性的选择标准,包括针对自然循环序列变异的功能评估,以及包含具有非重叠表位的多种抗体,可以提供增强的保护,防止疗效丧失。未来的体内动物和人类临床研究需要密切关注可能出现的逃逸突变体和潜在的后续药效损失。广泛强效的候选抗体的临床标准,包括针对自然循环序列变异的功能评估,以及包含多种结合表位不存在重叠的抗体,可能提供增强的保护,防止失效。未来的体内动物和人体临床研究需要密切关注可能出现的逃逸突变体以及随后可能发生的药物疗效丧失。
7.Science:揭示金丝雀羽毛颜色性别双色性的遗传机制
doi:10.1126/science.aba0803; doi:10.1126/science.abc2242
在一项新的研究中,来自葡萄牙波尔图大学、科英布拉大学、美国华盛顿大学、塔尔萨大学和奥本大学的研究人员发现一种酶导致马赛克金丝雀(mosaic canaries)羽毛颜色性别差异。相关研究结果发表在2020年6月12日的Science期刊上,论文标题为“A genetic mechanism for sexual dichromatism in birds”。在这篇论文中,他们描述了他们如何缩小对影响金丝雀颜色性别差异的因素的搜索范围,以及他们取得的发现。在同期Science期刊上,美国罗彻斯特大学的Nancy Chen针对这项研究发表了一篇观点类型(Perspective)的文章,详细介绍了鸟类颜色性别差异的研究历史,并概述了这项新研究取得的成果。
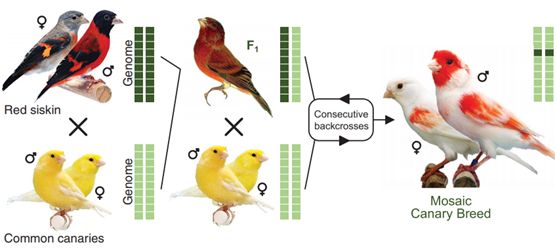
这些研究人员研究了红鶸金丝雀(red siskin canaries)和普通金丝雀(common canaries)。红鶸金丝雀具有性别二色性(sexual dichromatism),而雄性和雌性普通金丝雀具有相同的颜色。它们杂交后产生的后代称为马赛克金丝雀。这两种鸟类进行杂交,是为了帮助这些研究人员确定产生性别特异性羽毛颜色差异的基因---马赛克金丝雀是性别二色性的。然后,他们反复将马赛克金丝雀与普通金丝雀进行杂交,以缩小潜在的基因范围。
这些研究人员通过研究后代的基因表达模式,进一步缩小了潜在的基因列表。这种方法让他们缩小潜在的基因列表,直到只剩下一个基因:BCO2,它编码一种称为β-胡萝卜素氧合酶2(β-carotene oxygenase 2, BCO2)的酶。这项研究发现,它在分解鸟类羽毛中产生颜色的红橙色色素β-胡萝卜素的过程中发挥了作用。他们发现,雄性和雌性马赛克金丝雀之间的区别在于BCO2酶产生的数量。因此,雌鸟马赛克金丝雀的颜色较少,这是因为它们更多的红橙色色素β-胡萝卜素被分解,留给羽毛着色的β-胡萝卜素较少。他们猜测雌激素可能在BCO2基因的表达中起作用,这有助于解释羽毛着色的性别差异。
8.Science:重大突破!科学家开发出一种超快速的CRISPR-Cas9基因编辑技术 能在几秒钟内实现精准基因编辑!
doi:10.1126/science.aay8204; doi:10.1126/science.abc3997
近日,一项刊登在国际杂志Science上的研究报告中,来自约翰霍普金斯大学等机构的科学家们通过研究利用光敏核苷酸开发了一种新方法来加速CRISPR-Cas9基因编辑的过程,文章中,研究者描述了整个实验过程及其这种新方法的精准性;在Science杂志同一期的一篇展望文章中,来自纪念斯隆凯特琳癌症中心的科学家们还概述了CRISPR-Cas9基因编辑技术的进化历程。
在CRISPR-Cas9基因编辑过程中,酶类Cas9能被用作剪刀在基因编辑的特定位点切割DNA链,同时导向RNA分子则会帮助Cas9酶类结合到预想链的DNA位点上,目前该过程的部分流程需要几个小时才能完成,这项研究中,研究人员能将整个过程缩短到几秒钟时间。
文章中,研究人员通过添加光敏核苷酸分子来改变部分导向RNA的序列,这就会阻断导向RNA在光被引入之前完成其工作,一旦研究者引入光,结合过程就会在几秒内发生,研究者将这种方法称之为“笼中法”(caged approach),因为导向RNA分子会被限制,直至其被指示去完成它的工作,研究者将这种方法称之为超快速CRISPR基因编辑手段(vfCRISPR)。
研究者指出,推迟编辑过程随后迅速对其激活,这或许就能为详细研究该过程提供一定的可能性,同时这种新方法还能提高基因编辑的精准性,并能允许一次编辑单个等位基因;同时,这种新方法还能帮助研究者开发出杂合突变,并以新的方法来研究复杂的特性,最后研究者Medhi表示,文章中我们描述了如何将CRISPR-Cas9工具从一种钝化的工具转变为一种精确的工具,vfCRISPR技术似乎是一项变革性的科学进步,因为其能帮助研究人员更好地理解基因编辑过程中参与双链断裂的细胞反应的动力学变化。
9.Science重磅!人类大脑基因触发猴子长出更大的大脑
doi:10.1126/science.abb2401
人类大脑在进化过程中的扩张,特别是新大脑皮层的扩张,与诸如推理和语言等认知能力有关。有一种叫做ARHGAP11B的基因,只在人类身上表达,它能触发大脑干细胞形成更多的干细胞,这是大脑更大的先决条件。过去的研究表明,当ARHGAP11B在小鼠和雪貂体内表达到非生理上的高水平时,会导致新大脑皮层的扩张,但它与灵长类进化的相关性尚不清楚。
马克斯普朗克研究所分子细胞生物学和遗传学研究所(MPI-CBG)的研究员与日本川崎中央研究所实验动物(CIEA)和庆应义塾大学的同事合作发现,当狨猴体内的这个基因表达到人体生理水平时,会引起大脑皮层肿大。这表明ARHGAP11B基因可能在人类进化过程中导致了大脑皮层的扩张。研究人员在《科学》(Science)杂志上发表了他们的研究结果,题为"Human-specific ARHGAP11B increases size and folding of primate neocortex in the fetal marmoset"。
"人类的新大脑皮层是进化中最年轻的大脑皮层,它比人类的近亲黑猩猩的大脑皮层大三倍。在进化过程中,新大脑皮层的褶皱增加,以适应有限的颅骨空间。对科学家来说,一个关键问题是人类的新大脑皮层是如何变得如此巨大的。在2015年的一项研究中,MPI-CBG的创始主任Wieland Huttner的研究小组发现,在人类特异性基因ARHGAP11B的影响下,小鼠胚胎产生了更多的神经祖细胞,甚至可以折叠正常展开的新皮层。结果表明,ARHGAP11B基因在人类新皮层的进化扩展中起着关键作用。
10.Science:干扰素IFN-λ在COVID-19中有益还是有害?新研究发现它在识别病毒后会破坏肺部表面屏障
doi:10.1126/science.abc3545
免疫系统产生的干扰素和其他细胞因子是抵御病毒感染的重要防御手段,但正如我们在COVID-19中看到的那样,它们也会导致破坏性的、可能危及生命的肺部炎症。最近的证据提示着一种称为III型干扰素或干扰素λ(IFN-λ)的干扰素可以对抗病毒感染,同时限制这种炎症损伤。这导致人们开展临床试验来测试III型干扰素是否可用来治疗COVID-19。
不过,在一项新的研究中,来自意大利和美国的研究人员提供证据表明III型干扰素可以增加肺部出现危及生命的细菌“超级感染”风险。在流感和COVID-19中均可发生超级感染。这些研究人员提醒道,在COVID-19病程后期给予III型干扰素可能弊大于利。相关研究结果于2020年6月11日在线发表在Science期刊上,论文标题为“Type III interferons disrupt the lung epithelial barrier upon viral recognition”。
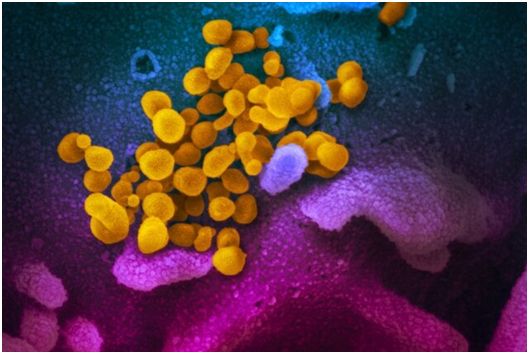
论文通讯作者、美国波士顿儿童医院免疫学家Ivan Zanoni博士说,“我们的数据表明,SARS-CoV-2抑制了上呼吸道中干扰素的产生,削弱了免疫反应,帮助这种冠状病毒存活。但是,当这种冠状病毒到达下呼吸道时,会出现旺盛的免疫反应,包括Ⅲ型干扰素上调,我们认为这是有害的。”(生物谷 Bioon.com)
1.Science:神奇的动物竟能让失去的眼睛重新长出!新研究揭示其中的奥秘
doi:10.1126/science.aba3203; doi:10.1126/science.abc8066
如果在淡水中生活的小型真涡虫地中海圆头涡虫(Schmidtea mediterranea)的眼睛发生了什么意外,它们可以在几天内把眼睛长回来。它们是如何做到这一点的,这是一个科学难题---美国怀特黑德研究所的Peter Reddien实验室多年来一直在研究这个问题。
该实验室的最新项目提供了一些启示:在一项新的研究中,Reddien实验室的研究人员鉴定出一类新的细胞,在这种真涡虫完成重建它的神经回路的困难任务时,这些细胞可能作为一种路标(guidepost),帮助将它的轴突从眼睛引导到大脑中。相关研究结果发表在2020年6月26日的Science期刊上,论文标题为“Muscle and neuronal guidepost-like cells facilitate planarian visual system regeneration”。

图片来自Science, 2020, doi:10.1126/science.aba3203。
真涡虫是研究再生的流行模型,它们可以重新长出身体的几乎任何部分;眼睛是一个有趣的研究部分,这是因为再生视觉系统需要真涡虫重新连接它们的神经元以连接到大脑。
当神经系统在胚胎中发育时,第一批神经纤维,称为先锋轴突(pioneer axon),蜿蜒穿过组织,形成感知和解释外部刺激所需的神经回路。轴突沿途得到称为路标细胞(guidepost cell)的特殊细胞的帮助。这些特殊细胞被安置在选择点--轴突的路径可能会在不同的方向发生分叉的地方。
2.Science:揭示梅斯纳小体感知轻微触觉机制
doi:10.1126/science.abb2751; doi:10.1126/science.abc7610
梅斯纳小体(Meissner corpuscle, 也称为触觉小体)是密集分布在哺乳动物无毛皮肤上的机械感觉末梢器官。梅斯纳小体的基本解剖结构和支配它的Aβ(较大的胞体直径和快速动作电位传导)机械感觉神经元已被广泛描述。然而,人们对梅斯纳小体以及支配它的Aβ 机械感觉神经元在触觉相关行为、感觉运动能力和触觉感知方面的要求却知之甚少。
缺乏脑源性神经营养因子(BDNF)或其受体TrkB的小鼠具有一系列发育障碍,包括缺乏梅斯纳小体。来自美国哈佛医学院和斯坦福大学的研究人员推断,将TrkB操纵限制在感觉神经元与选择性遗传标记方法相结合,将允许他们研究梅斯纳小体的发育组装及其在躯体感觉 中的功能。在研究梅斯纳小体发育时,他们发现有两种类型的Aβ机械感觉神经元支配梅斯纳小体。他们评估了梅斯纳小体对触觉敏感度和精细感觉运动控制的要求,以及支配该机械感觉末端器官的两种Aβ机械感觉神经元的解剖学、生理学和超微结构特性。相关研究结 果发表在2020年6月19日的Science期刊上,论文标题为“Meissner corpuscles and their spatially intermingled afferents underlie gentle touch perception”。
感觉神经元特异性敲除TrkB导致梅斯纳小体完全丧失,而不影响小鼠无毛皮肤的其他机械感觉末端器官,包括Aβ机械感觉神经元-梅克尔细胞复合物和帕西尼小体(Pacinian corpuscle,也称为环层小体)。行为测量表明,缺乏梅斯纳小体的小鼠在感知、对作用于无毛 皮肤的最轻微的可检测力作出的反应和精细的感觉运动控制方面存在缺陷。
遗传标记实验显示,梅斯纳小体由两种类型分子上不同的Aβ感觉神经元支配:一种表达TrkB,另一种表达酪氨酸激酶Ret。尽管支配着同一个末端器官,但是这两种Aβ神经元类型对触觉刺激的反应是不同的:TrkB阳性(TrkB+)的梅斯纳小体传入更敏感,在无毛皮肤的 梯形压痕的起始和偏移时都作出反应,而Ret+ 梅斯纳小体传入则不太敏感,很少在梯形压痕偏移时作出反应。一些Ret+神经元甚至在静态压痕刺激时有持续反应。此外,这两种Aβ机械感觉神经元类型的轴突末端被发现是同型平铺,但异型偏移。计算建模表明,这种解 剖学安排最大限度地提高了编码敏锐度的可用信息,同时确保使用有限数量的神经元完全覆盖皮肤。最后,使用电子显微镜的超微结构分析显示,更敏感的TrkB+梅斯纳小体传入的轴突末梢比不太敏感的Ret+梅斯纳小体传入的轴突末梢具有更多数量的片状细胞包裹。
3.Science:新研究表明通用流感疫苗的设计可能比预期的更具挑战性
doi:10.1126/science.aaz5143
在一项新的研究中,来自美国斯克里普斯研究所、弗雷德-哈金森癌症研究中心、华盛顿大学和中国香港大学的研究人员发现一些常见的流感病毒毒株有可能发生突变来逃避由通用流感疫苗引起的广效抗体。这些研究结果突显了设计这类疫苗面临的挑战,应当有助于指导 疫苗开发。相关研究结果发表在2020年6月19日的Science期刊上,论文标题为“Different genetic barriers for resistance to HA stem antibodies in influenza H3 and H1 viruses”。论文第一作者为斯克里普斯研究所的博士后研究员Nicholas Wu博士和斯克里普 斯研究所的研究员Andrew Thompson博士。
在这项研究中,这些研究人员发现有证据表明,作为最常见的流感病毒亚型之一,H3N2可以相对容易地发生突变,以逃避两种被认为可以阻断几乎所有流感病毒毒株的抗体。不过,他们发现,对另一种常见亚型H1N1来说,要逃脱同样具有广泛中和作用的抗体要困难得多 。
4.Science:新研究首次确定麻疹病毒的起源,从而为探究COVID-19起源提供信息
doi:10.1126/science.aba9411; doi:10.1126/science.abc5746
在一项新的研究中,来自德国、比利时、美国和法国的研究人员解决了麻疹首次出现的时间这个有争议的问题,发现它可能与大城市的崛起有关。他们对来自1912年的一种麻疹病毒毒株的基因组进行了测序,并反向评估了这种病毒可能在人类群体中出现的时间,并将它 确定在公元前6世纪左右。相关研究结果发表在2020年6月19日的Science期刊上,论文标题为“Measles virus and rinderpest virus divergence dated to the sixth century BCE”。

大脑中的麻疹病毒。
在针对这项研究发表的一篇评论类型文章中,澳大利亚悉尼大学的Simon Ho博士和墨尔本大学的Sebastián Duchêne博士提出类似地完善关于COVID-19和其他人畜共患疾病何时出现的研究将有助于理解这类病原体如何从动物跳跃到人类身上。Ho说,这项研究可能有助于帮 助确定麻疹在人类中出现的时间的努力。
5.Science:我国科学家发现人中和抗体结合SARS-CoV-2刺突蛋白的N端结构域
doi:10.1126/science.abc6952
三聚体刺突蛋白(S蛋白)装饰着冠状病毒的表面,在病毒进入过程中起着关键作用。在感染过程中,S蛋白被宿主蛋白酶(比如TMPRSS2)切割成N端的S1亚基和C端的S2亚基,并从融合前状态转变为融合后状态。S1和S2由胞外结构域(ECD,1-1208个氨基酸)和单个跨膜螺旋组成,分别介导受体结合和膜融合。S1由N端结构域(NTD)和受体结合结构域(RBD)组成,对决定组织嗜性和宿主范围至关重要。RBD负责与ACE2结合,而NTD的功能尚不十分清楚。在一些冠状病毒中,NTD可能在初始附着时识别特定的糖基团,并可能在S蛋白从融合前状态到融合后状态的转变中发挥重要作用。MERS-CoV S蛋白的NTD可以作为中和抗体的关键表位。
具有强效中和活性的靶向SARS-CoV-2 S蛋白的单克隆抗体(mAb)是开发COVID-19治疗干预的一个重点。许多研究报道了靶向RBD和抑制S蛋白与ACE2之间结合的SARS-CoV-2中和抗体的功能和结构。使用单一的RBD靶向抗体可能会诱发冠状病毒产生抵抗性突变。靶向非RBD表位的抗体可能被添加到针对SARS-CoV-2的抗体组合疗法中。
不仅位于S蛋白的RBD上的表位分布,而且位于整个S蛋白上的表位分布都可用来指导开发靶向SARS-CoV-2的治疗性药物。在一项新的研究中,来自中国军事医学科学院、西湖大学和清华大学的研究人员从10名康复期COVID-19患者中分离并描述了mAb。相关研究结果于2020年6月22日在线发表在Science期刊上,论文标题为“A neutralizing human antibody binds to the N-terminal domain of the Spike protein of SARS-CoV-2”。
他们分离出的三种mAb显示出对真正的SARS-CoV-2的中和活性。一种名为4A8的mAb对真正的SARS-CoV-2和SARS-CoV-2假病毒都有较高的中和效力,但并不结合RBD。他们解析出4A8与S蛋白结合在一起时的总体分辨率为3.1埃的低温电镜结构和针对4A8-NTD界面的局部分辨率为3.3埃的低温电镜结构,从而确定4A8的表位为S蛋白的NTD。这表明NTD是针对COVID-19的治疗性mAb的一个有希望的靶点。
6.Science:靶向SARS-CoV-2刺突蛋白的抗体组合可阻止单一抗体治疗时快速产生的逃逸突变
doi:10.1126/science.abd0831
科学家们最近利用基因人源化的小鼠和来自恢复期患者的B细胞,产生了一个非常大的靶向SARS-CoV-2 S蛋白的受体结合结构域(RBD)的高强效全人中和抗体的集合。产生这个非常大的集合的预期目标是筛选成对可以同时结合S蛋白的RBD的高强效抗体,因此它们可能构成治疗性的抗体混合物,不仅可以成为一种有效的治疗,而且也可能防止为了应对单一抗体治疗的选择性压力而产生的病毒逃逸突变体引起的抗体抵抗性。
在一项新的研究中,为了评估再生元制药公司(Regeneron Pharmaceuticals)近期描述的抗病毒抗体对截至2020年3月底已确定的可公开获得的SARS-CoV-2序列(代表超过7000个独特的基因组)所代表的一系列S蛋白RBD突变体的有效性,该公司的研究人员使用了表达这些SARS-CoV-2 S蛋白突变体的VSV假颗粒系统。他们的前八种中和抗体都可有效地抵抗所有测试的突变体,从而展示了对在人类中传播的SARS-CoV-2的广泛覆盖。相关研究结果于2020年6月15日在线发表在Science期刊上,论文标题为“Antibody cocktail to SARS-CoV-2 spike protein prevents rapid mutational escape seen with individual antibodies”。
这项研究描述的数据有力地支持了这样一个概念,即抗体组合疗法可能提供一个强大的方法,以最大限度地减少SARS-CoV-2的突变逃逸;特别是,这些研究人员的研究指出了抗体组合治疗---选择两种结合独特的非重叠的病毒靶标区域(就这项研究而言,S蛋白的RBD),因而需要在两个不同的遗传位点同时发生不太可能发生的突变以便病毒逃逸---的潜在价值。临床候选广效性的选择标准,包括针对自然循环序列变异的功能评估,以及包含具有非重叠表位的多种抗体,可以提供增强的保护,防止疗效丧失。未来的体内动物和人类临床研究需要密切关注可能出现的逃逸突变体和潜在的后续药效损失。广泛强效的候选抗体的临床标准,包括针对自然循环序列变异的功能评估,以及包含多种结合表位不存在重叠的抗体,可能提供增强的保护,防止失效。未来的体内动物和人体临床研究需要密切关注可能出现的逃逸突变体以及随后可能发生的药物疗效丧失。
7.Science:揭示金丝雀羽毛颜色性别双色性的遗传机制
doi:10.1126/science.aba0803; doi:10.1126/science.abc2242
在一项新的研究中,来自葡萄牙波尔图大学、科英布拉大学、美国华盛顿大学、塔尔萨大学和奥本大学的研究人员发现一种酶导致马赛克金丝雀(mosaic canaries)羽毛颜色性别差异。相关研究结果发表在2020年6月12日的Science期刊上,论文标题为“A genetic mechanism for sexual dichromatism in birds”。在这篇论文中,他们描述了他们如何缩小对影响金丝雀颜色性别差异的因素的搜索范围,以及他们取得的发现。在同期Science期刊上,美国罗彻斯特大学的Nancy Chen针对这项研究发表了一篇观点类型(Perspective)的文章,详细介绍了鸟类颜色性别差异的研究历史,并概述了这项新研究取得的成果。

图片来自Science, 2020, doi:10.1126/science.aba0803。
这些研究人员研究了红鶸金丝雀(red siskin canaries)和普通金丝雀(common canaries)。红鶸金丝雀具有性别二色性(sexual dichromatism),而雄性和雌性普通金丝雀具有相同的颜色。它们杂交后产生的后代称为马赛克金丝雀。这两种鸟类进行杂交,是为了帮助这些研究人员确定产生性别特异性羽毛颜色差异的基因---马赛克金丝雀是性别二色性的。然后,他们反复将马赛克金丝雀与普通金丝雀进行杂交,以缩小潜在的基因范围。
这些研究人员通过研究后代的基因表达模式,进一步缩小了潜在的基因列表。这种方法让他们缩小潜在的基因列表,直到只剩下一个基因:BCO2,它编码一种称为β-胡萝卜素氧合酶2(β-carotene oxygenase 2, BCO2)的酶。这项研究发现,它在分解鸟类羽毛中产生颜色的红橙色色素β-胡萝卜素的过程中发挥了作用。他们发现,雄性和雌性马赛克金丝雀之间的区别在于BCO2酶产生的数量。因此,雌鸟马赛克金丝雀的颜色较少,这是因为它们更多的红橙色色素β-胡萝卜素被分解,留给羽毛着色的β-胡萝卜素较少。他们猜测雌激素可能在BCO2基因的表达中起作用,这有助于解释羽毛着色的性别差异。
8.Science:重大突破!科学家开发出一种超快速的CRISPR-Cas9基因编辑技术 能在几秒钟内实现精准基因编辑!
doi:10.1126/science.aay8204; doi:10.1126/science.abc3997
近日,一项刊登在国际杂志Science上的研究报告中,来自约翰霍普金斯大学等机构的科学家们通过研究利用光敏核苷酸开发了一种新方法来加速CRISPR-Cas9基因编辑的过程,文章中,研究者描述了整个实验过程及其这种新方法的精准性;在Science杂志同一期的一篇展望文章中,来自纪念斯隆凯特琳癌症中心的科学家们还概述了CRISPR-Cas9基因编辑技术的进化历程。
在CRISPR-Cas9基因编辑过程中,酶类Cas9能被用作剪刀在基因编辑的特定位点切割DNA链,同时导向RNA分子则会帮助Cas9酶类结合到预想链的DNA位点上,目前该过程的部分流程需要几个小时才能完成,这项研究中,研究人员能将整个过程缩短到几秒钟时间。
文章中,研究人员通过添加光敏核苷酸分子来改变部分导向RNA的序列,这就会阻断导向RNA在光被引入之前完成其工作,一旦研究者引入光,结合过程就会在几秒内发生,研究者将这种方法称之为“笼中法”(caged approach),因为导向RNA分子会被限制,直至其被指示去完成它的工作,研究者将这种方法称之为超快速CRISPR基因编辑手段(vfCRISPR)。
研究者指出,推迟编辑过程随后迅速对其激活,这或许就能为详细研究该过程提供一定的可能性,同时这种新方法还能提高基因编辑的精准性,并能允许一次编辑单个等位基因;同时,这种新方法还能帮助研究者开发出杂合突变,并以新的方法来研究复杂的特性,最后研究者Medhi表示,文章中我们描述了如何将CRISPR-Cas9工具从一种钝化的工具转变为一种精确的工具,vfCRISPR技术似乎是一项变革性的科学进步,因为其能帮助研究人员更好地理解基因编辑过程中参与双链断裂的细胞反应的动力学变化。
9.Science重磅!人类大脑基因触发猴子长出更大的大脑
doi:10.1126/science.abb2401
人类大脑在进化过程中的扩张,特别是新大脑皮层的扩张,与诸如推理和语言等认知能力有关。有一种叫做ARHGAP11B的基因,只在人类身上表达,它能触发大脑干细胞形成更多的干细胞,这是大脑更大的先决条件。过去的研究表明,当ARHGAP11B在小鼠和雪貂体内表达到非生理上的高水平时,会导致新大脑皮层的扩张,但它与灵长类进化的相关性尚不清楚。
马克斯普朗克研究所分子细胞生物学和遗传学研究所(MPI-CBG)的研究员与日本川崎中央研究所实验动物(CIEA)和庆应义塾大学的同事合作发现,当狨猴体内的这个基因表达到人体生理水平时,会引起大脑皮层肿大。这表明ARHGAP11B基因可能在人类进化过程中导致了大脑皮层的扩张。研究人员在《科学》(Science)杂志上发表了他们的研究结果,题为"Human-specific ARHGAP11B increases size and folding of primate neocortex in the fetal marmoset"。
"人类的新大脑皮层是进化中最年轻的大脑皮层,它比人类的近亲黑猩猩的大脑皮层大三倍。在进化过程中,新大脑皮层的褶皱增加,以适应有限的颅骨空间。对科学家来说,一个关键问题是人类的新大脑皮层是如何变得如此巨大的。在2015年的一项研究中,MPI-CBG的创始主任Wieland Huttner的研究小组发现,在人类特异性基因ARHGAP11B的影响下,小鼠胚胎产生了更多的神经祖细胞,甚至可以折叠正常展开的新皮层。结果表明,ARHGAP11B基因在人类新皮层的进化扩展中起着关键作用。
10.Science:干扰素IFN-λ在COVID-19中有益还是有害?新研究发现它在识别病毒后会破坏肺部表面屏障
doi:10.1126/science.abc3545
免疫系统产生的干扰素和其他细胞因子是抵御病毒感染的重要防御手段,但正如我们在COVID-19中看到的那样,它们也会导致破坏性的、可能危及生命的肺部炎症。最近的证据提示着一种称为III型干扰素或干扰素λ(IFN-λ)的干扰素可以对抗病毒感染,同时限制这种炎症损伤。这导致人们开展临床试验来测试III型干扰素是否可用来治疗COVID-19。
不过,在一项新的研究中,来自意大利和美国的研究人员提供证据表明III型干扰素可以增加肺部出现危及生命的细菌“超级感染”风险。在流感和COVID-19中均可发生超级感染。这些研究人员提醒道,在COVID-19病程后期给予III型干扰素可能弊大于利。相关研究结果于2020年6月11日在线发表在Science期刊上,论文标题为“Type III interferons disrupt the lung epithelial barrier upon viral recognition”。

图片来自NIAID-RML。
论文通讯作者、美国波士顿儿童医院免疫学家Ivan Zanoni博士说,“我们的数据表明,SARS-CoV-2抑制了上呼吸道中干扰素的产生,削弱了免疫反应,帮助这种冠状病毒存活。但是,当这种冠状病毒到达下呼吸道时,会出现旺盛的免疫反应,包括Ⅲ型干扰素上调,我们认为这是有害的。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


