全球血友病基因疗法!欧盟授予valrox加速评估:治疗A型血友病,单次输注后5年,年均出血率↓95%!
来源:本站原创 2021-05-31 19:31
valrox用于治疗A型血友病,是进入监管审查的第一款血友病基因疗法。

2021年05月31日讯 /生物谷BIOON/ --BioMarin是一家全球性的生物技术公司,专注于开发治疗严重且危及生命的罕见和超罕见遗传疾病的创新疗法。近日,该公司宣布,欧洲药品管理局(EMA)已批准了对valoctocogene roxaparvovec(valrox,BMN270)进行加速评估的请求。valrox是一款一次性的基因疗法,单次输注治疗重度A型血友病成人患者。加速评估将缩短EMA人用医药产品委员会(CHMP)和先进疗法委员会(CAT)审查valrox营销授权申请(MAA)的时间框架。CHMP的意见预计在2022年上半年公布。
在欧洲,BioMarin计划根据今年早些时候EMA的积极反馈,在2021年6月提交一份valrox治疗重度A型血友病的营销授权申请(MAA),该申请将包括3期GENEr8-1研究的52周数据,以及正在进行的1/2期剂量递增研究中各剂量组的4年和3年随访。
如果CHMP和CAT认为产品对公众健康有重大意义,特别是从治疗创新的角度来看,则产品MAA将有资格进行加速评估。根据EMA集中程序评估MAA可能需要210天,不包括申请人被要求提供额外信息时的时钟停止。根据要求,CHMP和CAT可将时间框架缩短至150天,前提是申请人提供了加速评估的充分理由,尽管最初指定用于加速评估的申请可在审查期间因各种原因恢复到标准程序。批准加速评估的决定对CHMP和CAT关于是否应批准营销授权的最终意见没有影响。
在美国,BioMarin计划提交GENEr8-1研究中所有患者的2年随访安全性和有效性数据,以响应FDA对这些数据的要求,支持该机构对valrox进行的益处/风险评估。BioMarin的目标是2022年第二季度向美国FDA提交生物制品许可申请(BLA),前提是研究结果良好,随后FDA将进行为期6个月的优先审查程序。
BioMarin全球研发总裁Hank Fuchs医学博士表示:“BioMarin很高兴EMA批准了对valrox的加速评估,这认可了该药的治疗创新潜力和解决显著未满足医疗需求的潜力。我们将继续与EMA密切合作,尽快推出第一款治疗A型血友病的基因疗法。”
A型血友病也被称为因子VIII(FIII)缺乏或经典血友病,是一种由凝血因子VIII缺失或缺陷引起的X连锁遗传病,患者会反复发生持续或自发性出血,特别是在关节、肌肉或内脏器官中,长期可导致残疾。目前,重度A型血友病的护理标准是每周2-3次静脉输注凝血因子VIII的预防性治疗方案。
valrox是一种基于腺相关病毒(AAV)的基因疗法,开发用于A型血友病的治疗。该疗法通过向患者体内递送凝血因子VIII功能基因,恢复VIII的产生,从而消除或减少静脉VIII输注需求。如果获批,valrox将标志着A型血友病治疗的一个重大里程碑,这种开创性的疗法,有潜力使患者实现“一劳永逸”的治疗效果。
valrox是全球进入监管审查的第一款血友病基因疗法,用于治疗重度A型血友病成人患者。此前,valrox已被美国FDA授予突破性药物资格(BTD)和再生医学先进治疗产品(RMAT)、被欧盟EMA授予优先药物资格(PRIME)、被FDA和EMA授予孤儿药资格(ODD)。
然而,在2020年8月和9月,valrox在美欧监管方面均遭遇阻碍,要求提供3期临床试验的更多数据。
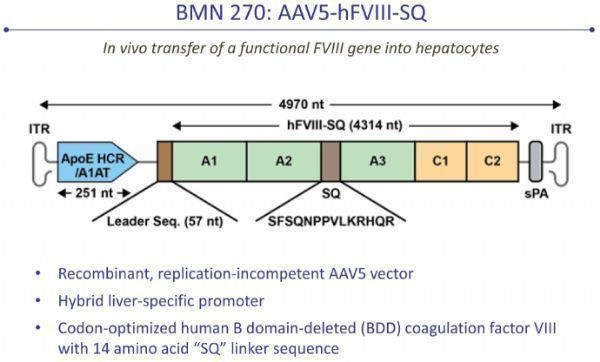
valoctocogene roxaparvovec(valrox,BMN270)
今年5月19日,BioMarin公布了valrox单次输注治疗重度A型血友病成人患者一项开放标签1/2期研究的最新结果。此次公布的长达5年的临床数据,代表着A型血友病基因治疗方面的最长临床经验。
对6e13 vg/kg队列和4e13 vg/kg队列分别进行的5年和4年治疗后随访显示,valrox具有持续的治疗益处。2个队列中的所有患者均保持不使用预防性因子VIII治疗。6e13 vg/kg队列平均累积年化出血率(ABR)仍低于1,并大大低于治疗前的基线水平;与输注前相比,6e13 vg/kg队列第5年的平均ABR为0.7,5年内ABR降低95%,因子VIII使用减少96%。4e13 vg/kg队列第4年的平均ABR为1.7,与输注前相比,4年内ABR降低92%,因子VIII使用减少95%。因子VIII活性水平下降与最近几年的观察结果相当,并继续保持在可提供止血效果的范围内。
总的来说,valrox的安全性与先前报道的数据一致,没有出现迟发性治疗相关不良事件。从第一年开始,所有患者继续停用皮质类固醇。没有患者体内产生因子VIII抑制剂,也没有患者退出研究。没有患者出现血栓性事件。与valrox相关的最常见不良事件发生在单次输注后的早期,包括短暂的输注相关反应和肝功能测试中测定的某些蛋白质和酶水平的短暂、无症状和轻度至中度升高,没有长期的临床后遗症。(生物谷Bioon.com)
原文出处:European Medicines Agency Grants BioMarin's Request for Accelerated Assessment of Valoctocogene Roxaparvovec for Treatment of Severe Hemophilia A
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


