Signal Transduction and Targeted Therapy:mRNA疫苗可增强对SARS-CoV-2变异株的免疫应答
来源:本站原创 2021-07-21 11:58
在最近发表在《科学》杂志上的一篇文章中,Stamatos等人表明,接种含有SARS-CoV-2病毒祖先形式的mRNA疫苗可以增强由该形式感染引起的交叉变异中和抗体,并在较小程度上诱导这种交叉变异抗体。图片来源:https://doi.org/10.1038/s41392-021-00681-6当前全球公共卫生关注的一个主要问题是,新出现的SARS-CoV-2
在最近发表在《科学》杂志上的一篇文章中,Stamatos等人表明,接种含有SARS-CoV-2病毒祖先形式的mRNA疫苗可以增强由该形式感染引起的交叉变异中和抗体,并在较小程度上诱导这种交叉变异抗体。
图片来源:https://doi.org/10.1038/s41392-021-00681-6
当前全球公共卫生关注的一个主要问题是,新出现的SARS-CoV-2变异病毒是否会失去通过编码病毒刺突蛋白的RNA或提供相同靶点的腺病毒载体介导疫苗的预防性接种所提供的对疾病的极佳保护。Stamatatos等人最近的一篇论文在一定程度上回答了这个问题,但好消息和坏消息都有。他们检测了13名sars-cov-2未接种的个体,两次接种了辉瑞/生物科技公司的BNT162b2或Moderna
mRNA-1273 RNA产品,重点研究抗体反应。这两种RNA疫苗都编码2019年12月分离的原始武汉-hu-1变种的刺突蛋白,预计将引发类似或相同的反应。这里提出的一个重要问题是,针对这种祖先形式产生的抗体是否会与B.1.351变体发生交叉反应,这种变体最初出现在南非,此后迅速传播,在许多国家取代了原始血统。通过测定IgG、IgA和IgM抗体滴度,以及对“武汉-hu-1”和“B.1.351”假病毒的中和能力来评估应答。将这些参数与15名从SARS-CoV-2确诊感染中康复并在单次mRNA疫苗接种前后血清中有抗体的人的抗刺抗体的行为进行了比较。
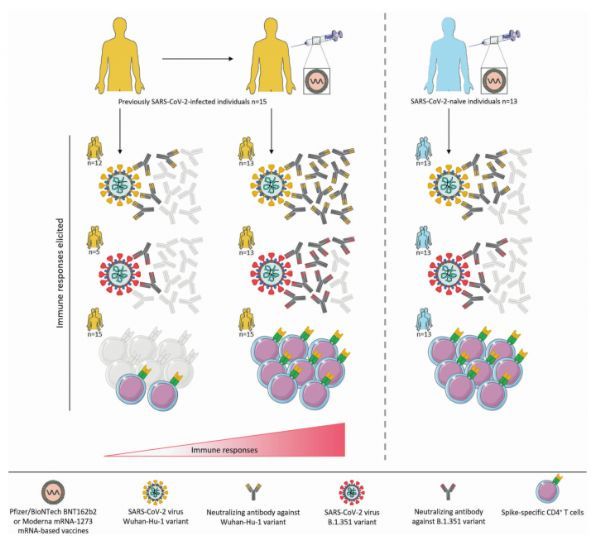
本研究中有几个重要的观察结果:(1)对既往未接触过病毒的个体接种两剂mRNA疫苗后,可产生抗B.1.351变异株的中和抗体,但效价远低于其祖先的武汉-hu -1变异株;(2)在既往感染者中,只有1/3的人有抗B-1351的中和抗体,而有80%的人有对武汉-HU-1的中和抗体,武汉-HU-1可能就是他们感染的那个毒株;(3)用mRNA疫苗免疫后,87%的既往感染者的抗体效价升高,但对B.1.351的抗体效价又低于武汉-HU1;(4)既往无中和抗体的感染者免疫后不产生这种抗体,与缺乏记忆B细胞特异性刺激性蛋白有关;(5)虽然已鉴定的交叉中和抗体针对受体结合区,但N端结构域的突变也影响了变异体对中和的敏感性;(6)重要的但没有详细研究的是,所有以前感染的供者中都存在棘波特异性的CD4+T细胞,并在接种疫苗后得到增强;(7)更重要的是,在两次接种疫苗的未感染个体中,检测到同样高水平的棘波特异性CD4+T细胞。
SARS-CoV-2变异体的免疫应答在mRNA免疫后被激发,并且在先前感染SARS-CoV-2的个体和接种后康复的个体中进一步增强
图片来源:https://doi.org/10.1038/s41392-021-00681-6
研究参与者的选择是基于可获得性,没有特定的纳入或排除标准。尽管如此,也可能是由于这些限制,该研究指出,SARS-CoV-2反应可能在人群中普遍存在,同时为我们了解自然感染和疫苗免疫反应的异质性增加了重要数据,这需要进一步探索。另一方面,Stamatatos等人只测试了B1.351变种,但还有其他已知的和正在出现的变种。然而,B.1.1.7和B1.351的变体有几个关键的突变,特别是在刺突受体结合域和影响病毒粒子上刺突密度的突变,这表明除B.1.351外,至少在其他变体上存在交叉反应。这仍有待检验,同样的问题是,使用脂质纳米颗粒mRNA疫苗以外的平台接种疫苗,特别是黑猩猩腺病毒载体疫苗,是否能引起相同程度的交叉变异反应。然而,这篇论文最重要的信息仍然是,无论他们以前是否感染过这种病毒,都应该尽可能多的人接种疫苗,以努力保护他们不仅免受祖先的SARS-CoV-2的影响,而且至少在一定程度上防止出现新的变种。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。