克罗恩病(CD)新药!艾伯维口服JAK1抑制剂Rinvoq(乌帕替尼)第二个3期诱导研究成功!
来源:本站原创 2022-02-26 00:17
与安慰剂相比,Rinvoq达到了临床缓解和内镜应答主要终点。
克罗恩病(CD)
2022年02月25日讯 /生物谷BIOON/ --艾伯维(AbbVie)近日公布了新型抗炎药口服JAK1抑制剂Rinvoq(瑞福®,通用名:upadacitinib,乌帕替尼缓释片)治疗中度至重度克罗恩病(CD)3期诱导研究U-EXCEL(NCT03345849)。该研究是2项3期诱导研究中的第二项,入组的是对一种或多种常规和/或生物制剂应答不足或不耐受的中重度CD成人患者。
2021年12月,艾伯维公布了3期诱导研究U-EXCEED(NCT03345836)的阳性顶线结果。该研究是2项3期诱导研究中的第一项,入组的是对生物制剂应答不足或不耐受的的中重度CD成人患者,其中60%以上的患者先前接受过2种或2种以上生物制剂治疗。(结果详见:克罗恩病(CD)新药!艾伯维口服JAK1抑制剂Rinvoq首个3期诱导研究成功:达到临床缓解&内镜应答终点!)
U-EXCEL与U-EXCEED具有相同的主要终点和关键次要终点。2项研究结果显示:治疗第12周,Rinvoq(45mg,每日一次)达到了临床缓解(clinical remission)和内镜应答(endoscopic response)主要终点。
临床缓解通过克罗恩病活动指数(CDAI)和患者报告的大便次数/腹痛症状(SF/AP)来衡量。U-EXCEL研究数据显示,与安慰剂相比,接受为期12周Rinvoq诱导方案(45mg,每日一次)治疗的患者,在第12周达到CDAI临床缓解的比例显著增加(49% vs 29%;p<0.0001)。采用SF/AP评价的临床缓解率也表现出类似的结果(51% vs 22%;p<0.0001)。在该研究中,所有患者还通过内镜检查评估了肠粘膜的改善情况。在第12周,与安慰剂组相比,Rinvoq(45mg,每日一次)治疗组,有更高比例的患者实现了内镜应答(46% vs 13%;p<0.0001)。
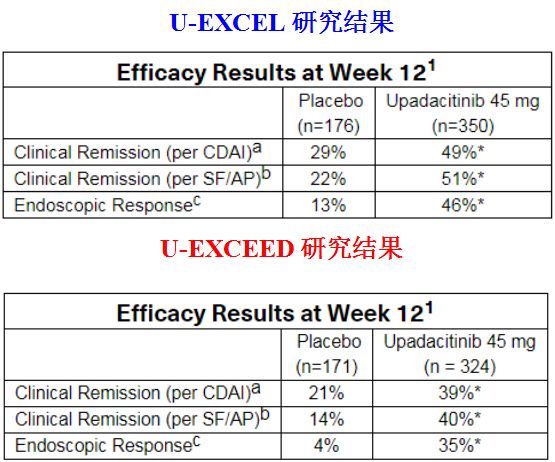
2项诱导研究(U-EXCEL,U-EXCEED)结果
与U-EXCEED诱导研究结果一致,U-EXCEL研究数据显示:在基线时接受皮质类固醇治疗的患者中,在第12周时,与安慰剂组相比,Rinvoq(45mg,每日一次)治疗组有显著更高比例的患者实现无类固醇临床缓解(采用CDAI和SF/AP评价)。此外,与安慰剂组相比,Rinvoq治疗组有显著更高比例的患者在第2周实现早期症状改善(采用CR-100评价,定义为CDAI评分相对基线降低≥100分)、在第4周实现临床缓解。
在12周、双盲、安慰剂对照期内,Rinvoq 45mg的安全性与先前研究中观察到的适应症安全性一致,未观察到新的安全风险。最常见的不良事件:Rinvoq治疗组为痤疮和贫血。在该研究中,安慰剂组报告了一例判定的重大心血管事件(MACE)。Rinvoq治疗组未报告判定的MACE、恶性肿瘤、静脉血栓栓塞事件。
U-EXCEL研究的全部结果将在即将召开的医学会议上公布。艾伯维副主席兼总裁Michael Severino博士表示:“这项研究的结果重申了U-EXCEED研究的数据,并证明了Rinvoq可能对中重度克罗恩病患者的临床和内镜结果产生的潜在影响。我们与胃肠病学界数十年的合作表明,艾伯维致力于为炎症性肠病患者发现和开发多种治疗方案。”
克罗恩病(CD)是一种慢性系统性疾病,表现为胃肠道(或消化道)内的炎症,引起持续性腹泻、腹痛和直肠出血。该病是一种进行性疾病,意味着随着时间的推移病情会恶化。因为CD的体征和症状是不可预测的,不仅在身体上而且在情感上和经济上给患者造成巨大的负担。
Rinvoq的活性药物成分为upadacitinib,这是由艾伯维发现和开发的一种口服选择性和可逆的JAK1抑制剂,正被开发治疗数种免疫介导的炎症性疾病。JAK1是一种激酶,在多种炎症性疾病的病理生理过程中发挥了关键作用。
截至目前,Rinvoq在欧盟已获批4个适应症(类风湿性关节炎[RA],银屑病关节炎[PsA],强直性脊柱炎[AS]、特应性皮炎[AD]),在美国已获批3个适应症(RA、PsA、AD)。Rinvoq 15mg剂量适用于治疗上述全部适应症,而Rinvoq 30mg仅适用于治疗AD。
在中国,2022年2月,国家药品监督管理局(NMPA)批准Rinvoq(瑞福®,乌帕替尼缓释片),治疗成人和12岁及以上儿童及青少年的难治性、中度至重度特应性皮炎(AD)。此次批准,标志着Rinvoq在中国获批的第一个适应症。
值得一提的是,Rinvoq(瑞福®,乌帕替尼缓释片)是中国第一个获批用于治疗特应性皮炎的口服选择性JAK抑制剂,开创了中国特应性皮炎口服靶向治疗新时代。全球同步,为中国患者带来全新治疗选择。2021年8月、2022年1月,Rinvoq分别在欧盟、美国获批特应性皮炎适应症。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


