BCMAxCD3双特异性抗体!强生teclistamab皮下注射治疗复发/难治多发骨髓瘤:总缓解率73%!
来源:本站原创 2020-12-09 16:32
teclistamab是强生探索多种途径靶向多个靶点治疗多发性骨髓瘤的项目之一。

2020年12月09日讯 /生物谷BIOON/ --强生(JNJ)旗下杨森制药近日在第62届美国血液学会(ASH)年会上公布了teclistamab(JNJ-64007957,JNJ-7957)I期首个人体剂量递增研究(NCT03145181)的最新结果。该研究评估了teclistamab治疗既往已过度预治疗(heavily-pretreated,指先前接受过多种方案治疗)的复发或难治性多发性骨髓瘤(RRMM)患者。
结果显示:在推荐的皮下(SC)2期剂量(RP2D)下,teclistamab治疗的总缓解率(ORR)为73%(n=16/22)。SC制剂的结果支持了关键2期注册试验的推荐剂量,该试验已经启动。此外,静脉(IV)制剂的最新结果证实了缓解的持久性。
teclistamab是一种以B细胞成熟抗原(BCMA)和T细胞CD3受体为靶点的双特异性抗体。BCMA在多发性骨髓瘤细胞上表达水平显著升高、CD3参与激活T细胞。teclistamab将CD3 T细胞重新定向到表达BCMA的骨髓瘤细胞,以诱导针对靶细胞的细胞毒作用。临床前研究结果表明,teclistamab可杀死来自过度预治疗患者的骨髓瘤细胞。
目前,teclistamab正在I期临床研究中评估治疗复发或难治性多发性骨髓瘤(RRMM)的疗效,同时也在联合研究中进行探索。teclistamab的生产和开发遵循了杨森生物科技公司与Genmab签订的使用DuoBody®技术平台的许可协议。
ASH会议报告者、宾夕法尼亚大学佩雷尔曼医学院医学助理教授Alfred Garfall博士表示:“今天的皮下制剂数据建立在今年早些时候静脉制剂非常有希望的结果基础之上。初步疗效,包括缓解的持久性,以及在这一高度预治疗人群中的初步安全性,非常令人鼓舞,并支持在需要额外治疗选择的复发或难治性多发性骨髓瘤患者群体中对teclistamab进行进一步的研究。”
杨森研发公司血液学恶性肿瘤全球主管Yusri Elsayed博士表示:“我们致力于探索在多发性骨髓瘤治疗中使用有前景的治疗方案,包括双特异性抗体,如teclistamab,通过抗原靶向来提供治疗反应。我们对多发性骨髓瘤的研究非常广泛,通过多种途径探索多个靶点。我们将继续寻找新的治疗方案,特别是对于现有疗法治疗后复发或对现有疗法不敏感的患者。”
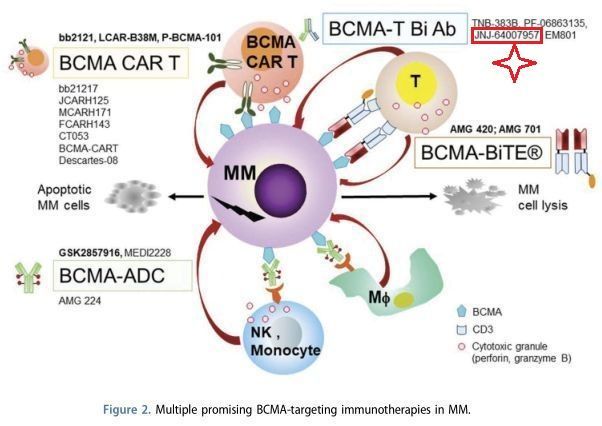
BCMA为靶点的在研MM免疫疗法(来源文献—PMID:31277554)
ASH年会上公布的I期研究入组的是对现有疗法治疗后复发或对这些疗法难治、先前接受过蛋白酶体抑制剂(PI)和免疫调节药物(IMiD)治疗的多发性骨髓瘤患者。在开始研究前,患者之前接受的治疗方案中位数为6种(范围2-14);92%接受过3类疗法、86%对最后一种疗法难治、80%对三类疗法难治、41%对五种药物难治,这意味着患者的癌症在使用≥2种免疫调节剂、≥2种PI、1种抗CD38疗法治疗无应答或在治疗60天内复发。三类疗法难治和五种药物难治的多发性骨髓瘤患者由于治疗方案有限,生存预后很差。
该研究分为2部分开展:剂量递增(第1部分)和剂量扩展(第2部分)。teclistamab RP2D已被确定为1500μg/kg SC,最大耐受剂量尚未确定。在RP2D SC方案下,55%的患者获得了非常好的部分缓解(VGPR)或更好的缓解(12/22)、23%的患者(5/22)获得完全缓解(CR)或更好缓解。中位随访3.9个月(范围:1.7-7.4个月),病情缓解的患者中,有94%(15/16)仍然存活且疾病无进展。在RP2D SC方案下,缓解表现持久且随着时间推移加深。
在全部IV和SC队列中病情获得CR且可评估微小残留病(MRD)的11例患者中,8例患者在10-6阈值下获得MRD阴性CR、1例患者在10-5阈值下获得MRD阴性CR。在IV和SC队列中,全部5例可评估患者均证实了持续的MRD阴性。
在SC RP2D方案下,64%的患者出现细胞因子释放综合征(CRS)事件,所有这些事件都是1级或2级,通常局限于逐步增加剂量或逐渐增加剂量,以及首次全剂量。没有患者因CRS而停止治疗。在接受RP2D治疗的33例患者中,仅观察到1例1级可逆的神经毒性事件。选择1500ug/kg SC-RP2D基于良好的安全性、有效性、药代动力学和药效学支持。SC制剂可能比IV制剂提供更低的给药频率,尽管目前的研究尚未对此进行探讨。
在SC队列中,RP2D最常见的不良事件(AE;所有级别≥20%)是CRS(64%)、中性粒细胞减少(52%)、贫血(39%)、血小板减少(33%)、白细胞减少(33%)和疲劳(24%)。在RP2D SC剂量下,出现3级及以上不良事件(≥20%)的患者中,最常见的是中性粒细胞减少症(33%)和贫血(21%)。在80μg/kg IV剂量下报告了1例5级治疗相关不良事件(肺炎),但在RP2D剂量下则没有。(生物谷Bioon.com)
原文出处:Updated Results from the Phase 1 Study of the BCMAxCD3 Bispecific Teclistamab Show Preliminary Efficacy in Patients with Heavily Pretreated Relapsed or Refractory Multiple Myeloma
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


