2019年9月Cell期刊不得不看的亮点研究
来源:本站原创 2019-09-30 23:59
2019年9月30日讯/生物谷BIOON/---2019年9月份即将结束了,9月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:重新思考胆固醇如何被整合到细胞中doi:10.1016/j.cell.2019.08.038NPC(Niemann-Pick type C)蛋白对于胆固醇之类的固醇体内平衡是必不可少的。人们认为在重新分配至其他细胞膜之前,NPC蛋白
2019年9月30日讯/生物谷BIOON/---2019年9月份即将结束了,9月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:重新思考胆固醇如何被整合到细胞中
doi:10.1016/j.cell.2019.08.038
NPC(Niemann-Pick type C)蛋白对于胆固醇之类的固醇体内平衡是必不可少的。人们认为在重新分配至其他细胞膜之前,NPC蛋白会促进固醇整合到溶酶体膜中。
在一项新的研究中,这些研究人员通过联合使用结晶学和低温电镜,以及对酿酒酵母NPC系统(NCR1和NPC2)的体内研究,提出了固醇膜整合的一种框架。相关研究结果于2019年9月19日在线发表在Cell期刊上,论文标题为“Structural Insight into Eukaryotic Sterol Transport through Niemann-Pick Type C Proteins”。
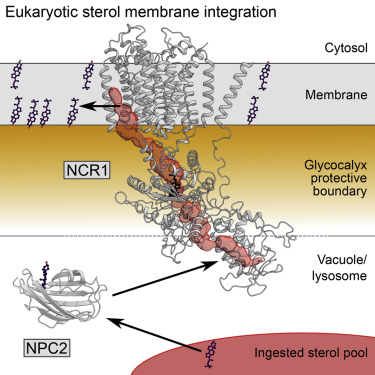
固醇在液泡NPC2和膜蛋白NCR1的疏水口袋之间转移。NCR1的N末端结构域(NTD)定位为将固醇递送至将NTD与距离 50Å的腔膜小叶连接在一起的隧道中。固醇在运输过程中被捕获在这个隧道的内部,这种跨膜区域中带电荷氨基酸残基组成的质子中继网络与这个隧道相连,从而支持一种质子驱动的运输机制。
这些研究人员提出了一种固醇整合模型,该模型阐明了NPC蛋白在这个必不可少的真核生物途径中的作用,并对C型尼曼匹克病(Niemann-Pick disease type C)患者体内发生的突变进行了合理化解释。
2.Cell:新研究表明肠道细菌可提高流感疫苗在临床试验中的疗效
doi:10.1016/j.cell.2019.08.010
在动物模型和人类相关研究中的越来越多证据表明肠道中存在的微生物可以塑造免疫反应。在一项新的研究中,来自美国斯坦福大学的研究人员在人体中证实了这种关联性。他们发现对没有接种流感疫苗或者在过去三年未感染流感病毒的人来说,在接种流感疫苗之前的抗生素治疗方案导致免疫接种产生的抗体数量少于没有接受抗生素治疗的研究参与者。相关研究结果近期发表在Cell期刊上,论文标题为“Antibiotics-Driven Gut Microbiome Perturbation Alters Immunity to Vaccines in Humans”。
在美国纽约大学医学院研究研究菌群-免疫系统相互作用的Dan Littman(未参与这项新的研究)说道,“在人体中开展这类研究非常重要,这是因为在动物模型中已开展了大量研究工作。尽管这非常有价值,特别是对于了解免疫系统如何对菌群、疫苗接种、致命性微生物感染作出反应的机制方面,但是在人体中明显会存在差异,而且我们对人体如何作出反应知之甚少。”
3.Cell:利用蛋白质组学技术揭示转移性黑色素瘤患者为何对免疫疗法没有反应?
doi:10.1016/j.cell.2019.08.012
近日,一项刊登在国际杂志Cell上的研究报告中,来自特拉维夫大学的研究人员通过研究解释了为何超过一半的转移性黑色素瘤患者对癌症免疫疗法没有反应,文章中,研究人员利用蛋白质组学技术(蛋白质图谱绘制)回答了目前他们迫切想要知道的一个问题,即为何免疫疗法对黑色素瘤患者有很大帮助,但对60%的转移性黑色素瘤患者却没有影响。
研究者对比了116名黑色素瘤患者对免疫疗法的反应(包括免疫疗法成功治疗和没有成功治疗的患者),运用蛋白质组学技术,研究者就能够发现两组患者机体中的癌细胞在代谢上的差异。研究者Markel教授说道,近些年来科学家们使用了多种癌症免疫疗法,即这些疗法能够增强机体免疫系统的抗癌活性,这些疗法能有效治疗部分癌症患者,但有些患者对免疫疗法却并没有反应,目前研究人员并不清楚其中的分子机制。
这项研究中,研究人员重点对转移性黑色素瘤进行研究,为了更好地理解癌细胞对疗法产生耐受性的分子机制,研究人员利用蛋白质组学技术分析了来自116名患者机体的肿瘤样本;研究者利用质谱仪对细胞中多种蛋白质进行图谱绘制,随后进行大量计算分析来识别两组患者机体中蛋白质的差异;蛋白质组的比较能帮助识别出对免疫疗法反应和无反应组患者机体的主要差异,在反应者机体中,高水平的蛋白表达与脂质代谢之间密切相关,其或许能被机体免疫系统更好地进行识别。
随后研究者在转移性黑色素瘤小鼠模型和黑色素瘤组织培养物中验证了他们的研究结果,利用遗传工程学技术,他们沉默了负责脂质代谢的细胞机制,研究者发现,沉默该代谢通路后,癌细胞就能够设法隐藏起来以免被宿主机体的T细胞识别并破坏,因此,小鼠机体的癌细胞要比对照组发育地更快。
4.Cell:成功绘制出小鼠大脑中1000个神经元的连接图谱
doi:10.1016/j.cell.2019.07.042
在一项新的研究中,来自美国霍华德休斯医学研究所珍妮亚研究中心的研究人员仔细地解开了1000多个纠缠在一起的神经元,追踪了每个细胞在大脑中的分支路径,以确定它的去向和与哪些细胞连接在一起。他们报道,如果端对端放置的话,这些神经元将伸展80多米,大约相当于两辆校车的长度。相关研究结果近期发表在Cell期刊上,论文标题为“Reconstruction of 1,000 Projection Neurons Reveals New Cell Types and Organization of Long-Range Connectivity in the Mouse Brain”。
两年前,当Jayaram Chandrashekar和他的同事们开始他们的神经制图工作时,神经科学家对哺乳动物大脑中的哪些区域相互交谈有一个大概的想法。但是,大脑中的信息传递架构在很大程度上是一个谜。一种完整的神经回路图可以帮助科学家们更好地理解大脑是如何连接的,以及信息如何通过这种神经回路进行传播。2017年10月,神经元追踪项目团队MouseLight发布了前300个神经元的数据。如今,他们大大扩展了这个数据集,增加了700多个神经元。Chandrashekar说,“这是迄今为止此类神经元的最大数字集合。”
5.Cell:新研究揭示选择性启动子在肿瘤中的调节作用
doi:10.1016/j.cell.2019.08.018
在一项新的研究中,来自新加坡基因组研究所(GIS)等研究机构的研究人员发现很多人类癌症在基因激活方面表现出广泛的变化,而且相同的基因使用不同的起始位置来产生选择性基因产物。这些变化未被早期的分析方法检测到,可能用于鉴定出预测癌症患者存活的新型生物标志物和新的治疗靶标。相关研究结果近期发表在Cell期刊上,论文标题为“A Pan-cancer Transcriptome Analysis Reveals Pervasive Regulation through Alternative Promoters”。
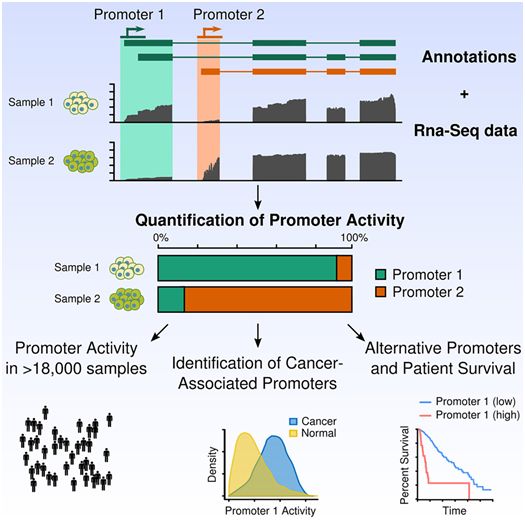
人类基因组包含我们所有的基因。控制基因起始位置的区域称为启动子,或者称为开启基因组中基因的“开关”。许多基因具有多个启动子,这甚至可以导致相同的基因出现不同功能。
这些研究人员设计出一种名为proActiv的专用软件,用于在全基因组范围内检测被激活的启动子,即活化启动子。proActiv中的基础算法适用于RNA分析数据,该数据通常由全球数百个研究癌症的实验室产生。他们将proActiv应用于从1.8万多个癌症样本中收集的大量公开数据,并发现癌基因中的启动子经常不同于未患癌症的人体中的基因启动子。他们还发现了与癌症患者存活率相关的特定活化启动子,这代表了一类新的生物标志物。
6.Cell:在关键时间窗口内靶向激活PV神经元有望治疗精神分裂症
doi:10.1016/j.cell.2019.07.023
尽管诱发过程发生得更早,但精神分裂症在成年早期出现,这表明它可能涉及易感个体大脑发育后期期间的病理转变。在一项新的研究中,通过使用精神分裂症的遗传小鼠模型,来自瑞士弗雷德里希米歇尔研究所(FMI)的Pico Caroni及其研究团队发现与人类患者一样,特征性的网络和认知缺陷仅在成年小鼠中出现。他们随后证实在青春期后期的敏感时间窗口期间,这些缺陷可通过特定治疗永久性地加以阻止。相关研究结果近期发表在Cell期刊上,论文标题为“Long-Lasting Rescue of Network and Cognitive Dysfunction in a Genetic Schizophrenia Model”。
为了研究一种具有复杂遗传成分的疾病的根本原因,人们需要尽可能将重点放在更简单的“遗传模型”上,即携带明确确定的突变的人或动物,它/他们表现出较高发病率的风险。在精神分裂症中,此类遗传模型包括患有22Q11DS综合征的人,22Q11DS综合征由22号染色体发生部分片段缺失引起,这些人患精神分裂症的风险增加20~30倍。这导致这些研究人员培育出携带相应缺失的小鼠,以便将它们用作精神分裂症模型用于实验室研究。(这些小鼠被称为“LgDel小鼠”,但为了简单起见,在这里将它们称为“精神分裂症小鼠”。)
通过使用精神分裂症小鼠模型,Caroni团队着手研究精神分裂症小鼠表现出的缺陷,以及如何治疗和预防这些缺陷。他们发现已知在人类患者身上存在的情况在精神分裂症小鼠身上也同样存在:网络和认知功能障碍在青春期后期出现。与人类患者一样,成年小鼠在称为PV神经元的特定类型神经元中显示出严重的功能障碍,其中PV神经元是神经网络的重要协调者。这种功能障碍导致网络同步缺陷,这是精神分裂症的一个标志。值得注意的是,抗精神病药物科暂时抑制成年精神分裂症小鼠的网络和认知缺陷。
7.Cell:长期存在的细胞发育难题终破解!揭示神经嵴细胞在胚胎发育早期清除死亡细胞
doi:10.1016/j.cell.2019.08.001
无论是人类、鱼类还是任何其他类型的脊椎动物,在其一生当中,细胞都会死亡,从而为新细胞腾出空间来进行重要的过程。但是死细胞必须被清除,在胚胎阶段之后,细胞碎片是通过称为巨噬细胞的免疫系统细胞清除的。 然而,处于胚胎阶段的有机体还没有发育出巨噬细胞和免疫系统。它们是随后在有机体的进一步发育过程中产生的。那么在巨噬细胞出现之前,死细胞是如何被清除的呢?这是发育生物学家长期以来提出的一个老问题。 如今,在一项新的研究中,来自美国弗吉尼亚大学的研究人员描述了他们发现的一个过程:神经系统的胚胎细胞---神经嵴细胞(neural crest cell)---在斑马鱼发育的较早阶段执行死细胞清除任务。相关研究结果近期发表在Cell期刊上,论文标题为“Migratory Neural Crest Cells Phagocytose Dead Cells in the Developing Nervous System”。

通过对活斑马鱼胚胎进行成像,这些研究人员能够观察到迁移性的神经嵴细胞以一种非常类似巨噬细胞的方式发挥功能。这些最终产生周围神经系统并产生多种组织(骨骼、色素细胞、软骨和纤维结缔组织)的神经嵴细胞似乎在物理上接触死细胞,包围它们,随后吸收它们所含的诸如氨基酸之类的化合物,这些化合物接着就可用于构建新的细胞。
论文通讯作者、弗吉尼亚大学生物学教授Sarah Kucenas说,“有趣且意外的是,神经嵴细胞使用相同的细胞碎片清除机制,巨噬细胞在接管这一重要角色后也将会使用这一机制。这也是有意义的,这是因为作为在体内能够快速移动的细胞,神经嵴细胞,发挥着这种重要的早期功能---死细胞清除---直到特化细胞,即巨噬细胞,出现。”
8.Cell重磅! 记忆性T细胞藏在骨髓中,提高免疫力!
doi:10.1016/j.cell.2019.07.049
即使摄入更少的热量和营养,人类和其他哺乳动物通常仍能抵御他们已经遇到过的传染病。据美国国立卫生研究院下属的美国国家过敏与传染病研究所(NIAID)的科学家们说,这可能是因为记忆T细胞分布在人体各处,可以维持对感染因子的免疫反应。他们近日在《Cell》杂志上发表的对小鼠的研究还发现,节食的动物比不节食的动物更能抵御肿瘤和细菌感染。
由Yasmine Belkaid博士(NIAID机体免疫部门的负责人)领导的研究人员,此前曾观察到老鼠体内的脂肪组织中含有记忆T细胞。他们研究了当卡路里摄入量减少时,这种现象是否有助于保持免疫记忆。为了进行研究,他们限制了先前完全接触食物的老鼠的饮食。当接受更少的食物时,小鼠淋巴组织中的记忆T细胞(它们通常在淋巴组织中逗留)更少,而骨髓中的更多T细胞则富含脂肪组织。
然后,研究人员评估了老鼠吃得少时,记忆T细胞的表现。当小鼠自由进食时,感染了假结核耶尔森菌。在小鼠产生免疫记忆后,研究人员限制了部分小鼠的饮食长达四周,然后再次将所有小鼠接触假结核杆菌。限制饮食的小鼠有更强的记忆T细胞反应,更好地防止疾病。研究人员使用一种训练免疫细胞对抗黑色素瘤的疫苗重复了这个实验,并发现接受较少食物的小鼠体内的记忆T细胞具有更强的抗肿瘤效果。
9.Cell:揭示饮食通过作用于肠道细菌来影响二甲双胍的疗效
doi:10.1016/j.cell.2019.08.003
在一项新的研究中,英国MRC伦敦医学科学研究所的Filipe Cabreiro团队和德国基尔大学的Christoph Kaleta团队证实饮食可通过对肠道细菌的作用来改变一种2型糖尿病药物的疗效。相关研究结果于2019年8月29日在线发表在Cell期刊上,论文标题为“Host-Microbe-Drug-Nutrient Screen Identifies Bacterial Effectors of Metformin Therapy”。
存在于我们胃肠道中的细菌,统称为肠道微生物组,可产生许多能够影响健康和疾病的分子。已知肠道微生物组的功能受饮食和诸如二甲双胍(metformin)之类的药物的调节,其中二甲双胍用于治疗2型糖尿病并且已显示可延长几种有机体的寿命。然而,理解饮食、药物和肠道微生物组之间复杂的多向关系是一个相当大的挑战。Cabreiro说,“破解这种相互作用网络至关重要,这是因为二甲双胍的具体作用机制尚不清楚。”
Cabreiro和他的团队开发出一种新的四向高通量筛选技术,以更好地了解饮食、药物和肠道微生物组如何相互作用来影响宿主生理学特性。他们使用定植着大肠杆菌(一种人类肠道细菌)的秀丽隐杆线虫作为一种简化的宿主-微生物组模型,并且在数百种不同的营养化合物存在下将这种线虫暴露于二甲双胍。他们发现二甲双胍治疗改变了宿主秀丽隐杆线虫的代谢和寿命,而且这些影响可以通过特定的营养物加以增强或抑制。至关重要的是,他们揭示出肠道细菌在调节这种现象方面发挥了关键作用。
饮食和肠道细菌的重要性解释了为何二甲双胍以前被证实对另一种常被研究的有机体果蝇的寿命没有影响。论文共同作者、Helena Cochemé说:“结果证实针对果蝇的典型实验室食物含有丰富的糖分。在除去糖分后,我们也观察到二甲双胍对定殖着大肠杆菌的果蝇的正面影响。”
10.Cell:系统性构建出病毒与人类宿主之间的蛋白-蛋白相互作用图谱
doi:10.1016/j.cell.2019.08.005
在一项新的研究中,来自美国哥伦比亚大学的研究人员利用一种计算方法绘制出所有已知感染人类的病毒与它们感染的宿主细胞之间的蛋白-蛋白相互作用图谱。这种方法及其产生的数据已给出了大量关于病毒如何操纵它们感染的宿主细胞和引起疾病的信息。这项研究的发现包括雌激素受体在调节寨卡病毒感染中的作用和人乳头瘤病毒(HPV)如何导致癌症。相关研究结果于2019年8月29日在线发表在Cell期刊上,论文标题为“A Structure-Informed Atlas of Human-Virus Interactions”。论文通讯作者为哥伦比亚大学医学中心的Sagi Shapira博士和Barry Honig博士。
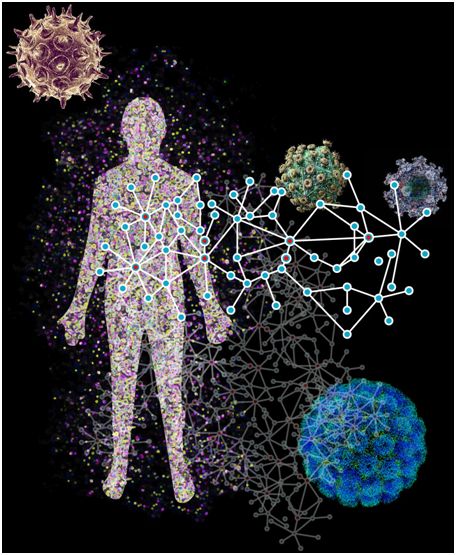
在分子水平上,病毒侵入细胞并操纵细胞进行复制、存活并引发疾病。鉴于它们依赖于人体细胞完成它们的生命周期,因此病毒利用细胞功能的一种方式是通过宿主细胞内的蛋白-蛋白相互作用。类似地,细胞通过启动控制和限制病毒复制的免疫应答来对病毒感染作出反应 ,这也依赖于蛋白-蛋白相互作用。
迄今为止,已经投入了大量精力来鉴定这些关键的相互作用---这些努力中的一些产生了许多基本发现,其中的一些基本发现具有治疗意义。然而,传统方法在可扩展性、效率甚至获取方面受到限制。为了应对这一挑战,Shapira博士及其合作者开发并执行了一个计算框架---P-HipsTer,它可推导病毒性病原体蛋白和人类蛋白之间的相互作用。
11.Cell:科学家成功筛选出开发新型癌症免疫疗法的关键靶点
doi:10.1016/j.cell.2019.07.044
在过去10年里免疫疗法给癌症治疗带来了革命性的变革,然而很多肿瘤对这些新型疗法并没有反应,近日,来自耶鲁大学的科学家们通过研究对T细胞中2万个人类基因进行全基因组筛选,鉴别出了多个新型候选基因,其能促进机体免疫系统攻击多种类型的肿瘤,相关研究结果刊登在国际杂志Cell上。
研究者Sidi Chen教授说道,免疫疗法对于所有患者并非都有效果,大约70%-80%的患者对疗法并无反应;那么我们为何不从基因层面进行研究来分析哪些基因主要负责肿瘤生长,同时寻找开发新型癌症疗法的潜在靶点;很多免疫疗法都基于抑制PD1基因而开发,PD-1能抑制T细胞动员并攻击肿瘤细胞的能力,这些疗法明显提高了多种类型癌症患者的存活率,比如黑色素瘤和肺癌等,然而即便在这些癌症中,也仅有30%-40%的患者对免疫疗法能产生反应,对于大多数癌症类型而言,患者的反应率在20%以下,某些恶性肿瘤患者的反应率甚至在10%以下。
研究人员开发的新型平台能利用CRISPR基因编辑技术敲除小鼠机体中的基因来观察哪种基因对机体免疫系统对肿瘤产生的反应效应最大,其中研究者鉴别出的一个基因名为DHX37,其能够有效抑制小鼠机体中CD8杀伤性T细胞对肿瘤的反应,当DHX37基因被编辑后,患三阴性乳腺癌的小鼠机体中的肿瘤尺寸会明显下降。(生物谷 Bioon.com)
1.Cell:重新思考胆固醇如何被整合到细胞中
doi:10.1016/j.cell.2019.08.038
NPC(Niemann-Pick type C)蛋白对于胆固醇之类的固醇体内平衡是必不可少的。人们认为在重新分配至其他细胞膜之前,NPC蛋白会促进固醇整合到溶酶体膜中。
在一项新的研究中,这些研究人员通过联合使用结晶学和低温电镜,以及对酿酒酵母NPC系统(NCR1和NPC2)的体内研究,提出了固醇膜整合的一种框架。相关研究结果于2019年9月19日在线发表在Cell期刊上,论文标题为“Structural Insight into Eukaryotic Sterol Transport through Niemann-Pick Type C Proteins”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.08.038。
固醇在液泡NPC2和膜蛋白NCR1的疏水口袋之间转移。NCR1的N末端结构域(NTD)定位为将固醇递送至将NTD与距离 50Å的腔膜小叶连接在一起的隧道中。固醇在运输过程中被捕获在这个隧道的内部,这种跨膜区域中带电荷氨基酸残基组成的质子中继网络与这个隧道相连,从而支持一种质子驱动的运输机制。
这些研究人员提出了一种固醇整合模型,该模型阐明了NPC蛋白在这个必不可少的真核生物途径中的作用,并对C型尼曼匹克病(Niemann-Pick disease type C)患者体内发生的突变进行了合理化解释。
2.Cell:新研究表明肠道细菌可提高流感疫苗在临床试验中的疗效
doi:10.1016/j.cell.2019.08.010
在动物模型和人类相关研究中的越来越多证据表明肠道中存在的微生物可以塑造免疫反应。在一项新的研究中,来自美国斯坦福大学的研究人员在人体中证实了这种关联性。他们发现对没有接种流感疫苗或者在过去三年未感染流感病毒的人来说,在接种流感疫苗之前的抗生素治疗方案导致免疫接种产生的抗体数量少于没有接受抗生素治疗的研究参与者。相关研究结果近期发表在Cell期刊上,论文标题为“Antibiotics-Driven Gut Microbiome Perturbation Alters Immunity to Vaccines in Humans”。
在美国纽约大学医学院研究研究菌群-免疫系统相互作用的Dan Littman(未参与这项新的研究)说道,“在人体中开展这类研究非常重要,这是因为在动物模型中已开展了大量研究工作。尽管这非常有价值,特别是对于了解免疫系统如何对菌群、疫苗接种、致命性微生物感染作出反应的机制方面,但是在人体中明显会存在差异,而且我们对人体如何作出反应知之甚少。”
3.Cell:利用蛋白质组学技术揭示转移性黑色素瘤患者为何对免疫疗法没有反应?
doi:10.1016/j.cell.2019.08.012
近日,一项刊登在国际杂志Cell上的研究报告中,来自特拉维夫大学的研究人员通过研究解释了为何超过一半的转移性黑色素瘤患者对癌症免疫疗法没有反应,文章中,研究人员利用蛋白质组学技术(蛋白质图谱绘制)回答了目前他们迫切想要知道的一个问题,即为何免疫疗法对黑色素瘤患者有很大帮助,但对60%的转移性黑色素瘤患者却没有影响。
研究者对比了116名黑色素瘤患者对免疫疗法的反应(包括免疫疗法成功治疗和没有成功治疗的患者),运用蛋白质组学技术,研究者就能够发现两组患者机体中的癌细胞在代谢上的差异。研究者Markel教授说道,近些年来科学家们使用了多种癌症免疫疗法,即这些疗法能够增强机体免疫系统的抗癌活性,这些疗法能有效治疗部分癌症患者,但有些患者对免疫疗法却并没有反应,目前研究人员并不清楚其中的分子机制。
这项研究中,研究人员重点对转移性黑色素瘤进行研究,为了更好地理解癌细胞对疗法产生耐受性的分子机制,研究人员利用蛋白质组学技术分析了来自116名患者机体的肿瘤样本;研究者利用质谱仪对细胞中多种蛋白质进行图谱绘制,随后进行大量计算分析来识别两组患者机体中蛋白质的差异;蛋白质组的比较能帮助识别出对免疫疗法反应和无反应组患者机体的主要差异,在反应者机体中,高水平的蛋白表达与脂质代谢之间密切相关,其或许能被机体免疫系统更好地进行识别。
随后研究者在转移性黑色素瘤小鼠模型和黑色素瘤组织培养物中验证了他们的研究结果,利用遗传工程学技术,他们沉默了负责脂质代谢的细胞机制,研究者发现,沉默该代谢通路后,癌细胞就能够设法隐藏起来以免被宿主机体的T细胞识别并破坏,因此,小鼠机体的癌细胞要比对照组发育地更快。
4.Cell:成功绘制出小鼠大脑中1000个神经元的连接图谱
doi:10.1016/j.cell.2019.07.042
在一项新的研究中,来自美国霍华德休斯医学研究所珍妮亚研究中心的研究人员仔细地解开了1000多个纠缠在一起的神经元,追踪了每个细胞在大脑中的分支路径,以确定它的去向和与哪些细胞连接在一起。他们报道,如果端对端放置的话,这些神经元将伸展80多米,大约相当于两辆校车的长度。相关研究结果近期发表在Cell期刊上,论文标题为“Reconstruction of 1,000 Projection Neurons Reveals New Cell Types and Organization of Long-Range Connectivity in the Mouse Brain”。
两年前,当Jayaram Chandrashekar和他的同事们开始他们的神经制图工作时,神经科学家对哺乳动物大脑中的哪些区域相互交谈有一个大概的想法。但是,大脑中的信息传递架构在很大程度上是一个谜。一种完整的神经回路图可以帮助科学家们更好地理解大脑是如何连接的,以及信息如何通过这种神经回路进行传播。2017年10月,神经元追踪项目团队MouseLight发布了前300个神经元的数据。如今,他们大大扩展了这个数据集,增加了700多个神经元。Chandrashekar说,“这是迄今为止此类神经元的最大数字集合。”
5.Cell:新研究揭示选择性启动子在肿瘤中的调节作用
doi:10.1016/j.cell.2019.08.018
在一项新的研究中,来自新加坡基因组研究所(GIS)等研究机构的研究人员发现很多人类癌症在基因激活方面表现出广泛的变化,而且相同的基因使用不同的起始位置来产生选择性基因产物。这些变化未被早期的分析方法检测到,可能用于鉴定出预测癌症患者存活的新型生物标志物和新的治疗靶标。相关研究结果近期发表在Cell期刊上,论文标题为“A Pan-cancer Transcriptome Analysis Reveals Pervasive Regulation through Alternative Promoters”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.08.018。
人类基因组包含我们所有的基因。控制基因起始位置的区域称为启动子,或者称为开启基因组中基因的“开关”。许多基因具有多个启动子,这甚至可以导致相同的基因出现不同功能。
这些研究人员设计出一种名为proActiv的专用软件,用于在全基因组范围内检测被激活的启动子,即活化启动子。proActiv中的基础算法适用于RNA分析数据,该数据通常由全球数百个研究癌症的实验室产生。他们将proActiv应用于从1.8万多个癌症样本中收集的大量公开数据,并发现癌基因中的启动子经常不同于未患癌症的人体中的基因启动子。他们还发现了与癌症患者存活率相关的特定活化启动子,这代表了一类新的生物标志物。
6.Cell:在关键时间窗口内靶向激活PV神经元有望治疗精神分裂症
doi:10.1016/j.cell.2019.07.023
尽管诱发过程发生得更早,但精神分裂症在成年早期出现,这表明它可能涉及易感个体大脑发育后期期间的病理转变。在一项新的研究中,通过使用精神分裂症的遗传小鼠模型,来自瑞士弗雷德里希米歇尔研究所(FMI)的Pico Caroni及其研究团队发现与人类患者一样,特征性的网络和认知缺陷仅在成年小鼠中出现。他们随后证实在青春期后期的敏感时间窗口期间,这些缺陷可通过特定治疗永久性地加以阻止。相关研究结果近期发表在Cell期刊上,论文标题为“Long-Lasting Rescue of Network and Cognitive Dysfunction in a Genetic Schizophrenia Model”。
为了研究一种具有复杂遗传成分的疾病的根本原因,人们需要尽可能将重点放在更简单的“遗传模型”上,即携带明确确定的突变的人或动物,它/他们表现出较高发病率的风险。在精神分裂症中,此类遗传模型包括患有22Q11DS综合征的人,22Q11DS综合征由22号染色体发生部分片段缺失引起,这些人患精神分裂症的风险增加20~30倍。这导致这些研究人员培育出携带相应缺失的小鼠,以便将它们用作精神分裂症模型用于实验室研究。(这些小鼠被称为“LgDel小鼠”,但为了简单起见,在这里将它们称为“精神分裂症小鼠”。)
通过使用精神分裂症小鼠模型,Caroni团队着手研究精神分裂症小鼠表现出的缺陷,以及如何治疗和预防这些缺陷。他们发现已知在人类患者身上存在的情况在精神分裂症小鼠身上也同样存在:网络和认知功能障碍在青春期后期出现。与人类患者一样,成年小鼠在称为PV神经元的特定类型神经元中显示出严重的功能障碍,其中PV神经元是神经网络的重要协调者。这种功能障碍导致网络同步缺陷,这是精神分裂症的一个标志。值得注意的是,抗精神病药物科暂时抑制成年精神分裂症小鼠的网络和认知缺陷。
7.Cell:长期存在的细胞发育难题终破解!揭示神经嵴细胞在胚胎发育早期清除死亡细胞
doi:10.1016/j.cell.2019.08.001
无论是人类、鱼类还是任何其他类型的脊椎动物,在其一生当中,细胞都会死亡,从而为新细胞腾出空间来进行重要的过程。但是死细胞必须被清除,在胚胎阶段之后,细胞碎片是通过称为巨噬细胞的免疫系统细胞清除的。 然而,处于胚胎阶段的有机体还没有发育出巨噬细胞和免疫系统。它们是随后在有机体的进一步发育过程中产生的。那么在巨噬细胞出现之前,死细胞是如何被清除的呢?这是发育生物学家长期以来提出的一个老问题。 如今,在一项新的研究中,来自美国弗吉尼亚大学的研究人员描述了他们发现的一个过程:神经系统的胚胎细胞---神经嵴细胞(neural crest cell)---在斑马鱼发育的较早阶段执行死细胞清除任务。相关研究结果近期发表在Cell期刊上,论文标题为“Migratory Neural Crest Cells Phagocytose Dead Cells in the Developing Nervous System”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.08.001。
通过对活斑马鱼胚胎进行成像,这些研究人员能够观察到迁移性的神经嵴细胞以一种非常类似巨噬细胞的方式发挥功能。这些最终产生周围神经系统并产生多种组织(骨骼、色素细胞、软骨和纤维结缔组织)的神经嵴细胞似乎在物理上接触死细胞,包围它们,随后吸收它们所含的诸如氨基酸之类的化合物,这些化合物接着就可用于构建新的细胞。
论文通讯作者、弗吉尼亚大学生物学教授Sarah Kucenas说,“有趣且意外的是,神经嵴细胞使用相同的细胞碎片清除机制,巨噬细胞在接管这一重要角色后也将会使用这一机制。这也是有意义的,这是因为作为在体内能够快速移动的细胞,神经嵴细胞,发挥着这种重要的早期功能---死细胞清除---直到特化细胞,即巨噬细胞,出现。”
8.Cell重磅! 记忆性T细胞藏在骨髓中,提高免疫力!
doi:10.1016/j.cell.2019.07.049
即使摄入更少的热量和营养,人类和其他哺乳动物通常仍能抵御他们已经遇到过的传染病。据美国国立卫生研究院下属的美国国家过敏与传染病研究所(NIAID)的科学家们说,这可能是因为记忆T细胞分布在人体各处,可以维持对感染因子的免疫反应。他们近日在《Cell》杂志上发表的对小鼠的研究还发现,节食的动物比不节食的动物更能抵御肿瘤和细菌感染。
由Yasmine Belkaid博士(NIAID机体免疫部门的负责人)领导的研究人员,此前曾观察到老鼠体内的脂肪组织中含有记忆T细胞。他们研究了当卡路里摄入量减少时,这种现象是否有助于保持免疫记忆。为了进行研究,他们限制了先前完全接触食物的老鼠的饮食。当接受更少的食物时,小鼠淋巴组织中的记忆T细胞(它们通常在淋巴组织中逗留)更少,而骨髓中的更多T细胞则富含脂肪组织。
然后,研究人员评估了老鼠吃得少时,记忆T细胞的表现。当小鼠自由进食时,感染了假结核耶尔森菌。在小鼠产生免疫记忆后,研究人员限制了部分小鼠的饮食长达四周,然后再次将所有小鼠接触假结核杆菌。限制饮食的小鼠有更强的记忆T细胞反应,更好地防止疾病。研究人员使用一种训练免疫细胞对抗黑色素瘤的疫苗重复了这个实验,并发现接受较少食物的小鼠体内的记忆T细胞具有更强的抗肿瘤效果。
9.Cell:揭示饮食通过作用于肠道细菌来影响二甲双胍的疗效
doi:10.1016/j.cell.2019.08.003
在一项新的研究中,英国MRC伦敦医学科学研究所的Filipe Cabreiro团队和德国基尔大学的Christoph Kaleta团队证实饮食可通过对肠道细菌的作用来改变一种2型糖尿病药物的疗效。相关研究结果于2019年8月29日在线发表在Cell期刊上,论文标题为“Host-Microbe-Drug-Nutrient Screen Identifies Bacterial Effectors of Metformin Therapy”。
存在于我们胃肠道中的细菌,统称为肠道微生物组,可产生许多能够影响健康和疾病的分子。已知肠道微生物组的功能受饮食和诸如二甲双胍(metformin)之类的药物的调节,其中二甲双胍用于治疗2型糖尿病并且已显示可延长几种有机体的寿命。然而,理解饮食、药物和肠道微生物组之间复杂的多向关系是一个相当大的挑战。Cabreiro说,“破解这种相互作用网络至关重要,这是因为二甲双胍的具体作用机制尚不清楚。”
Cabreiro和他的团队开发出一种新的四向高通量筛选技术,以更好地了解饮食、药物和肠道微生物组如何相互作用来影响宿主生理学特性。他们使用定植着大肠杆菌(一种人类肠道细菌)的秀丽隐杆线虫作为一种简化的宿主-微生物组模型,并且在数百种不同的营养化合物存在下将这种线虫暴露于二甲双胍。他们发现二甲双胍治疗改变了宿主秀丽隐杆线虫的代谢和寿命,而且这些影响可以通过特定的营养物加以增强或抑制。至关重要的是,他们揭示出肠道细菌在调节这种现象方面发挥了关键作用。
饮食和肠道细菌的重要性解释了为何二甲双胍以前被证实对另一种常被研究的有机体果蝇的寿命没有影响。论文共同作者、Helena Cochemé说:“结果证实针对果蝇的典型实验室食物含有丰富的糖分。在除去糖分后,我们也观察到二甲双胍对定殖着大肠杆菌的果蝇的正面影响。”
10.Cell:系统性构建出病毒与人类宿主之间的蛋白-蛋白相互作用图谱
doi:10.1016/j.cell.2019.08.005
在一项新的研究中,来自美国哥伦比亚大学的研究人员利用一种计算方法绘制出所有已知感染人类的病毒与它们感染的宿主细胞之间的蛋白-蛋白相互作用图谱。这种方法及其产生的数据已给出了大量关于病毒如何操纵它们感染的宿主细胞和引起疾病的信息。这项研究的发现包括雌激素受体在调节寨卡病毒感染中的作用和人乳头瘤病毒(HPV)如何导致癌症。相关研究结果于2019年8月29日在线发表在Cell期刊上,论文标题为“A Structure-Informed Atlas of Human-Virus Interactions”。论文通讯作者为哥伦比亚大学医学中心的Sagi Shapira博士和Barry Honig博士。

图片来自Sagi Shapira, PhD, Columbia University Vagelos College of Physicians and Surgeons。
在分子水平上,病毒侵入细胞并操纵细胞进行复制、存活并引发疾病。鉴于它们依赖于人体细胞完成它们的生命周期,因此病毒利用细胞功能的一种方式是通过宿主细胞内的蛋白-蛋白相互作用。类似地,细胞通过启动控制和限制病毒复制的免疫应答来对病毒感染作出反应 ,这也依赖于蛋白-蛋白相互作用。
迄今为止,已经投入了大量精力来鉴定这些关键的相互作用---这些努力中的一些产生了许多基本发现,其中的一些基本发现具有治疗意义。然而,传统方法在可扩展性、效率甚至获取方面受到限制。为了应对这一挑战,Shapira博士及其合作者开发并执行了一个计算框架---P-HipsTer,它可推导病毒性病原体蛋白和人类蛋白之间的相互作用。
11.Cell:科学家成功筛选出开发新型癌症免疫疗法的关键靶点
doi:10.1016/j.cell.2019.07.044
在过去10年里免疫疗法给癌症治疗带来了革命性的变革,然而很多肿瘤对这些新型疗法并没有反应,近日,来自耶鲁大学的科学家们通过研究对T细胞中2万个人类基因进行全基因组筛选,鉴别出了多个新型候选基因,其能促进机体免疫系统攻击多种类型的肿瘤,相关研究结果刊登在国际杂志Cell上。
研究者Sidi Chen教授说道,免疫疗法对于所有患者并非都有效果,大约70%-80%的患者对疗法并无反应;那么我们为何不从基因层面进行研究来分析哪些基因主要负责肿瘤生长,同时寻找开发新型癌症疗法的潜在靶点;很多免疫疗法都基于抑制PD1基因而开发,PD-1能抑制T细胞动员并攻击肿瘤细胞的能力,这些疗法明显提高了多种类型癌症患者的存活率,比如黑色素瘤和肺癌等,然而即便在这些癌症中,也仅有30%-40%的患者对免疫疗法能产生反应,对于大多数癌症类型而言,患者的反应率在20%以下,某些恶性肿瘤患者的反应率甚至在10%以下。
研究人员开发的新型平台能利用CRISPR基因编辑技术敲除小鼠机体中的基因来观察哪种基因对机体免疫系统对肿瘤产生的反应效应最大,其中研究者鉴别出的一个基因名为DHX37,其能够有效抑制小鼠机体中CD8杀伤性T细胞对肿瘤的反应,当DHX37基因被编辑后,患三阴性乳腺癌的小鼠机体中的肿瘤尺寸会明显下降。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


