慢性肾脏病相关性瘙痒(CKD-aP)突破性药物!外周κ阿片受体(KOR)激动剂Korsuva(difelikefalin)申请上市!
来源:本站原创 2020-12-29 01:31
Korsuva是一款突破性药物,在3期临床显著改善瘙痒强度和生活质量。

2020年12月28日讯 /生物谷BIOON/ --Cara Therapeutics是一家临床阶段的生物制药公司,专注于开发和商业化新的化学物质,旨在通过选择性靶向外周κ阿片受体(KOR)来缓解瘙痒。近日,该公司宣布,已向美国食品和药物管理局(FDA)提交了Korsuva(CR845,difelikefalin)注射液的新药申请(NDA),用于治疗血液透析患者的中度至重度瘙痒。此前,FDA已授予Korsuva治疗该适应症的突破性药物资格(BTD)。Cara Therapeutics已要求FDA对NDA进行优先审查,如果获准,其审查周期将比常规审查缩短4个月。
慢性肾脏疾病相关性瘙痒(CKD-aP)是接受血液透析的慢性肾脏病患者中发生的一种疾病,许多透析患者(60-70%)会出现瘙痒,30-40%的病例报告为中度或重度。
Korsuva活性药物成分为difelikefalin,这是一种首创(first-in-class)KOR激动剂,作用于人体外周神经系统和某些免疫细胞。
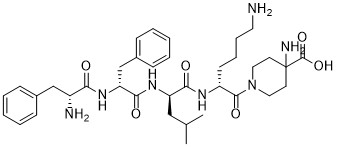
difelikefalin化学结构式(图片来源:medkoo.com)
此次NDA,基于2项关键3期临床试验的阳性数据,包括在美国开展的KALM-1试验和全球性KALM-2试验,以及来自额外32项临床研究的支持性数据。在3期临床试验中,伴有中度至重度CKD-aP的血液透析患者,接受Korsuva注射液治疗后,瘙痒强度和生活质量指标均表现出统计学意义的显著改善。
Cara Therapeutics总裁兼首席执行官Derek Chalmers博士表示:“Korsuva注射液NDA提交,标志着Cara和患有顽固性瘙痒的血液透析患者的一个重要里程碑。我要感谢整个Cara团队,感谢他们不懈努力,从内部发现、到开发、到完成NDA提交,以及参与临床试验的患者、研究人员和现场人员。我们期待着在审查过程中与FDA合作,并与我们的商业合作伙伴Vifor Pharma一起,继续专注于Korsuva注射剂在美国上市的准备工作。”
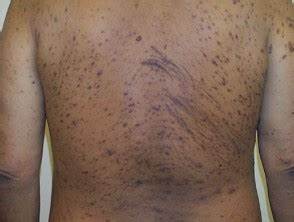
慢性肾脏病相关瘙痒症(CKD-aP,图片来源:DermNet NZ)
慢性肾病相关性瘙痒(CKD-aP)是一种难治性全身瘙痒病,在接受透析的慢性肾脏疾病患者中发生频率高、强度大。在没有透析的III-V期CKD患者中也有瘙痒的报道。综合、纵向、多国研究估计,终末期肾病(ESRD)患者CKD-aP的加权患病率约为40%,约25%的患者报告严重瘙痒。
大多数透析患者(约60%至70%)报告瘙痒,其中30%至40%报告中度或重度瘙痒。来自ITCH National Registry Study(瘙痒国家注册研究)的最新数据显示,在瘙痒患者中,约59%的患者每天或几乎每天都会出现症状,持续一年以上。鉴于其与CKD/ESRD的关系,大多数患者将持续数月或数年的症状,目前使用的止痒药,如抗组胺药和皮质类固醇,无法提供一致的、充分的缓解。中重度慢性瘙痒反复被证明直接降低生活质量,导致损害生活质量的症状(如睡眠质量差),并与抑郁相关。CKD-aP也是血液透析患者死亡率的独立预测因子,主要与炎症和感染风险增加有关。(生物谷Bioon.com)
原文出处:Cara Therapeutics Submits New Drug application to U.S. Food and Drug Administration for KORSUVA™ Injection in Hemodialysis Patients with Moderate-to-Severe Pruritus
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


