美国FDA授予默沙东口服抗病毒药物molnupiravir紧急使用授权(EUA):治疗高危轻中度COVID-19患者!
来源:本站原创 2021-12-27 01:30
molnupiravir是一种口服强效核糖核苷类似物,可抑制多种RNA病毒的复制,包括新型冠状病毒(SARS-CoV-2)。

2021年12月26日讯 /生物谷BIOON/ --默沙东(Merck & Co)与Ridgeback Biotherapeutics近日联合宣布,美国食品和药物管理局(FDA)已授予molnupiravir(MK-4482/EIDD-2801)紧急使用授权(EUA),该药是一种口服抗病毒药物,用于治疗:(1)直接SARS-CoV-2病毒检测为阳性结果且有高风险发展为严重COVID-19(包括住院或死亡)的轻度至中度COVID-19患者;(2)直接SARS-CoV病毒检测为阳性结果且对于FDA授权的COVID-19治疗方案不可及或临床上不适用的轻度至中度COVID-19患者。
用药方面,molnupiravir应在确诊为COVID-19并在症状出现后5天内尽快给药,推荐剂量为800mg(4粒200mg胶囊),每12小时口服一次,连续5天,可与或不与食物同服。完成为期5天的完整疗程对于最大限度地清除病毒和减少SARS-CoV-2的传播非常重要。
需要指出的是,molnupiravir不推荐用于怀孕的患者。根据动物繁殖研究的结果,molnupiravir给怀孕的动物服用时可能会对胎儿造成伤害。
此次EUA,基于3期MOVe-OUT临床试验的结果。该试验在患有轻度至中度COVID-19、有风险发展为严重COVID-19和/或住院的成人患者中开展,评估了molnupiravir(800mg,每日2次)的疗效和安全性。入组的这些患者,未接种疫苗预防SARS-CoV-2感染、经实验室检测确认为SARS-CoV-2感染、在症状出现后5天内随机化、至少有一个与不良疾病结果相关的风险因素(如心脏病、糖尿病)。
对所有随机化患者(n=1433)开展的分析显示:与安慰剂相比,molnupiravir降低了住院或死亡风险:安慰剂组有9.7%(n=68/699)的患者住院或死亡,molnupiravir治疗组为6.8%(n=48/709),绝对风险降低为3.0%(95%CI:0.1,5.9)。安慰剂组报告9例死亡,molnupiravir治疗组为1例。
主要疗效的确定基于对762例患者的计划中期分析。在中期分析中,至第29天,与安慰剂相比,molnupiravir治疗将住院或死亡风险显著降低了50%:安慰剂组有14.1%(n=53/377)的患者住院或死亡,molnupiravir治疗组为7.3%(n=28/385),绝对风险降低为6.8%(95%CI:2.4,11.3;p=0.0024)。
该研究中,molnupiravir最常见的不良反应(发生率≥1%)为腹泻(molnupiravir 2% vs 安慰剂2%)、恶心(molnupiravir 1% vs 安慰剂1%)、恶心(molnupiravir 1% vs 安慰剂1%)、头晕(molnupiravir 1% vs 安慰剂1%)。molnupiravir治疗组因不良事件而中断治疗的患者较少( 1% vs 3%)、严重不良事件发生率也较低(7% vs 10%),最严重的AE为COVID-19相关。
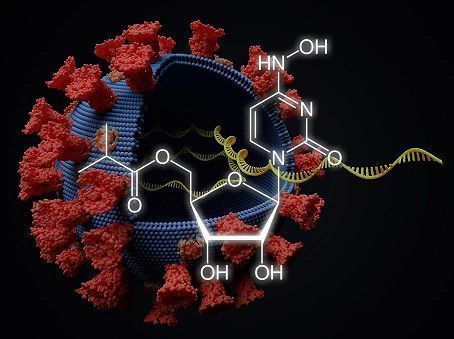
molnupiravir化学结构式(图片来源:scinexx.de)
molnupiravir是一种口服给药的强效核糖核苷类似物,可抑制多种RNA病毒的复制,包括新型冠状病毒(SARS-CoV-2),这是导致COVID-19的病原体。molnupiravir已被证明在SARS-CoV-2的几个临床前模型中具有活性,包括用于预防、治疗和预防传播,在SARS-CoV-1和MERS的临床前模型中也显示出活性。
今年11月,molnupiravir获得英国药品和保健品管理局(MHRA)批准,用于治疗SARS-CoV-2诊断检测为阳性且至少有一种发生严重疾病的风险因素的轻中度COVID-19成人患者。在英国,molnupiravir的拟定商标名为Lagevrio。值得一提的是,molnupiravir是第一个被批准用于治疗COVID-19的口服抗病毒药物。
MOVe-OUT(MK-4482-002;NCT04575597)是一项全球性2/3期、随机、安慰剂对照、双盲、多地点研究,入组对象是实验室检测确认为轻度至中度COVID-19的非住院成人患者(年龄≥18岁),这些患者未接种SARS-CoV-2疫苗、至少有一个与不良疾病结局相关的风险因素、并且在随机化前5天内出现症状。
该试验的3期部分在全球范围内开展,患者以1:1的比例随机分为2组,每天2次,口服molnupiravir(800mg)或安慰剂,为期5天。主要疗效目标是通过从随机分组至第29天期间住院和/或死亡的患者百分比来评估molnupiravir与安慰剂的疗效。
该试验中,最常见的疾病预后不良风险因素包括肥胖、高龄(>60岁)、糖尿病和心脏病。Delta、Gamma、Mu变体占中期分析时已测序的基线病毒变体的近80%。拉丁美洲、欧洲、非洲的招募患者人数分别占研究人群的56%、23%、15%。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


