2023年5月Cell期刊精华
来源:生物谷原创 2023-05-31 10:14
2023年5月份即将结束,5月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
2023年5月份即将结束,5月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:成功解析Spns2转运体的低温电镜结构,为药物开发铺平了道路
doi:10.1016/j.cell.2023.04.028
在一项新的研究中,来自美国圣犹达儿童研究医院和德克萨斯大学西南医学中心的科研究人员研究了一种参与癌症和免疫的转运体的结构和功能。他们捕获了该转运体的六种结构,包括它与抑制剂结合时的结构,为了解它的工作方式提供了前所未有的见解。这一发现对药物开发有影响。相关研究结果于2023年5月23日在线发表在Cell期刊上,论文标题为“Structural and functional insights into Spns2-mediated transport of sphingosine-1-phosphate”。
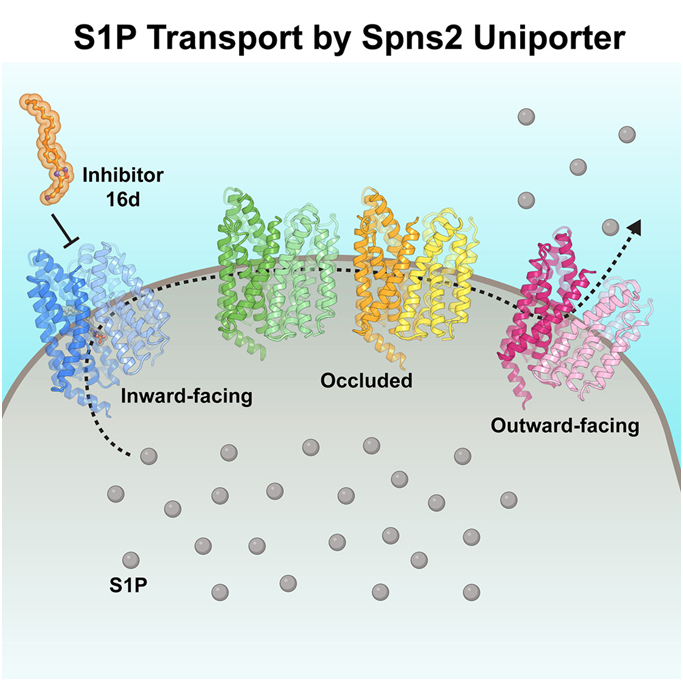
图片来自Cell, 2023, doi:10.1016/j.cell.2023.04.028。
这些作者获得了Spns2的六种低温电镜(cryo-EM)结构,包括两种与功能相关的中间构象(形状),它们连接着向内(细胞内)和向外(细胞外)的状态。这些发现揭示了S1P转运周期的结构基础。论文共同通讯作者、圣犹达儿童研究医院结构生物学系的Chia-Hsueh Lee博士说,“我们希望我们的结构信息将为将来开发的改进的、更具特异性的靶向Spns2的小分子铺平道路。我认为在治疗上抑制Spns2转运体有巨大的潜力。”
论文共同第一作者、圣犹达儿童研究医院结构生物学系的Shahbaz Ahmed博士说,“我们使用低温电镜来捕捉这种转运体的结构,并发现它如何将S1P转移到细胞外。我们还研究了一种抑制剂,并提供了结构数据,说明它如何结合这种转运体并阻断它的活性。”
这些作者研究了Spns2如何与抑制剂16d结合,16d是一种特殊的小分子,已经显示出极少的脱靶效应。他们发现,16d通过将Spns2锁定在向内状态来阻断它的转运活性。这项研究有助于开发先进的Spns2抑制剂。
2.Cell:蝙蝠蛋白ASC2强效抑制炎性体的能力有望开发对抗人类炎症性疾病的新策略
doi:10.1016/j.cell.2023.03.036
在一项新的研究中,来自杜克-新加坡国立大学医学院的研究人员通过研究蝙蝠在没有明显疾病的情况下容纳病毒的不寻常能力,发现了一种可能开启对抗人类炎症性疾病的新策略的蛋白。相关研究结果发表在2023年5月11日的Cell期刊上,论文标题为“Bat ASC2 suppresses inflammasomes and ameliorates inflammatory diseases”。
这项新的研究着重关注称为炎性体(inflammasome)的多蛋白复合物,这类蛋白复合物这种复合物负责过度活跃的炎症,从而导致许多疾病中的严重症状。炎性体也与衰老过程中的功能衰退有关。
这些作者发现一种名为ASC2的蝙蝠蛋白具有抑制炎性体的强大能力,从而限制了炎症的发生。论文共同第一作者兼论文共同通讯作者Matae Ahn博士解释说,“这表明ASC2的高水平活性是蝙蝠控制炎症的一个关键机制,对它们的长寿命和作为病毒储存库的独特地位有影响。”
论文共同第一作者、杜克-新加坡国立大学医学院博士生Vivian Chen强调,这些作者能够通过展示这种蝙蝠蛋白在小鼠身上的有效性来证明它在人类身上的潜力。她阐述说,“在经过基因改造的小鼠中表达这种蝙蝠蛋白可以抑制炎症,并减少由多种诱因(包括病毒)驱动的疾病的严重性。”
对ASC2蛋白的详细研究发现这种蝙蝠蛋白分子中的四个氨基酸是使它比其相应的人类蛋白更有效地抑制炎症的关键。这为开发能够模拟这种蝙蝠蛋白的抗炎作用的药物提供了宝贵的见解。
3.Cell:揭示RNA聚合酶驱动核糖核苷酸切除修复机制
doi:10.1016/j.cell.2023.04.029
在一项新的研究中,来自美国纽约大学朗格尼健康中心的研究人员描述了一种DNA修复途径背后的分子机制,该修复途径能够对抗将某种类型的核糖核苷酸错误地整入遗传密码。这种错误在细菌和其他有机体的遗传代码复制过程中经常发生。相关研究结果于2023年5月16日在线发表在Cell期刊上,论文标题为“RNA polymerase drives ribonucleotide excision DNA repair in E. coli”。
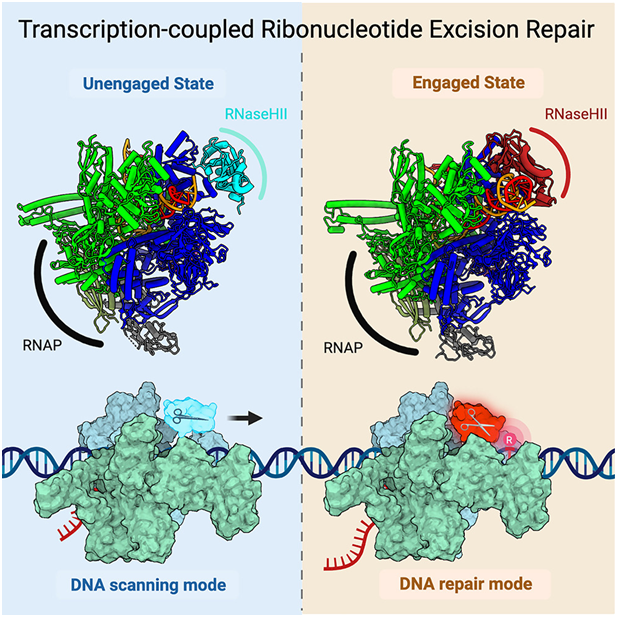
图片来自Cell, 2023, doi:10.1016/j.cell.2023.04.029。
鉴于核糖核苷酸的错误整入会导致有害的DNA代码变化(突变)和DNA断裂,所有有机体都进化出了一种叫做核糖核苷酸切除修复(ribonucleotide excision repair, RER)的DNA修复途径,可以快速修复此类错误。
如今,这项新的研究提供了第一个证据,表明像在NER途径中一样,RER与转录紧密相连。这些作者发现证据表明,参与RER的关键酶RNaseHII也与RNA聚合酶合作,因为它在活的细菌细胞的DNA链中扫描错误整入的核糖核苷酸。
Nudler说,“我们的结果继续激励人们重新思考DNA修复领域的某些基本原则。在未来,我们的团队计划研究RNA聚合酶是否扫描DNA中出现的一系列问题,并在全基因组范围内触发修复,不仅在细菌中是如此,而且在人类细胞中也是如此。”
论文第一作者、Nudler实验室博士后学者Zhitai Hao说,“这项新的研究支持一种模型,即RNaseHII在沿着DNA移动时骑在RNA聚合酶上扫描DNA上错误整入的核糖核苷酸。这项研究对于我们对DNA修复过程的基本了解至关重要,并具有深远的临床意义。”
4.Cell:诱导R环形成有望治疗脆性X综合征
doi:10.1016/j.cell.2023.04.035
脆性X综合征(fragile X syndrome)是导致自闭症谱系障碍的一个主要原因。这种疾病的特征为FMR1基因的DNA序列中某些核苷酸的遗传性重复。在一项新的研究中,来自美国麻省总医院的研究人员发现了一种治疗脆性X综合征的潜在方法。相关研究结果于2023年5月19日在线发表在Cell期刊上,论文标题为“Site-specific R-loops induce CGG repeat contraction and fragile X gene reactivation”。
论文通讯作者、麻省总医院分子生物学家Jeannie T. Lee博士解释说,“我们想知道是否可以通过减少FMR1中的三核苷酸重复序列并恢复FMRP表达来治疗脆性X综合征。当业界正试图通过基因疗法和基因编辑来恢复FMRP的表达时,我们的方法是减少CGG重复,通过刺激人体自身的DNA修复机制来恢复这种蛋白的表达。”
通过构建脆性X综合征患者细胞衍生性的模型,并将这些模型暴露在不同的实验室条件下,Lee和论文第一作者、麻省总医院博士后学者Hun-Goo Lee博士发现了诱发强烈的三核苷酸重复序列减少和完全的FMR1重新激活的条件。这种条件需要有称为MEK和BRAF的两种激酶的抑制剂存在。
抑制两种激酶会导致DNA和RNA之间形成的称为“R环(R-loop)”的特殊核酸结构的产生,细胞将这种结构视为DNA损伤,并因此触发修复机制来进行修复。细胞的修复机制随后切除扩张的CGG重复序列,以达到正常的CGG水平,使细胞能够重新表达关键的FMR1基因。
5.Cell:成功解析出Commander蛋白复合物的三维结构
doi:10.1016/j.cell.2023.04.003
在一项新的研究中,来自澳大利亚昆士兰大学和英国布里斯托大学的研究人员利用人工智能建立了称为Commander蛋白复合物(Commander complex)的关键细胞成分的三维图谱,以更好地了解痴呆症和包括COVID-19在内的传染病。相关研究结果发表在2023年5月11日的Cell期刊上,论文标题为“Structure of the endosomal Commander complex linked to Ritscher-Schinzel syndrome”。论文通讯作者为昆士兰大学分子生物科学研究所的Brett Collins教授和布里斯托大学的Pete Cullen教授。
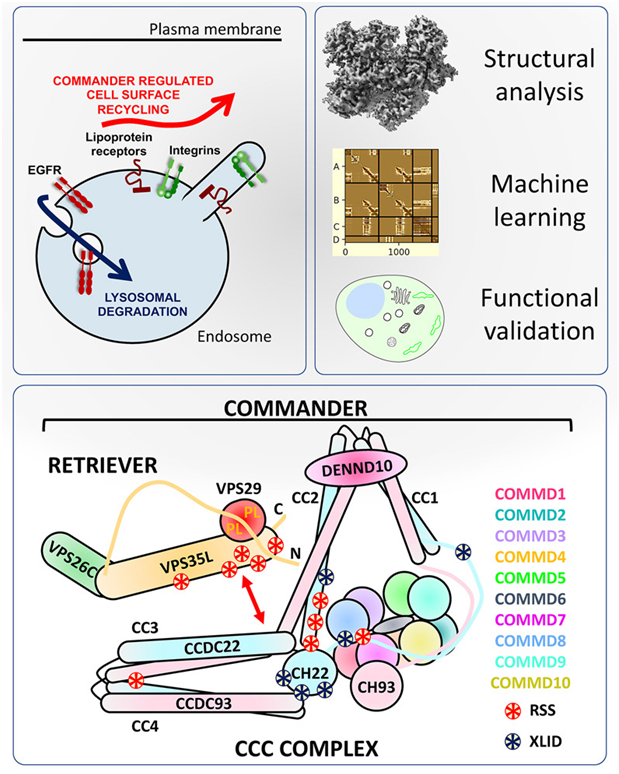
图片来自Cell, 2023, doi:10.1016/j.cell.2023.04.003。
Commander复合物由16个亚基组成,在细胞中充当“邮递员”的作用。Collins教授说,“正如邮政系统有运输和分拣货物的过程一样,我们体内的细胞有运输和分拣蛋白的分子机器。货物运输就是要在正确的时间将正确的包裹送到正确的目的地,而在细胞中,Commander复合物控制着这个系统,以确保正确数量的蛋白被运输到正确的地方。”
这种蛋白运输系统牵涉到许多疾病,包括心脏病、阿尔茨海默病和感染。Collins教授说,“了解这些蛋白的三维形状有助于我们了解它们是如何运作的,为什么它们发生突变会导致疾病,以及未来如何设计药物来靶向它们。导致导致COVID-19的冠状病毒SARS-CoV-2和可导致癌症的类乳头瘤病毒(HPV)需要Commander复合物来感染细胞,而且它与阿尔茨海默病中淀粉样蛋白的运输有关。Commander复合物发生的突变破坏了进入细胞的脂质运输,导致高胆固醇和患有罕见的Ritscher-Schinzel综合征(Ritscher-Schinzel syndrome)的人的心脏缺陷,综合征的特点是智力障碍和发育迟缓。了解Commander复合物的结构意味着我们可以更好地了解这种情形是如何发生的,并推进我们对它如何参与疾病的理解。”
6.Cell:成功构建出可以研究人类小胶质细胞的发育和功能的类器官模型
doi:10.1016/j.cell.2023.04.022
小胶质细胞位于人类免疫系统和大脑的交汇处,是一种专门的大脑免疫细胞,在发育和疾病中发挥着至关重要的作用。尽管小胶质细胞的重要性是无可争议的,但对它们进行建模和研究仍然是一项艰巨的任务。
与一些可以在体外或非人类模型中研究的人类细胞不同,当将人类小胶质细胞从人脑环境中移除时,很难对它们进行研究。为了克服这一障碍,来自美国索尔克生物科学研究所的研究人员在一项新的研究中开发出一种类器官(organoid)模型,即一种模拟人体组织特征的三维细胞集合。该模型使得他们能够首次在人类来源的活组织中研究人类小胶质细胞的发育和功能。此外,他们研究了患有巨头畸形自闭症谱系障碍(macrocephalic autism spectrum disorder, 在这种疾病中,患儿头围大于大于97%的其他婴儿)的儿童的患者源性小胶质细胞,以确定大脑环境是否会影响更具反应性的小胶质细胞的发育。这些研究结果强调了免疫细胞和大脑相互作用的重要性,并提高了对神经退行性和发育性疾病的理解,如自闭症谱系障碍和阿尔茨海默病。相关研究结果发表在2023年5月11日的Cell期刊上,论文标题为“An in vivo neuroimmune organoid model to study human microglia phenotypes”。
论文通讯作者、索尔克生物科学研究所的Fred H. Gage教授说,“在大脑环境之外,小胶质细胞几乎失去了所有的功能和意义。我们知道,如果我们找到了一种在类器官中复制人类大脑环境的方法来研究人类小胶质细胞,那么我们最终将有一种工具来研究健康和患病的大脑如何影响小胶质细胞以及健康和患病小胶质细胞如何影响大脑。”
与之前的模型不同,这些作者构建了一种具有小胶质细胞和类似于人类大脑环境的人类大脑类器官,这最终使他们能够观察在整个大脑发育过程中大脑环境对小胶质细胞的影响。他们发现,一种名为SALL1的特征性蛋白早在发育11周时就出现了,用于确认小胶质细胞的身份并促进它们出现成熟时的功能。此外,他们发现大脑环境特异性因子,比如蛋白TMEM119和P2RY12,是小胶质细胞发挥功能所必需的。
论文共同作者、索尔克生物科学研究所副教授Axel Nimmerjahn说,“构建一种能够有效复制人类大脑环境的人类大脑模型是非常令人兴奋的。有了这种模型,我们终于可以研究人类小胶质细胞在人类大脑环境中的功能。”
7.Cell:经改造后携带Myomaker和Myomerger的包膜病毒有望治疗杜兴氏肌肉萎缩症
doi:10.1016/j.cell.2023.03.033
美国辛辛那提儿童医院分子心血管生物学部门的Doug Millay博士一直致力于揭示骨骼肌发育的最基本机制。他在研究两种名为Myomaker和Myomerger的“促融剂(fusogen)”如何介导肌肉干细胞产生成熟肌肉细胞从而构建人类赖以运动、呼吸和生存的组织方面一直处于领先地位。
如今,Millay及其同事们的一些基本发现正在转化为对杜兴氏肌肉萎缩症(Duchenne muscular dystrophy, DMD)患者的潜在治疗。在一项新的研究中,他们发现在小鼠身上,经基因改造后携带Myomaker和Myomerger的改良包膜病毒会导致与肌肉细胞之间的特异性融合。因此,这种改良病毒可被用作载体,递送肌肉功能所需的一个在DMD患者身上发生了突变的重要基因。相关研究结果于2023年4月18日在线发表在Cell期刊上,论文标题为“Enveloped viruses pseudotyped with mammalian myogenic cell fusogens target skeletal muscle for gene delivery”。
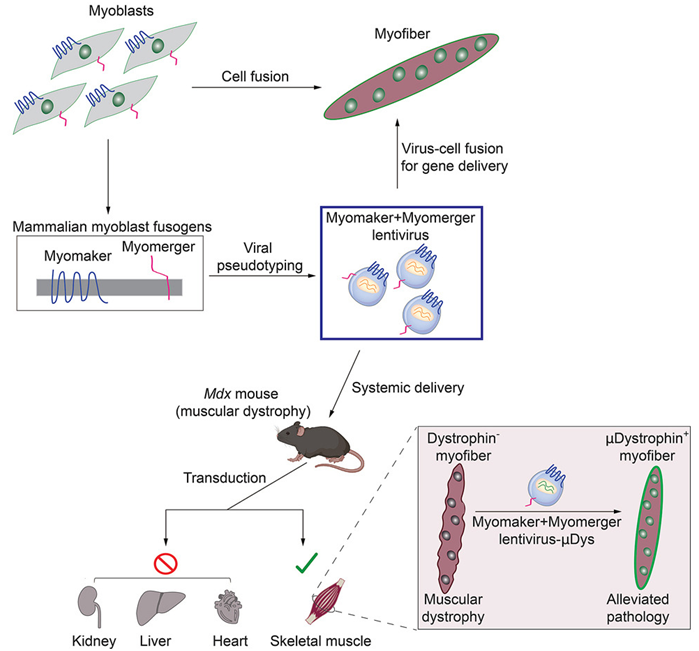
图片来自Cell, 2023, doi:10.1016/j.cell.2023.03.033。
在这项新的研究之前,一个关键的未知数是像Myomaker和Myomerger这样主要在细胞上发挥作用的蛋白,是否能在病毒上发挥作用。论文第一作者、辛辛那提儿童医院分子心血管生物学部门成员Sajedah Hindi博士接受了挑战,测试了这个想法。
Hindi首先设计了一种将Myomaker和Myomerger放在病毒表面的策略,并发现它们在体外培养的细胞中具有功能性。她继续利用她在骨骼肌生物学方面的丰富经验,在小鼠身上测试这种新型载体的功效。
Millay说,“这种改良的病毒载体似乎是一种有希望的工具,可以递送一个在DMD患者中是缺乏的基因,而且这个基因是潜在终身供应的。这种载体的独特优势提供了一个机会,对针对无数肌肉疾病的基因疗法产生重大影响。”
8.Cell:利用新型碱基编辑技术研究单核苷酸变异对人类造血干细胞的影响
doi:10.1016/j.cell.2023.03.035
在一项新的研究中,来自美国哈佛医学院、布罗德研究所和哈佛干细胞研究所等研究机构的研究人员使用了一种高度精确的称为碱基编辑(base editing)的基因组编辑技术,对来自患者骨髓的造血干细胞进行了数百次直接编辑。相关研究结果于2023年5月2日在线发表在Nature期刊上,论文标题为“Massively parallel base editing to map variant effects in human hematopoiesis”。
这项新的研究是第一次将这种高通量的碱基编辑技术应用于造血干细胞,该技术可以同时在许多细胞中对DNA进行许多单碱基替换。这些作者展示了基因中的这些单核苷酸变化如何影响血细胞的生物学,并有助于治疗包括白血病和镰状细胞病在内的疾病。这些发现表明该技术如何能够帮助科学家们在多种细胞类型中更多地了解基因变体在疾病中的作用。
论文通讯作者、布罗德研究所副研究员Vijay Sankaran说,“我们的方法使我们不仅能够了解某个特定的基因是否可能与人类疾病有关,而且能够了解该基因的个别变化如何在分子水平上发挥作用。这种更精细的分辨率为我们提供了一个关于疾病如何发生以及如何治疗的新路线图。”
9.Cell:新研究揭示β-arrestin作用机制
doi:10.1016/j.cell.2023.04.018
在一项新的研究中,由英国伯明翰大学的Davide Calebiro教授领导的一个国际研究小组利用先进的显微镜技术首次以前所未有的细节观察到了像空中交通管制员一样发挥作用的管理着进出人类细胞的信号流的蛋白。他们观察到这种称为β-arrestin的蛋白是如何工作的。相关研究结果于2023年5月4日在线发表在Cell期刊上,论文标题为“Plasma membrane preassociation drives β-arrestin coupling to receptors and activation”。
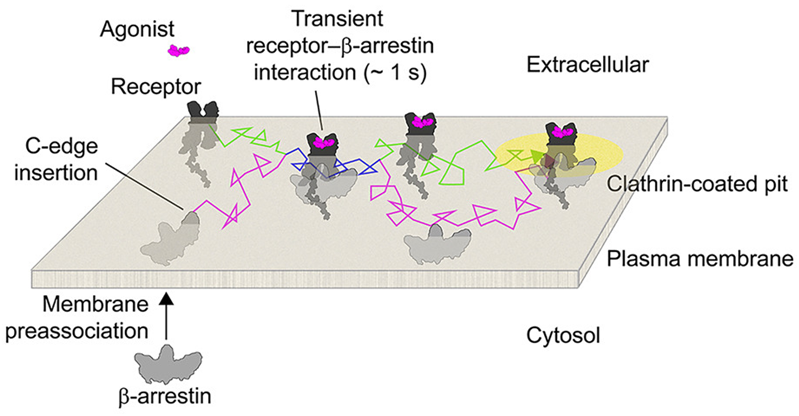
图片来自Cell, 2023, doi:10.1016/j.cell.2023.04.018。
β-arrestin参与控制G蛋白偶联受体(GPCR)的活性,其中GPCR是人体中最大的一组受体,介导许多激素和神经递质的作用。因此,GPCR是药物开发的主要靶标,目前所有的治疗药物中有30%至40%靶向这些受体。一旦GPCR被激活,β-arrestin就会在一种称为脱敏(desensitization)的过程中抑制这种信号传导,不过它也可以介导自己的信号。
这项新的研究意外地发现β-arrestin将自己附着在细胞外膜上,等待荷激素或神经递质到达受体。令人惊讶的是,β-arrestin和活性受体之间的相互作用比以前认为的要动态得多,从而可以更好地控制受体介导的信号传导。
Calebiro说,“在我们的研究中,我们使用了我们实验室开发的创新单分子显微镜和计算方法,首次以前所未有的细节观察单个β-restin分子如何在我们的细胞中工作。我们揭示了一种新的机制,解释了β-arrestin如何能够与细胞质膜上的受体有效地相互作用。这类蛋白就像空中交通管制员一样,当受体被一种激素或神经递质激活时,它们就会感知,从而调节我们细胞内的信号流。通过这样做,它们在信号脱敏中发挥了关键作用,其中信号脱敏是一种基本的生物过程,使我们的机体能够适应长时间的刺激。这些结果非常出人意料,可能为心力衰竭和糖尿病等疾病的新型治疗方法或开发更有效和更耐受的镇痛剂铺平道路。”
10.Cell:基于迷幻药伊博格碱,开发出两种可能用于治疗成瘾和抑郁症的新候选药物
doi:10.1016/j.cell.2023.04.010
在一项新的研究中,来自美国加州大学旧金山分校、耶鲁大学和杜克大学的研究人员根据非洲传统迷幻植物药物伊博格碱(ibogaine)的药理学原理,开发出两种可能用于治疗成瘾和抑郁症的新候选药物。在非常低的剂量下,这两种新的化合物能够减轻小鼠这两种疾病的症状。相关研究结果于2023年5月2日在线发表在Cell期刊上,论文标题为“Structure-based discovery of conformationally selective inhibitors of the serotonin transporter”。
这些研究结果从伊博格碱对5-羟色胺转运体(serotonin transporter, SERT)的影响中得到启发,SERT也是氟西汀(fluoxetine, 商品名为Prozac)等SSRI抗抑郁药的作用靶标。这些作者虚拟地筛选了2亿种分子结构,以找到与伊博格碱相同方式阻断SERT的分子。
论文共同通讯作者、加州大学旧金山分校药学院教授Brian Shoichet博士说,“有些人相信伊博格碱可以治疗成瘾,但它并不是一种很好的药物。它有不好的副作用,而且在美国还没有被批准使用。我们的化合物只是模拟了伊博格碱众多药理作用中的一种,而且仍然重现了它对行为最理想的影响,至少在小鼠身上是这样。”其他的论文共同通讯作者为加州大学旧金山分校的Allan Basbaum博士和Aashish Manglik博士;耶鲁大学的Gary Rudnick博士;杜克大学的Bill Wetsel博士。
这些作者证实了这两种新的化合物的现实前景,它们最初是用Shoichet开发的计算对接方法鉴定出来的。这种计算对接方法涉及系统地测试与蛋白结合的虚拟化学结构,使科学家们能够确定新的药物线索,而不必在实验室中合成它们。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


