Nat Cancer:揭示癌细胞如何产生PD-L1实现免疫逃逸!
来源:本站原创 2020-05-04 08:18
2020年5月4日讯 /生物谷BIOON /——针对癌细胞表面一种名为"程序性死亡配体1"(PD-L1)的蛋白质的免疫治疗药物已迅速成为治疗多种癌症的主要手段,通常效果显着。但确切地说,癌细胞是如何激活这种蛋白质的还不完全清楚。而德克萨斯大学西南医学中心科学家的最新相关研究成果近日发表在Nature Cancer杂志上,揭示了这一机制的关键部分。这些发现可能提
2020年5月4日讯 /生物谷BIOON /——针对癌细胞表面一种名为"程序性死亡配体1"(PD-L1)的蛋白质的免疫治疗药物已迅速成为治疗多种癌症的主要手段,通常效果显着。但确切地说,癌细胞是如何激活这种蛋白质的还不完全清楚。而德克萨斯大学西南医学中心科学家的最新相关研究成果近日发表在Nature Cancer杂志上,揭示了这一机制的关键部分。这些发现可能提供新的靶点,可能进一步改善目前癌症免疫治疗的效果。
近10年前,美国FDA批准了一种名为检查点抑制剂(checkpoint inhibitors)的新型药物中的第一种药物。这些药物逆转了许多类型的癌细胞用来避免被免疫系统发现的隐藏机制,允许名为T细胞的抗癌免疫细胞攻击肿瘤。阻断其中一种隐形蛋白PD-L1与其T细胞表面受体之间的相互作用是目前市场上几种药物的基础,包括nivolumab、pembrolizumab和atezolizumab。
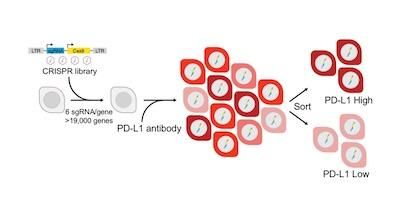
图片来源:UTSW
尽管这些药物已经在几种癌症上取得了进展,尤其是非小细胞肺癌(NSCLC)--世界范围内与癌症相关的死亡的主要原因--但癌细胞如何过度表达PD-L1以保护自己免受免疫系统攻击仍是一个谜。
为了回答这个问题,德克萨斯大学西南分校的分子生物学副教授Kathryn A. O'donnell博士和她的同事们开始广泛研究哪些基因可能作为调节因子在非小细胞肺癌中制造PD-L1。研究人员使用CRISPR技术,像分子剪刀一样去除特定的基因,他们分别从一个人类NSCLC细胞系中去除了19000个基因。然后,他们使用一种荧光PD-L1抗体来检测哪些细胞具有更多或更少的PD-L1。这使得他们能够识别那些通常会促进PD-L1产生的基因,即阳性调节基因,以及那些阻碍PD-L1产生的基因,即阴性调节基因。
令人惊讶的是,他们发现一种制造PD-L1的有效抑制剂是一种叫做UROD的基因,它在产生血红素的过程中起着关键作用。这种含铁的化学物质是红细胞中携带氧气的关键,同时也是维持正常平衡或体内平衡所必需的。为了证实这些发现,研究人员使用了其他方法来去除NSCLC细胞中的血红素,这也触发了肺癌细胞产生更多的PD-L1蛋白。当UROD被耗尽的肿瘤被移植到健康小鼠体内时,它们的生长速度明显快于那些免疫系统不正常的小鼠。O'Donnell说,这些发现表明,通过激活PD-L1的产生,这种基因通过抑制抗肿瘤免疫来加速癌症。
进一步的实验表明,阻碍血红素的产生开启了一种被称为综合应激反应(ISR)的途径,这种途径被细胞广泛用于处理各种应激条件,如缺氧、毒素或营养缺乏。在这种情况下,NSCLC细胞利用一种特殊的机制,依靠一种被称为eIF5B的蛋白质来增加PD-L1的产生。研究人员发现,即使不干扰血红素的合成,只要用这种单一的蛋白质刺激细胞,就可以增加PD-L1的产生。
O'Donnell和她的团队通过检查各种癌症中过量或少量产生eIF5B的基因数据库,发现编码eIF5B的基因在肺癌中经常过量产生,而这种过量产生在肺癌患者中是预后不良的一个标志。"开发专门针对这种蛋白或其他参与制造PD-L1的蛋白的新药,可能有助于提高目前使用的免疫治疗药物的成功率,"O'Donnell说,她也是德克萨斯大学西南医学中心Harold C. Simmons综合癌症中心的成员。
该研究的第一作者、O'Donnell课题组前成员Shruthy Suresh博士说:"研究癌症患者的应激反应和免疫逃避之间的关系将是未来工作的一个重要重点。"(生物谷Bioon.com)
参考资料:
Suresh, S., Chen, B., Zhu, J. et al. eIF5B drives integrated stress response-dependent translation of PD-L1 in lung cancer. Nat Cancer (2020). https://doi.org/10.1038/s43018-020-0056-0
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


