近期基因疗法研究领域重要成果!
来源:本站原创 2019-11-21 21:55
本文中,小编整理了多篇研究成果,共同解读科学家们在基因疗法研究领域取得的新成果,分享给大家!图片来源:www.pixabay.com【1】JCI:新技术提高基因疗法治疗视力的效果doi:10.1172/JCI129085在以大鼠,猪和猴子为模型的实验中,约翰霍普金斯大学医学院的研究人员开发了一种挽救视力的基因疗法。如果被证明对人类安全有效,该技术可以为诸如湿性年龄相关性黄斑变性(AMD)等常见疾病
本文中,小编整理了多篇研究成果,共同解读科学家们在基因疗法研究领域取得的新成果,分享给大家!

图片来源:www.pixabay.com
doi:10.1172/JCI129085
在以大鼠,猪和猴子为模型的实验中,约翰霍普金斯大学医学院的研究人员开发了一种挽救视力的基因疗法。如果被证明对人类安全有效,该技术可以为诸如湿性年龄相关性黄斑变性(AMD)等常见疾病的患者提供一种新的,更持久的治疗选择,并且它有可能替代遗传性视网膜疾病患者的缺陷基因。
这种新方法发表在最近的The Journal of Clinical Investigation杂志上。该方法使用一根小针将无害的,基因工程化的病毒颗粒注射到眼白与眼睛血管层之间的空间(称为脉络膜上腔)。从那里,病毒可以将治疗基因传递到视网膜细胞。尽管目前仅在动物身上进行过测试,但新的脉络膜上腔注射技术的侵入性较小,因为它不涉及视网膜的分离,并且理论上可以在门诊进行,这标志着新的治疗视力的基因疗法的问世。
【2】Science子刊:I期临床试验表明药物局部诱导的IL-12基因疗法有望治疗复发性胶质母细胞瘤患者
doi:10.1126/scitranslmed.aaw5680
在一项新的临床研究中,一种可诱导的肿瘤定位基因疗法首次在胶质母细胞瘤患者中进行了测试。这种由两部分组成的方法涉及将一个编码免疫激活物的基因注射到脑瘤部位中并服用一种激活这个基因的药物,从而导致免疫激活物---白细胞介素12(IL-12)---的产生和免疫细胞渗入到肿瘤组织中。这些结果还提示着这种治疗可能延长患者的生存期,相关研究结果发表在Science Translational Medicine期刊上。
研究者Frederick Lang表示,所有近期的证据都提示着如果你能真正让免疫系统攻击肿瘤,那么你就有增加治愈肿瘤的潜力,而且这项[研究]正朝着这个方向发展。我认为这是令人兴奋的。胶质母细胞瘤是一种侵袭性和致命性的脑癌形式,在确诊后仅有6至9个月的平均生存期。领导这项研究的哈佛医学院神经外科医生Antonio Chiocca说,即使采用标准治疗(手术切除全部或部分肿瘤,然后进行6周化放疗),“平均7个月内. . .肿瘤复发了”。
【3】Sci Rep:深入剖析microRNAs分子的功能或有望开发出新型疾病基因疗法
doi:10.1038/s41598-019-46841-1
日前,一项发表在国际杂志Scientific Reports上的研究报告中,来自东芬兰大学和牛津大学的科学家们通过研究发现,细胞中天然存在的小RNA分子—microRNA或许在细胞核中也大量存在;此前,microRNAs被认为主要存在于细胞质中,而研究者却发现,细胞核中microRNA的浓度会因缺氧状况而发生改变,而且microRNA在细胞核基因的表达中扮演着关键角色,相关研究结果对于开发新型基因疗法至关重要。
文章中,研究者分析了内皮细胞不同部位中microRNAs分子的特性,结果发现,大部分的microRNAs会在细胞核中富集,当研究人员将细胞培养物暴露于缺氧状态下时他们发现,单个microRNA浓度的变化主要发生在细胞质或细胞核中,microRNA在调节细胞中基因表达中所扮演的关键作用或许比此前研究人员认为的更为重要,比如,研究者发现,一种此前被认为与缺氧状况有关的分子microRNA-210实际上在细胞核中较为丰富,这一发现或许揭示了细胞适应缺氧环境的分子机制。
【4】Circulation:利用基因疗法抑制CaMKII,有望治疗CPVT遗传性心律失常
doi:10.1161/CIRCULATIONAHA.118.038514
在一项新的研究中,来自美国波士顿儿童医院的研究人员报道了在遗传性心律失常小鼠模型中利用基因疗法抑制了这种疾病。这些发现为开发治疗遗传性心律失常的单剂量基因疗法提供了可能,而且也可能为治疗更为常见的心律失常(比如心房颤动)的单剂量基因疗法提供了可能,相关研究结果近期发表在Circulation期刊上。
研究者Vassilios Bezzerides博士说道,“我们希望能够提供长期发挥作用的单剂量基因疗法。我们的研究为开发治疗遗传性心律失常的可转化基因治疗策略提供了概念验证。这项研究着重关注儿茶酚胺能多形性室性心动过速(CPVT),这是儿童和年轻人猝死的主要原因。这种心律失常通常由运动或精神压力引发,并且在平均12岁时首次出现,通常是突然失去意识。
【5】Sci Trans Med:基因疗法—治疗视力的新手段
doi:10.1126/scitranslmed.aax2324
在最近一篇文章中,作者总结了最近治疗致盲疾病的治疗策略。基因替换或基因编辑策略可能潜在地逆转视力丧失的问题。在视网膜变性的早期阶段,当感光细胞(视杆细胞和视锥细胞)仍然完整时,早期干预是特别有希望的。第一个批准用于Leber先天性黑蒙(LCA)的基因疗法确认了双等位基因RPE65突变,为全球其他条件下30多个基因替代试验铺平了道路。
基因独立策略旨在用广谱的,针对视网膜营养不良的神经保护剂预防或减缓感光细胞的进行性退化。神经保护策略,特别是保存锥体的策略,是治疗正在进行感光细胞变性的疾病的最佳方法。干细胞疗法,光遗传学疗法和视网膜假体用于在视网膜变性的后期恢复视力。这些方法可以独立于因果突变而应用,并且有望在盲人患者中恢复低视力。用于替代退化细胞以恢复视力的干细胞疗法正在开发或临床评估中在广泛的视网膜退行性病症中。
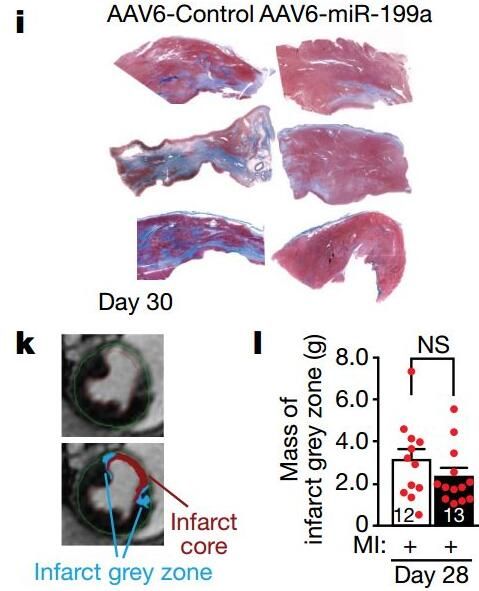
图片来源:Nature
doi:10.1038/s41586-019-1191-6
来自伦敦国王学院的研究人员发现,一种疗法可以诱导心脏病发作后的心脏细胞再生。世界卫生组织(who)的数据显示,心肌梗死是心力衰竭的主要原因,通常被称为心脏病发作,由心脏冠状动脉的突然阻塞引起,目前全球有2300多万人受到这种疾病的影响。
目前,当一个病人心脏病发作后幸存下来,他们的心脏会留下永久性的结构性损伤,形成疤痕,这可能导致未来的心力衰竭。与鱼类和蝾螈形成鲜明对比的是,蝾螈的心脏能在一生中再生;近日发表在Nature杂志上的这项研究中,研究团队将一小段名为microRNA-199的基因材料植入猪的心脏。这段基因可以在猪发生心肌梗死一个月后,促进其心功能几乎完全恢复。
doi:10.1073/pnas.1817537116
与迈阿密,哥伦比亚和旧金山的大学合作,来自巴斯德研究所,Inserm,CNRS,法兰西学院,索邦大学和Clermont Auvergne大学的科学家们成功恢复了DFNB9耳聋小鼠的听力,这是最常见的先天性遗传性耳聋病例之一。患有DFNB9耳聋的个体缺乏编码otoferlin的基因,而otoferlin是一种对于在听觉感觉细胞突触中传递声音信息必不可少的蛋白质。通过在成人DFNB9小鼠模型中进行该基因的耳蜗内注射,科学家们成功地将听觉突触功能和听力阈值恢复到接近正常水平。这些发现发表在PNAS期刊上,为DFNB9患者的未来基因治疗试验开辟了新的途径。
超过一半的非综合征性先天性耳聋患者有遗传原因,其中大多数(约80%)是由常染色体隐性遗传性耳聋(DFNB)引起的。人工耳蜗是目前恢复这些患者听力的唯一选择。DFNB9耳聋是由编码otoferlin的基因突变引起的,otoferlin是一种在内毛细胞突触传递声音信息中起关键作用的蛋白质。尽管没有可检测的感觉上皮缺陷,但是这些突触在响应声音刺激时不能释放神经递质,因此缺乏耳铁蛋白的突变小鼠是非常聋的。因此,DFNB9小鼠构成了用于在晚期施用时测试病毒基因治疗功效的合适模型。
doi:10.1093/brain/awy340
来自荷兰神经科学研究所(NIN)和莱顿大学医学中心(LUMC)的研究人员表明,使用基因疗法治疗可以在神经损伤后更快恢复。通过将手术修复程序与基因治疗相结合,首次刺激了神经细胞的存活和长距离神经纤维的再生。发表在《Brain》杂志上的这一发现是朝着为神经损伤患者开发新疗法迈出的重要一步。
在出生或交通事故发生后,颈部的神经可能会从脊髓中被撕裂。结果,这些患者失去了手臂功能,并且无法进行日常活动。目前,手术修复是患有这种神经损伤的患者唯一可用的治疗方法。 “手术后,神经纤维在到达肌肉和神经细胞之前必须桥接数厘米,新纤维需要再生的神经细胞大量丢失。大多数再生神经纤维不会到达肌肉。因此手臂功能的恢复令人失望,不完整,“作者说道。
【9】Cell Stem Cell:基因疗法可以用于治疗致命性自体免疫疾病
doi:10.1016/j.stem.2018.12.003
最近,加州大学洛杉矶分校研究人员创造了一种修复血液干细胞的基因突变的方法,以逆转导致威胁生命的自身免疫综合症(称为IPEX)的发生。这项工作在发表在最近的Cell Stem Cell杂志上。
IPEX是由一种突变引起的自身免疫疾病。该突变阻止了一种名为FoxP3的基因的表达,从而导致产生血液干细胞分化形成调节性T细胞的功能受到了阻碍。调节性T细胞可以负向控制身体的免疫系统的活性。缺少这一类细胞的话,免疫系统会攻击身体自身的组织和器官,最终导致自身免疫疾病的发生。
doi:10.1126/sciadv.aau6762
基因疗法在医学研究领域有着非常大的潜力,如果我们能够安全地改变自身的DNA,或许就能消除祖先遗传给我们的疾病。近日,一项刊登在国际杂志Science Advances上的研究报告中,来自特拉华大学的科学家们通过对微粒子进行工程化改造,使其能够运输基因调节物质进入造血干祖细胞(hematopoietic stem and progenitor cells),最终在基因疗法领域取得了新的研究突破。
造血干祖细胞位于骨髓中,其能指挥血细胞的形成,文章中,研究人员描述了如何利用巨核细胞微粒来运输质粒DNA和小型RNAs进入到造血干细胞中,这种巨核细胞微粒能在血液中天然循环。研究人员所开发的新技术能用于治疗影响成千上万美国人的遗传性血液障碍,比如镰状细胞性贫血和地中海贫血,前者是一种影响红细胞形状的疾病,而后者则是一种干扰血红蛋白产生的疾病。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


