淋巴瘤新药!新一代口服PI3Kδ/CK1-ε双重抑制剂Ukoniq获美国FDA批准!
来源:本站原创 2021-02-10 00:53
Ukoniq是第一款也是唯一一款口服、每日一次PI3Kδ/CK1-ε抑制剂。

2021年02月09日讯 /生物谷BIOON/ --TG Therapeutics是一家致力于为B细胞介导的疾病患者开发创新疗法的生物制药公司。近日,该公司宣布,美国食品和药物管理局(FDA)已加速批准Ukoniq(umbralisib,200mg片剂),用于治疗:(1)已接受过至少一种基于抗CD20方案的复发或难治性边缘区淋巴瘤(MZL)患者;(2)已接受过至少3种系统疗法的复发或难治性滤泡性淋巴瘤(FL)成人患者。用药方面,Ukoniq推荐剂量为800mg(4片),每日口服一次,与食物同服。
值得一提的是,Ukoniq是获批治疗复发/难治性MZL和FL的第一个也是唯一一个口服、每日一次、磷酸肌醇-3-激酶δ(PI3K-δ)和酪蛋白激酶1-ε(CK1-ε)双重抑制剂。根据2期UNITY-NHL试验(NCT02793583)的总缓解率(ORR)数据,Ukoniq获得了加速批准。针对这些适应症的继续批准,将取决于验证性试验中对临床益处的验证和描述。2个适应症中,MZL适应症被授予了优先审查。此外,Ukoniq之前还被授予了治疗MZL的突破性药物资格(BTD)、治疗MZL和FL的孤儿药资格(ODD)。
TG Therapeutics公司执行主席兼首席执行官MichaelS.Weiss表示:“今天Ukoniq的批准,标志着我们公司的历史性一天,这是我们收获的第一项批准,我们非常高兴能够将新型PI3K-δ和CK1-ε抑制剂带给复发/难治性MZL和FL患者。”
UNITY-NHL研究MZL&FL队列的研究主席、德克萨斯大学MD安德森癌症中心的医学教授Nathan Fowler博士表示:“尽管治疗取得进展,MZL和FL仍然是不可治愈的疾病,对先前治疗后复发的患者的治疗选择有限,而且没有明确的护理标准。随着umbralisib的批准,我们现在有了一个有针对性的、口服的、每天一次的选择,为患者提供了一个新的治疗选择,也为对抗这些疾病带来了新的希望。”

此次批准,基于UNITY-NHL 2b期试验中2个单臂队列的数据。UNITY-NHL是一项多中心、开放标签2b期研究,2个队列分别评估了Ukoniq作为单药疗法治疗69例复发/难治性MZL患者(先前接受过至少一种疗法,包括一种抗CD20方案)、117例复发/难治性FL患者(先前接受过至少2种系统疗法,包括一种抗CD20单抗和烷基化剂)的疗效。每个队列均达到其总缓解率(ORR)主要终点,达到了独立审查委员会(IRC)确认的40-50%的公司目标指导。
MZL队列数据显示:ORR为49%,其中完全缓解率(CR)为16%、部分缓解率(PR)为33%,中位缓解持续时间(DOR)尚未达到。FL队列数据显示:ORR为43%,其中CR为3.4%、PR为39%,中位DOR为11.1个月。研究中,Ukoniq的耐受性和安全性良好。
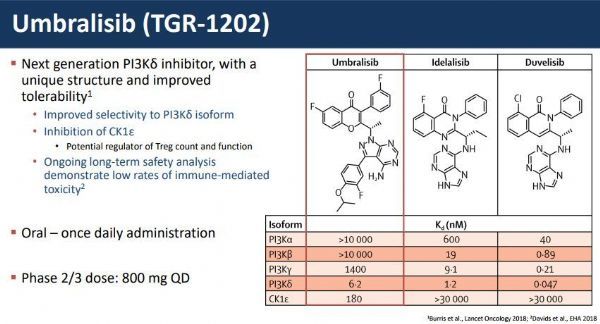
Ukoniq的活性药物成分为umbralisib,这是一种口服、每日一次的PI3Kδ和CK1-ε双效抑制剂,这可能使其克服第一代PI3Kδ抑制剂相关的某些耐受性问题。磷脂酰肌醇-3激酶(PI3K)是一类参与细胞增殖和存活、细胞分化、细胞内运输和免疫等多种细胞功能的酶。PI3K有四种亚型(α、β、δ和γ),其中δ亚型在造血来源的细胞中强烈表达,常与B细胞相关淋巴瘤有关。
umbrasib对PI3K的δ亚型具有纳米摩尔效力,并且对α、β、γ亚型具有高选择性。umbralisib还独特地抑制酪蛋白激酶1-ε(CK1-ε),这可能具有直接的抗癌作用,也可能调节先前PI3K抑制剂中观察到的与免疫介导不良事件相关的T细胞活性。
当前已批准的PI3Kδ抑制剂与自身免疫介导的毒性有关,如肝毒性、肺毒性和结肠炎。与已批准的PI3K抑制剂相比,umbralisib的特异性差异、其对CK1-ε的独特抑制作用以及其独特和专利的化学结构可能会在PI3K抑制剂类中具有差异化特征。
umbralisib已在血液系统恶性肿瘤的临床前模型和临床研究中证明了其活性。目前,在CLL和NHL患者中开展的IIb期和III期试验正在继续评估umbralisib的治疗潜力。
除了umbralisib之外,TG公司也正在开发一款单抗药物ublituximab(TG-1101),这是一种糖工程化嵌合IgG1单克隆抗体,靶向CD20,目前处于III期临床开发,评估治疗癌症(慢性淋巴细胞白血病[CLL]、非霍奇金淋巴瘤[NHL])和非癌症(多发性骨髓瘤[MM])适应症。
此外,TG公司还有多款资产进入了I期临床,包括PD-L1单抗TG-1501、共价结合布鲁顿酪氨酸激酶(BTK)抑制剂TG-1701等。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->