银屑病关节炎(PsA)新药!艾伯维口服JAK1抑制剂Rinvoq新适应症审查遭美国FDA推迟3个月!
来源:本站原创 2021-03-18 22:41
JAK1是一种激酶,在多种炎症性疾病的病理生理过程中发挥了关键作用。

2021年03月18日讯 /生物谷BIOON/ --艾伯维(AbbVie)近日宣布,美国食品和药物管理局(FDA)已延长了口服抗炎药Rinvoq(upadacitinib,15mg,每日一次)治疗活动性银屑病关节炎(PsA)成人患者补充新药申请(sNDA)的审查期。最新的《处方药用户收费法》(PDUFA)目标行动日期已延长3个月,至2021年第二季度末。Rinvoq是一种口服、选择性、可逆性JAK抑制剂,在美国已被批准用于治疗类风湿性关节炎(RA)。
在公告中,艾伯维表示,公司最近收到了美国FDA关于更新Rinvoq治疗银屑病关节炎的受益风险评估的信息请求。艾伯维已回应了这一请求,FDA将需要额外的时间对提交的文件进行全面审查。另外,艾伯维还收到了美国FDA的一份类似请求,涉及Rinvoq治疗特应性皮炎的sNDA。目前,回复文件正在准备中,不久将提交FDA。
艾伯维副主席兼总裁Michael Severino医学博士表示:“我们仍然对这项sNDA充满信心,并致力于与FDA合作,为患有银屑病关节炎和其他免疫介导性疾病的患者提供Rinvoq。”
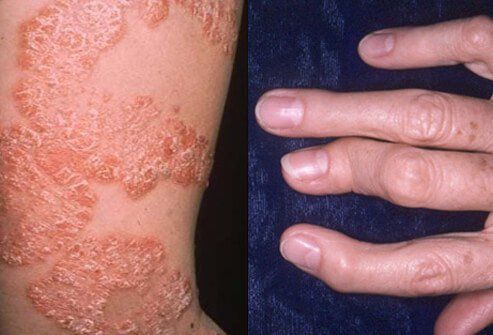
银屑病关节炎(图片来源:onhealth.com)
银屑病关节炎(PsA)是一种复杂的异质性疾病,表现跨越多个领域,包括关节和皮肤,导致日常疼痛、疲劳和僵硬。2020年6月,艾伯维同时向美国FDA和欧盟EMA提交了Rinvoq治疗PsA的新适应症申请。
今年1月,Rinvoq在欧盟获批2个新的风湿适应症:(1)用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的活动性PsA成人患者;(2)用于治疗对常规疗法应答不足的活动性强直性脊柱炎(AS)成人患者。
随着这项最新批准,Rinvoq成为了欧盟批准的第一个可用于治疗3种风湿适应症(RA、PsA、AS)的口服、每日一次、选择性、可逆性JAK抑制剂。在治疗这3种风湿适应症中,Rinvoq的批准剂量为15mg。
Rinvoq治疗PsA的新适应症,基于2项III期临床研究SELECT-PsA-1(NCT03104400)和SELECT-PsA-2(NCT03104374)的数据支持。这2项研究入组了超过2000例活动性PsA患者,结果显示,在2项研究中,与安慰剂相比,Rinvoq均达到了ACR20应答的主要终点。此外,15mg剂量Rinvoq与阿达木单抗在治疗第12周ACR20应答方面显示出非劣效性。接受Rinvoq治疗的患者在身体功能(HAQ-DI)和皮肤症状(PASI 75)方面也有更大的改善,并且有更大比例的患者达到了最低疾病活动度。

Rinvoq的活性药物成分为upadacitinib,这是由艾伯维发现和开发的一种口服选择性和可逆的JAK1抑制剂,正被开发治疗数种免疫介导的炎症性疾病。JAK1是一种激酶,在多种炎症性疾病的病理生理过程中发挥了关键作用。
Rinvoq于2019年8月在美国获得全球首个监管批准,用于治疗对甲氨蝶呤(MTX)应答不足或不耐受的中度至重度活动性类风湿性关节炎(RA)成人患者。在欧盟,Rinvoq于2019年12月获批上市,目前已批准的适应症包括:(1)用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的中度至重度RA成人患者;(2)用于治疗对一种或多种DMARD应答不足或不耐受的活动性PsA成人患者;(2)用于治疗对常规疗法应答不足的活动性强直性脊柱炎(AS)成人患者。
目前,Rinvoq治疗溃疡性结肠炎(UC)、类风湿性关节炎(RA)、银屑病关节炎(PsA)、中轴型脊柱关节炎(axSpA)、克罗恩病(CD)、特应性皮炎(AD)、巨细胞动脉炎(GCA)的III期临床研究正在进行中。
业界对Rinvoq的商业前景非常看好。瑞银集团分析师此前预测,Rinvoq与艾伯维的另一款单抗抗炎药Skyrizi,销售峰值将达到110亿美元。这2款新产品,将能够弥补艾伯维旗舰产品Humira(修美乐,阿达木单抗)遭遇生物仿制药冲击带来的销售损失。
Humira是全球第一个获批的抗肿瘤坏死因子α(TNF-α)药物,也是全球最畅销的抗炎药,2020年的全球销售额接近200亿美元(198.32亿美元)。在欧盟,已有多款阿达木单抗生物仿制药上市销售。而在美国市场,Humira将在2023年受到生物仿制药冲击。(生物谷Bioon.com)
原文出处:AbbVie Announces Extension of Review for Supplemental New Drug application of Upadacitinib for the Treatment of Adults with Active Psoriatic Arthritis
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


