早期肺癌新辅助(术前)免疫治疗方案!百时美施贵宝Opdivo+化疗方案获美国FDA批准!
来源:本站原创 2022-03-21 01:45
Opdivo+化疗是第一个针对可切除NSCLC患者的新辅助免疫治疗方案。
2022年03月20日讯 /生物谷BIOON/ --百时美施贵宝(BMS)近日宣布,美国食品和药物管理局(FDA)已批准抗PD-1疗法Opdivo(欧狄沃,通用名:nivolumab,纳武利尤单抗)360mg(静脉制剂)联合含铂双药化疗,每3周给药一次共3个周期,用于新辅助(术前)治疗可切除性(肿瘤≥4厘米或淋巴结阳性)非小细胞肺癌(NSCLC)成人患者,不论PD-L1状态如何。
值得一提的是,Opdivo+化疗标志着用于NSCLC术前治疗的第一种也是唯一一种基于免疫疗法的治疗方案。此前,基于Opdivo的免疫治疗组合方案已被批准用于治疗转移性和早期NSCLC。
此次批准基于关键3期CheckMate-816试验(NCT02998528)的结果,这是免疫疗法在新辅助治疗NSCLC中获得阳性结果的第一项3期试验。数据显示,在可切除IB-IIIA期NSCLC患者中,与化疗相比,Opdivo+化疗显著改善了无事件生存期(EFS)和病理学完全缓解率(pCR)。
CheckMate-816是一项随机、开放标签、多中心试验,在可切除性IB-IIIA期NSCLC患者中开展,不论PD-L1表达状态如何。试验中,患者被随机分配,接受Opdivo+化疗方案(每3周一次,共3次)、化疗(每3周一次,共3次)新辅助(术前)治疗,随后进行手术。该试验的主要终点是病理学完全缓解(pCR)和无事件生存期(EFS)。pCR定义为:根据盲法独立病理学审查评估,切除组织中没有癌细胞存在的证据。EFS定义为:疾病无进展或复发的生存时间。
结果显示,用于新辅助(术前)治疗时,与化疗组相比,Opdivo+化疗组EFS实现统计学意义和临床意义的改善,疾病进展、复发或死亡风险显著降低37%(HR=0.63;95%CI:0.45-0.87;p=0.0052)。Opdivo+化疗组的中位EFS为31.6个月,化疗组为20.8个月。
此外,与化疗组相比,Opdivo+化疗组pCR显著提高。术前接受Opdivo+化疗治疗的患者中有24%实现了pCR,而化疗组比例仅为2.2%(估计治疗差异21.6;95%CI:15.1-28.2;p<0.0001)。此外,Opdivo+化疗方案的耐受性良好,无论PD-L1表达水平、组织学或疾病分期如何,pCR均表现出一致的改善。对总生存期(OS)进行的预先指定中期分析显示,HR为0.57(95%CI:0.38-0.87),无统计学意义。
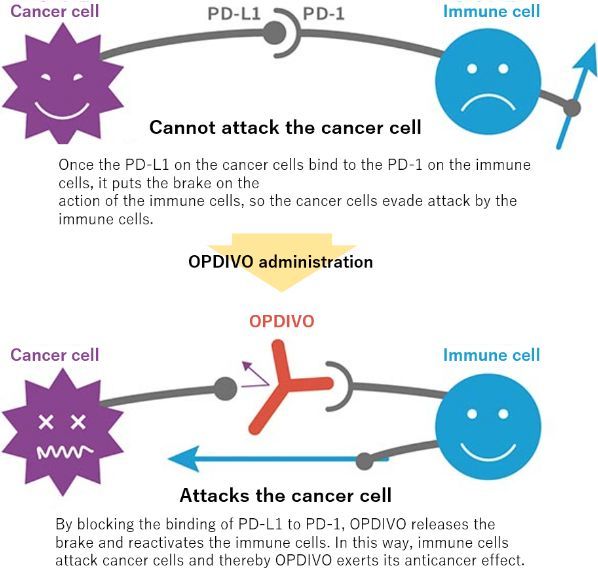
Opdivo作用机制(图片来源:ono-pharma.com)
肺癌是全球癌症死亡的首要原因。肺癌的2种主要类型是非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)。NSCLC是最常见的肺癌类型,占肺癌诊断的84%。非转移性病例占NSCLC诊断的大多数(约60%)。尽管许多非转移性NSCLC患者通过手术治愈,但仍有30%-55%的患者在手术切除后复发并死于疾病,因此需要在手术前(新辅助)和/或手术后(辅助)给予治疗方案以改善长期预后。
目前,在早期阶段的NSCLC中,百时美施贵宝及其合作者正在探索免疫疗法在新辅助治疗、辅助治疗、围手术期治疗中的应用,以及与放化疗联合应用。在新辅助治疗环境中使用免疫治疗的科学依据有2个方面:(1)它提供了最早的机会来治疗在未被发现的情况下在体内扩散的癌细胞(隐蔽性转移);(2)在免疫治疗期间肿瘤的存在可能产生更强的免疫反应,可能使治疗对原发性肿瘤更有效。
Opdivo属于PD-(L)1肿瘤免疫疗法,旨在利用人体自身的免疫系统抵御癌症,通过阻断PD-1/PD-L1信号通路使癌细胞死亡,具有治疗多种类型肿瘤的潜力。截止目前,Opdivo已在全球范围内获批多种癌症适应症。
在中国,Opdivo(欧狄沃)于2018年6月获批上市,成为中国市场首个获批的免疫肿瘤(I-O)治疗药物,目前已获批多个适应症,详见《Opdivo(纳武利尤单抗注射液说明书)》。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


