Cell:开发出高灵敏检测疾病相关突变的SNIPR技术
来源:本站原创 2020-03-10 12:47
2020年3月10日讯/生物谷BIOON/---出现在小说草稿中的错别字不是什么大灾难。但是,自然通常很少容忍错误。遗传密码中仅一个碱基的更改可能会对人类健康造成灾难性的后果。这种涉及DNA或RNA中单个碱基的基因组变化称为点突变。它们可导致轻微的异常,比如色盲,但也可导致严重的疾病,包括神经纤维瘤病、镰状细胞贫血、某些癌症和泰伊-萨克斯二氏病(Tay-Sa
2020年3月10日讯/生物谷BIOON/---出现在小说草稿中的错别字不是什么大灾难。但是,自然通常很少容忍错误。遗传密码中仅一个碱基的更改可能会对人类健康造成灾难性的后果。这种涉及DNA或RNA中单个碱基的基因组变化称为点突变。它们可导致轻微的异常,比如色盲,但也可导致严重的疾病,包括神经纤维瘤病、镰状细胞贫血、某些癌症和泰伊-萨克斯二氏病(Tay-Sachs disease)。突变也能产生对常规治疗有抵抗力的疾病变体。
科学家们希望检测这些点突变,以更好地评估人类健康中的脆弱性,提供准确的早期诊断并指导适当的治疗。但是,到目前为止,在活细胞内记录诸如点突变之类的细微变化一直具有挑战性。
在一项新研究中,来自美国亚利桑那州立大学等研究机构的研究人员描述了一种检测点突变的新方法。它可以应用于活细胞中,从而提供了一种快速、高度准确和廉价的方法来鉴定与人类健康有关的突变。相关研究结果发表在2020年3月5日的Cell期刊上,论文标题为“Precise and Programmable Detection of Mutations Using Ultraspecific Riboregulators”。论文通讯作者为亚利桑那州立大学的Alexander A. Green博士和Hao Yan博士。
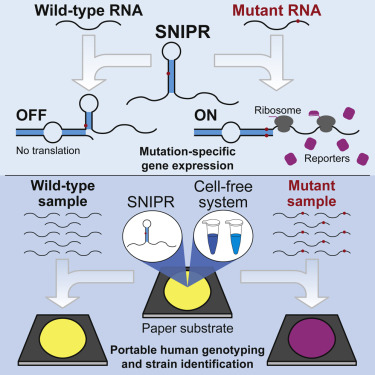
这种方法可与基于试纸的诊断测试(由Green及其同事们开发)结合使用,能够在人体热量驱动的反应中查明突变并显示基于颜色的读数。
Green说,“我们使用我们的技术完成的工作是开发一种新的可移植的方法来检测你想要检测的RNA之间的微小序列差异。有了这种我们称为SNIPR(Single-Nucleotide-Specific Programmable Riboregulator)的系统,我们就有能力根据单个核苷酸差异识别任何RNA序列。”
这种技术非常灵敏,甚至可以检测到表观遗传变化,即对遗传序列的细微化学修饰,可以调节基因表达而无需改变单个碱基的身份。
Yan表示,“这种方法取得的进展有朝一日可能能够用作个人基因分型的低成本替代技术。这种技术的简单性可能允许在家筛查与疾病有关的突变,从而提供快速而准确的测试,同时为用户保持数据隐私。”
除了利用一种廉价、多用途的石蕊试验用于检测突变相关疾病的便利性之外,这种技术还有望为细胞生物学的基础问题---对抗生素的基因耐药性和导致针对疟疾和艾滋病等疾病的一线治疗失败的突变---提供新的思路。
遗传密码中的碱基
在人类中,遗传密码由排列在标志性的DNA双螺旋结构中的大约30亿对核苷酸(即碱基)组成。遗传密码仅由4个碱基组成,这4个碱基可用字母A、T、C和G表示。
这4个碱基按照一定的次序排列在一起可形成基因,所形成的基因为蛋白的产生提供了指令。蛋白为细胞和包括肌肉、软骨、韧带、头发和皮肤在内的组织提供结构。蛋白还提供生命的重要机制,监督无数的细胞过程,包括代谢、信号传递、免疫防御、食物消化和细胞分裂。
捕捉突变
发生点突变的DNA基因将被转录为RNA,这有时会破坏所产生的蛋白或改变它的功能,这通常会危害人体健康。为了识别这些突变,这些研究人员设计出SNIPR---包含能够与细胞中RNA序列结合的互补RNA片段的巧妙结构。在细胞内,这种结构在遇到突变的RNA序列(由细胞的修饰基因决定)时会激活。
如果细胞的突变RNA与触发链(trigger strand,即互补RNA片段)的结合正确,则SNIPR会展开,从而允许核糖体(将RNA转化为蛋白所需的复合物)进行序列访问。但是,如果SNIPR遇到未突变的序列,则说明存在错配,蛋白翻译受阻。
校对RNA
在细菌大肠杆菌中观察到了突变的和未突变的RNA序列之间基因表达的100倍差异(以蛋白产生为准),这使得检测点突变变得容易。
这种技术依赖于敏锐地检测所谓的结合能(binding energy)或者说杂交能(hybridization energy)的差异。Green说:“通常,当你考虑DNA或RNA碱基配对时,它是通过氢键进行的。碱基G与C的结合需要三个氢键,而A与U的结合需要两个氢键。”除了点突变外,当发生表观遗传变化(如甲基化)时,体外分析还可以检测结合能的微小差异。
这种基于试纸的测试可以在医疗资源匮乏的地区进行现场使用。该技术对发展中国家特别有希望,这是因为它不需要复杂的设备,并且可以在人体温度下运行。
论文第一作者Fan Hong设计了计算机算法,该算法允许根据所需的RNA靶序列有效设计SNIPR。
Hong说,“为了让SNIPR易于使用,我们使得这一过程自动化,以便每个人都可以在不了解RNA折叠和RNA相互作用的情况下进行设计。他们已经显示出许多实际应用,比如人类基因分型、寨卡病毒检测和病毒毒株鉴定。”
强大的技术为科学带来福音
在流行病学上,鉴定特定菌株或毒株至关重要。比如,寨卡病毒的某些遗传变体似乎增加出生畸形的风险,而当前正在传播的新型冠状病毒也在进化,并且它的序列与导致2002-2003年严重急性呼吸综合征(SARS)疫情的冠状病毒(SARS-CoV)非常相似。鉴定这些突变病原体的影响及其地理分布对于应对这些疫情以及未来的疾病暴发至关重要。
这种方法还可以为抗击癌症提供新的希望。比如,与一种罕见的侵袭性卵巢癌有关的颗粒细胞瘤(granulosa cell tumor)是由构成人类遗传密码的30亿个核苷酸对中的一个错误碱基导致的,而肿瘤抑制基因BRCA1和BRCA2中的点突变导致乳腺癌的终生风险增加了6倍。
SNIPR的精细敏感性可以区分对于给定突变是杂合的还是纯合的患者,也就是说,他们的染色体携带一或两个突变基因的拷贝,这是确定疾病易感性的关键因素。
HIV中的某些点突变可能导致常见的抗逆转录病毒疗法失败。针对此类突变的SNIPR测试可能能够快速识别这些突变并指导适当的治疗。对于许多有需要的人来说,常规的HIV耐药性测试价格过高,每个样本的测试成本超过200美元。
当SNIPR探针与基于试纸的识别系统结合使用时,快速、低成本和精确检测基因点突变的潜力就可以在全球最需要此类诊断工具的任何地方进行拓展。此外,SNIPR有望帮助科学家们了解菌株或毒株变异和与突变相关的对常见药物的耐药性。(生物谷 Bioon.com)
参考资料:
1.Fan Hong et al. Precise and Programmable Detection of Mutations Using Ultraspecific Riboregulators. Cell, 2020, doi:10.1016/j.cell.2020.02.011.
2.SNIPRs take aim at disease-related mutations
https://phys.org/news/2020-02-sniprs-aim-disease-related-mutations.html
科学家们希望检测这些点突变,以更好地评估人类健康中的脆弱性,提供准确的早期诊断并指导适当的治疗。但是,到目前为止,在活细胞内记录诸如点突变之类的细微变化一直具有挑战性。
在一项新研究中,来自美国亚利桑那州立大学等研究机构的研究人员描述了一种检测点突变的新方法。它可以应用于活细胞中,从而提供了一种快速、高度准确和廉价的方法来鉴定与人类健康有关的突变。相关研究结果发表在2020年3月5日的Cell期刊上,论文标题为“Precise and Programmable Detection of Mutations Using Ultraspecific Riboregulators”。论文通讯作者为亚利桑那州立大学的Alexander A. Green博士和Hao Yan博士。

图片来自Cell, 2020, doi:10.1016/j.cell.2020.02.011。
这种方法可与基于试纸的诊断测试(由Green及其同事们开发)结合使用,能够在人体热量驱动的反应中查明突变并显示基于颜色的读数。
Green说,“我们使用我们的技术完成的工作是开发一种新的可移植的方法来检测你想要检测的RNA之间的微小序列差异。有了这种我们称为SNIPR(Single-Nucleotide-Specific Programmable Riboregulator)的系统,我们就有能力根据单个核苷酸差异识别任何RNA序列。”
这种技术非常灵敏,甚至可以检测到表观遗传变化,即对遗传序列的细微化学修饰,可以调节基因表达而无需改变单个碱基的身份。
Yan表示,“这种方法取得的进展有朝一日可能能够用作个人基因分型的低成本替代技术。这种技术的简单性可能允许在家筛查与疾病有关的突变,从而提供快速而准确的测试,同时为用户保持数据隐私。”
除了利用一种廉价、多用途的石蕊试验用于检测突变相关疾病的便利性之外,这种技术还有望为细胞生物学的基础问题---对抗生素的基因耐药性和导致针对疟疾和艾滋病等疾病的一线治疗失败的突变---提供新的思路。
遗传密码中的碱基
在人类中,遗传密码由排列在标志性的DNA双螺旋结构中的大约30亿对核苷酸(即碱基)组成。遗传密码仅由4个碱基组成,这4个碱基可用字母A、T、C和G表示。
这4个碱基按照一定的次序排列在一起可形成基因,所形成的基因为蛋白的产生提供了指令。蛋白为细胞和包括肌肉、软骨、韧带、头发和皮肤在内的组织提供结构。蛋白还提供生命的重要机制,监督无数的细胞过程,包括代谢、信号传递、免疫防御、食物消化和细胞分裂。
捕捉突变
发生点突变的DNA基因将被转录为RNA,这有时会破坏所产生的蛋白或改变它的功能,这通常会危害人体健康。为了识别这些突变,这些研究人员设计出SNIPR---包含能够与细胞中RNA序列结合的互补RNA片段的巧妙结构。在细胞内,这种结构在遇到突变的RNA序列(由细胞的修饰基因决定)时会激活。
如果细胞的突变RNA与触发链(trigger strand,即互补RNA片段)的结合正确,则SNIPR会展开,从而允许核糖体(将RNA转化为蛋白所需的复合物)进行序列访问。但是,如果SNIPR遇到未突变的序列,则说明存在错配,蛋白翻译受阻。
校对RNA
在细菌大肠杆菌中观察到了突变的和未突变的RNA序列之间基因表达的100倍差异(以蛋白产生为准),这使得检测点突变变得容易。
这种技术依赖于敏锐地检测所谓的结合能(binding energy)或者说杂交能(hybridization energy)的差异。Green说:“通常,当你考虑DNA或RNA碱基配对时,它是通过氢键进行的。碱基G与C的结合需要三个氢键,而A与U的结合需要两个氢键。”除了点突变外,当发生表观遗传变化(如甲基化)时,体外分析还可以检测结合能的微小差异。
这种基于试纸的测试可以在医疗资源匮乏的地区进行现场使用。该技术对发展中国家特别有希望,这是因为它不需要复杂的设备,并且可以在人体温度下运行。
论文第一作者Fan Hong设计了计算机算法,该算法允许根据所需的RNA靶序列有效设计SNIPR。
Hong说,“为了让SNIPR易于使用,我们使得这一过程自动化,以便每个人都可以在不了解RNA折叠和RNA相互作用的情况下进行设计。他们已经显示出许多实际应用,比如人类基因分型、寨卡病毒检测和病毒毒株鉴定。”
强大的技术为科学带来福音
在流行病学上,鉴定特定菌株或毒株至关重要。比如,寨卡病毒的某些遗传变体似乎增加出生畸形的风险,而当前正在传播的新型冠状病毒也在进化,并且它的序列与导致2002-2003年严重急性呼吸综合征(SARS)疫情的冠状病毒(SARS-CoV)非常相似。鉴定这些突变病原体的影响及其地理分布对于应对这些疫情以及未来的疾病暴发至关重要。
这种方法还可以为抗击癌症提供新的希望。比如,与一种罕见的侵袭性卵巢癌有关的颗粒细胞瘤(granulosa cell tumor)是由构成人类遗传密码的30亿个核苷酸对中的一个错误碱基导致的,而肿瘤抑制基因BRCA1和BRCA2中的点突变导致乳腺癌的终生风险增加了6倍。
SNIPR的精细敏感性可以区分对于给定突变是杂合的还是纯合的患者,也就是说,他们的染色体携带一或两个突变基因的拷贝,这是确定疾病易感性的关键因素。
HIV中的某些点突变可能导致常见的抗逆转录病毒疗法失败。针对此类突变的SNIPR测试可能能够快速识别这些突变并指导适当的治疗。对于许多有需要的人来说,常规的HIV耐药性测试价格过高,每个样本的测试成本超过200美元。
当SNIPR探针与基于试纸的识别系统结合使用时,快速、低成本和精确检测基因点突变的潜力就可以在全球最需要此类诊断工具的任何地方进行拓展。此外,SNIPR有望帮助科学家们了解菌株或毒株变异和与突变相关的对常见药物的耐药性。(生物谷 Bioon.com)
参考资料:
1.Fan Hong et al. Precise and Programmable Detection of Mutations Using Ultraspecific Riboregulators. Cell, 2020, doi:10.1016/j.cell.2020.02.011.
2.SNIPRs take aim at disease-related mutations
https://phys.org/news/2020-02-sniprs-aim-disease-related-mutations.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


