治疗斑秃的JAK抑制剂!礼来/Incyte Olumiant第二个3期试验成功:显著促进头发再生!
来源:本站原创 2021-04-21 02:52
Olumiant有潜力成为第一款治疗斑秃疾病的药物。

2021年04月20日讯 /生物谷BIOON/ --礼来(Eli Lilly)与合作伙伴Incyte近日公布了评估口服JAK抑制剂Olumiant(baricitinib)治疗成人重度斑秃(alopecia areata,AA)第二项3期研究BRAVE-AA1的阳性顶线结果。该研究评估了2种剂量Olumiant(2mg,4mg,每日一次)的疗效和安全性。这些数据与今年早些时候公布的首个3期研究BRAVE-AA2的结果一致。数据显示,治疗第36周,2项研究均达到了主要疗效终点:与接受安慰剂的患者相比,接受2种剂量Olumiant治疗的患者头皮毛发再生有统计学意义的显著改善。
Olumiant的活性药物成分为baricitinib,这是由Incyte发现的一种口服JAK1/JAK2抑制剂,由礼来根据Incyte的许可开发。2020年11月,Olumiant获得欧盟批准第二个适应症,用于治疗适合系统疗法的中度至重度AD成人患者。值得一提的是,Olumiant是全球第一个被批准治疗特应性皮炎(AD)的JAK抑制剂。
斑秃(AA)是一种毁灭性的自身免疫性疾病,可导致头皮、面部、有时身体其他部位出现片状脱发,还会对患者产生重大的心里影响。目前,尚无获美国FDA批准的治疗AA的药物。此前,美国FDA已授予baricitinib治疗AA的突破性药物资格(BTD)。
BRAVE-AA项目的数据,将支持Olumiant治疗重度AA的监管申请提交。如果获得批准,Olumiant有潜力成为第一个治疗斑秃的药物,而AA也将成为继特应性皮炎(AD)之后Olumiant在皮肤病学领域的第2个治疗适应症。
BRAVE-AA1研究的调查员、哈佛医学院皮肤病学助理教授Maryanne Senna医学博士表示:“由于现有的局部用药和类固醇不能为许多患者提供有意义的改善,因此对获得监管批准的有效斑秃治疗方案存在着迫切需求。我很高兴从这些重要的baricitinib试验中看到如此积极的结果,该药将为这种疾病提供一种急需的潜在突破性治疗选择。”
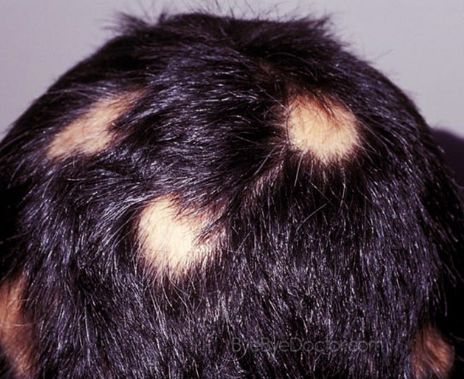
斑秃(图片来源:byebyedoctor.com)
BRAVE-AA试验项目旨在评估baricitinib治疗重度AA成人患者的疗效和安全性。该项目包括2个试验:BRAVE-AA1和BRAVE-AA2。BRAVE-AA1是一项多中心、随机、双盲、安慰剂对照的适应性2/3期试验。根据第12周时BRAVE-AA1 2期部分的中期结果,在该研究的3期部分选择每日一次2mg和4mg剂量baricitinib进行进一步评估。BRAVE-AA2是一项多中心、随机、双盲、安慰剂对照研究,评估了baricitinib 2mg和4mg剂量方案与安慰剂的疗效和安全性。这2项研究均入组了患有严重斑秃的成人患者,严重斑秃定义为严重脱发工具(SALT)评分≥50(即头皮脱发≥50%)且目前严重AA发作持续至少6个月但不超过8年。该项目包括来自多个国家的不同患者群体,包括中国。
在这2项研究中,在9个月的治疗期间,根据医生的评估,与安慰剂治疗的患者相比,接受2种剂量baricitinib治疗的患者头皮毛发再生有统计学意义的显著改善。BRAVE-AA1研究的结果显示,在第36周,达到80%或以上头皮毛发覆盖率的患者比例,baricitinib 4mg组为35%(p≤0.001)、2mg组为22%(p≤0.001)、安慰剂组为5%,达到了主要终结点。BRAVE-AA2研究的结果显示,在第36周时,达到80%或以上头皮毛发覆盖率的患者比例,baricitinib 4mg组为33%(p≤0.001)、2mg组为17%(p≤0.001)、安慰剂组为3%,达到了主要终点。在这2项研究中,到第36周,2mg组和4mg组自我报告头皮覆盖率至少为80%的患者比例显著高于安慰剂组(p≤0.001)。
BRAVE-AA1和BRAVE-AA2中最常见的治疗期间出现的不良事件(TEAE)包括上呼吸道感染、头痛和痤疮。试验中未报告死亡或静脉血栓栓塞事件(VTE)。这2项研究中baricitinib的安全性与已知的在类风湿关节炎(RA)和特应性皮炎(AD)患者中的安全性一致。
礼来将在今年晚些时候的科学会议上提供这些研究的详细数据,并将结果提交给同行评审的期刊。基于这些结果,礼来计划在2021年下半年向美国FDA提交baricitinib治疗重度AA的补充新药申请(sNDA),随后向全球其他监管机构提交申请。在2020年第1季度,美国授予了baricitinib治疗AA的突破性药物资格(BTD)。
礼来免疫学开发副总裁Lotus Mallbris医学博士表示:“baricitinib治疗斑秃3期临床试验项目的阳性结果,使我们距离为遭受这种严重自身免疫性疾病影响的患者提供一种经批准的治疗方案又近了一步。我们期待着与全球监管机构讨论来自BRAVE-AA临床项目的数据。baricitinib有潜力成为第一个治疗斑秃的治疗方法。”

Olumiant的活性药物成分为baricitinib,该药是一种每日口服一次的选择性、可逆性JAK1和JAK2抑制剂,目前处于临床开发,用于多种炎症性疾病和自身免疫性疾病的治疗,包括类风湿性关节炎(RA)、银屑病、糖尿病肾病、特应性皮炎、系统性红斑狼疮(SLE)等。JAK酶有4种,分别为JAK1、JAK2、JAK3和TYK2。JAK-依赖性细胞因子参与多种炎症和自身免疫性疾病的发病过程,提示JAK抑制剂或可广泛用于治疗各种炎症性疾病。在激酶检测试验中,baricitinib针对JAK1和JAK2表现出的抑制强度要比JAK3高出100倍。
baricitinib由Incyte发现并授权给礼来。在美国和70多个国家,baricitinib已被批准以商品名Olumiant上市销售,用于治疗中度至重度活动性类风湿性关节炎(RA)成人患者。在欧盟和日本,Olumiant还被批准用于治疗中度至重度特应性皮炎(AD)成人患者。
治疗RA方面,Olumiant在欧盟批准的剂量为4mg和2mg,在美国批准的剂量为2mg。用药方面,Olumiant每日口服一次,可作为单药或联合甲氨蝶呤(MTX)或其他非生物疾病修饰抗风湿疗法(non-biologic DMARDs)。不推荐将Olumiant与其他JAK抑制剂、或生物DMARD、强效免疫抑制剂(如硫唑嘌呤和环孢菌素)联合用药。值得注意的是,Olumiant的美国药物标签中附有一则黑框警告,提示严重感染、恶性肿瘤和血栓形成的风险。
目前,baricitinib也正在临床研究中被评估用于治疗系统性红斑狼疮(SLE)、幼年特发性关节炎(JIA)、新型冠状病毒肺炎(COVID-19)。(生物谷Bioon.com)
原文出处:Lilly and Incyte's Baricitinib Improved Hair Regrowth for Alopecia Areata Patients in Second Phase 3 Study
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


