一举两得!同时改善CAR-T安全性和有效性,GM-CSF中和策略或成趋势
来源:陈婉仪 医麦客 2019-05-27 17:18
5月16日,Humanigen公司宣布,Blood杂志上发表了一篇由Omar Ahmed博士撰写的题为“CAR-T Cell Neurotoxicity: Hope is on the Horizon(CAR-T细胞神经毒性: 希望就在眼前)”,重点阐述了当前缓解CAR-T诱导神经毒性(Neurotoxicity, NT)的未满足需求。这篇文章扩展了由哈佛医学院、耶鲁医学院和马萨诸塞州总医院癌症中
5月16日,Humanigen公司宣布,Blood杂志上发表了一篇由Omar Ahmed博士撰写的题为“CAR-T Cell Neurotoxicity: Hope is on the Horizon(CAR-T细胞神经毒性: 希望就在眼前)”,重点阐述了当前缓解CAR-T诱导神经毒性(Neurotoxicity, NT)的未满足需求。
这篇文章扩展了由哈佛医学院、耶鲁医学院和马萨诸塞州总医院癌症中心的研究人员领导的一项研究的结果,题为“Clinical presentation, management, and biomarkers of neurotoxicity after adoptive immunotherapy with CAR T cells(CAR-T细胞过继免疫疗法后神经毒性的临床表现、管理和生物标志物)”,该研究由Karschnia等人撰写,也刊登在本期Blood上。
毒副作用限制了CAR-T疗法的可及性
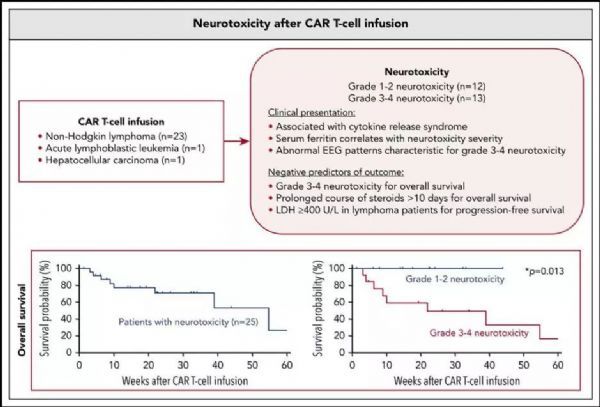
Karschnia等人一个关键发现是,严重的NT和长时间暴露于糖皮质激素(目前推荐的治疗),>10天是CAR-T治疗后总体生存的不利预后因素(分别为p=0.013和p=0.030),本研究中>50%的NT患者发生了严重的NT。
此外,NT与细胞因子释放综合征(CRS)有关,抗IL-6受体拮抗剂托珠单抗(tocilizumab, Actemra),是FDA目前唯一批准的严重CRS治疗方法。但研究表明,托珠单抗的预防性使用可提高NT的总体发生率和严重NT的发生率。
(图片来源:blood)
大多数患者作为住院病人接受CAR-T治疗,有时需要进入重症监护病房(ICU)来管理这些毒副作用,这给医院和机构造成额外的卫生经济负担和较不优惠的报销,这不可避免地导致准入受到限制。
因此,文中指出,在不影响疗效的前提下,需要制定提高CAR-T安全性的策略,以改善其获益-风险特征、成本效益,并使CAR-T不仅可以在复发/难治性患者中使用,还可以用于早期治疗。
GM-CSF中和:同时改善CAR-T的安全性和有效性
文章还重点介绍了CAR-T诱导NT和细胞因子释放综合征(CRS)的病理生理学,并确定了粒细胞-巨噬细胞集落刺激因子(GM-CSF)中和作为一种有可能同时改善CAR-T的安全性和有效性的策略,鉴于GM-CSF中和的双重作用机制。
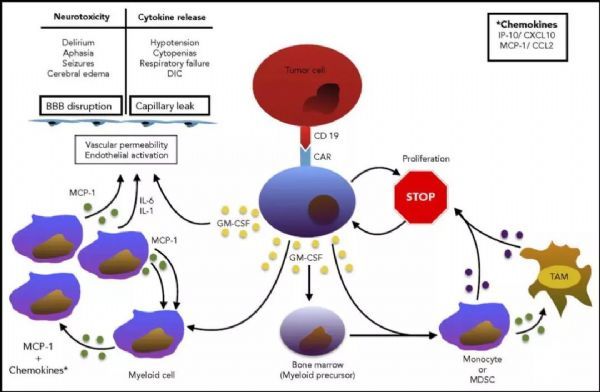
神经毒性和CRS的病理生理机制(图片来源:blood)
GM-CSF是CAR-T细胞在与肿瘤接触后产生的,其作为CAR-T细胞特异性免疫反应与髓系细胞(myeloid lineage cells)产生的靶外炎症级联之间的通信管道。
一方面,GM-CSF是导致NT和CRS的炎性细胞因子级联反应的关键上游触发因子。
GM-CSF直接作用于骨髓细胞(myeloid cells),扩大、激活和促进其他趋化因子和细胞因子的产生,包括MCP-1/CCL2、IP-10/CXCL10以及细胞因子IL-6和IL-1。
CAR-T细胞给药36小时后发热和MCP-1水平升高,已被证明是具有高水平特异性和敏感性的严重NT和CRS的最佳预测因子。此外,IL-6仅由抗原呈递细胞或肿瘤细胞以不依赖接触的方式释放,这有助于解释为什么预防性给予托珠单抗不能有效降低CRS或NT的总体发病率,因为这种细胞因子位于炎症级联的下游。
一旦启动,这种炎症级联可能成为一种自我延续的“风暴”,趋化因子的产生导致髓系细胞进一步增殖和向肿瘤病灶转运,正反馈回路可导致异常高水平的炎性细胞因子、内皮激活、血管通透性,最终导致CRS和NT。
另一方面,GM-CSF还直接作用于髓系细胞,促进髓系来源抑制细胞(MDSC)和肿瘤相关巨噬细胞(TAM)的增殖和运输,这些细胞已被证明能抑制T细胞增殖和效应功能。
因此,中和GM-CSF是一种可能打破正在开发中的新型下一代CAR-T构建体的功效/毒性联系的新方法。Humanigen的首席执行官Cameron Durrant博士说:“GM-CSF中和可能成为下一代策略,以潜在地提高CAR-T疗法的有效性、安全性和成本效益。”
其他NT发病影响因素
除了最显而易见的炎症级联反应,血脑屏障(BBB)破坏以及骨髓细胞和促炎细胞因子向中枢神经系统(CNS)的浸润是NT发病机制中的其他重要因素。
在Karschnia等人的研究中,在CAR-T细胞输注之前,低血小板计数(BBB破坏的生物标志物)与严重NT相关。可以通过磁共振成像(MRI)无创地监测BBB的完整性。含有钆的常规造影剂与MRI结合使用以检测和量化BBB泄漏。临床前体内研究显示,CAR-T细胞治疗后弥漫性神经炎症和BBB损伤,使得促炎性细胞因子大量涌入CNS,这被认为可传播神经炎症。这与CAR-T细胞临床试验中报道的数据一致,在发生严重NT的患者中观察到BBB的破坏和脑脊液中促炎细胞因子和CD14+骨髓细胞水平的显著增加,表明局部CNS特异性产生的可能性。
多项研究聚焦抑制GM-CSF
此前,多项研究已经揭示GM-CSF中和策略的双重作用。
Cellectis公司,专注于开发基于基因编辑的同种异体CAR-T细胞(UCART)免疫疗法,探索了一种旨在预防CRS而不是限制其后果的治疗途径。今年2月,在The Journal of Biological Chemistry上发表的一项研究发现,GM-CSF是一种关键的促细胞因子释放综合征(CRS)蛋白。
结合体外实验和基因编辑技术,研究者进一步证明抗体介导的中和或TALEN介导的CAR-T细胞中GM-CSF的基因失活大大减少可用的GM-CSF,并消除巨噬细胞依赖性分泌的CRS生物标志物,包括MCP-1、IL-6和IL-8。值得注意的是,该项研究还发现GM-CSF基因失活并不影响CAR-T细胞的体外抗肿瘤功能或增殖能力。
总之,通过使用“一体化”GM-CSF敲除CAR-T细胞可以预防CRS。该方法可以消除对抗CRS治疗的需要,并且可以改善癌症患者接受CAR-T细胞疗法的总体安全性。
对此Cellectis创新项目负责人Mohit Sachdeva博士表示:“我们的这一工程策略规避了CAR-T细胞治疗可能带来的副作用,制造了更安全而且同样有效的UCART,以改善患者在治疗期间的生活质量。”
Cellectis创新团队负责人Julien Valton博士补充道,“目前,托珠单抗或糖皮质激素治疗被认为是CRS的标准治疗方法。然而,这些治疗会增加患者的药物负担,同时增加费用并延长治疗时间。为了解决这些临床问题,我们研究了CRS发生的分子机制,并基于研究结果开发了可以预防而不是治疗CRS的CAR-T细胞候选产品。我们希望这种方法能够绕过CRS症状治疗,并提高癌症患者CAR-T细胞治疗的整体安全性。”
去年发表于Blood杂志上的一项研究,梅奥医学中心研究者及其合作者也有类似的思路:既然单核细胞和巨噬细胞导致CAR-T细胞治疗后CRS和神经毒性的发生发展,那么抑制GM-CSF是否能改善与CAR-T细胞治疗相关的毒性。
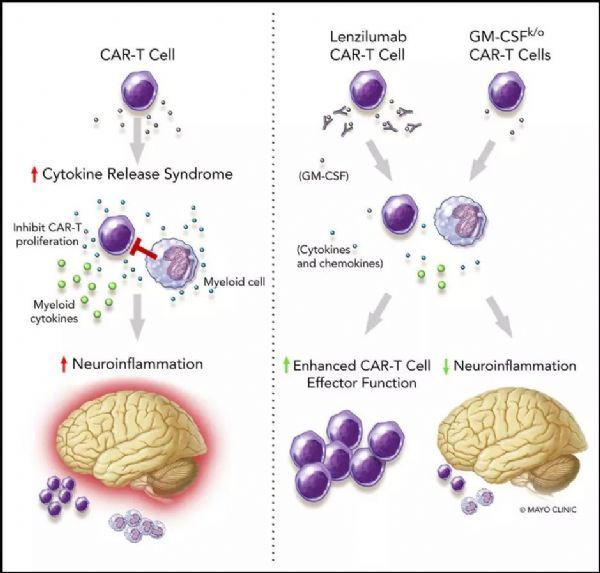
在体外和体内实验中,他们正是使用Humanigen公司的GM-CSF抑制剂Lenzilumab。小鼠研究中,接受患者来源的T细胞异种移植并使用lenzilumab,CAR-T19细胞增殖增强,而且白血病控制更持久。在CRS和神经炎症(NI)原发性急性淋巴细胞白血病(ALL)异种移植模型中,抑制GM-CSF使中枢神经系统中髓样T细胞浸润减少,同时大大减少了NI、预防了CRS的发生。
(图片来源:blood)
而当他们利用CRISPR/Cas9产生GM-CSF敲除(k/o)CAR-T19细胞时,结果是与CAR-T19细胞相比,GM-CSF敲除的CAR-T19细胞保证了正常功能,而且在体内增强了抗肿瘤效应提高了整体存活率。
如此,他们证实了GM-CSF抑制,可能可消除CRS和NI同时增强CAR-T细胞功能。而关于其CAR-T19细胞治疗联合lenzilumab的临床2期研究正在计划当中。
GM-CSF中和是一种很有前景的治疗策略,它首次证明CAR-T细胞治疗的毒性可以在体内有效预防,并且不需以牺牲抗癌效力为代价。体内的临床前研究表明,中和GM-CSF可以预防CAR-T细胞诱导的CRS,并显著降低NT。GM-CSF中和在异种移植瘤模型中也观察到增强的抗肿瘤活性,提高了整体存活率和反应的持久性,降低了复发率。
关于Humanigen公司
Humanigen正在开发其Humaneered®单克隆抗体组合,以解决CAR-T优化的前沿问题,以及提供更安全、更好、更有效的癌症治疗的新型肿瘤药物的需求。Lenzilumab、Ifabotuzumab和HGEN005均来自该公司的人源平台,是具有first-in-class机制的单克隆抗体。
Lenzilumab可以中和人类GM-CSF,目前正作为一种潜在的生物疗法开发,以使CAR-T更安全、更有效,同时也是一种潜在的血液癌治疗方法。靶向EphA3的Ifabotuzumab正在进行I期研究,作为多形性胶质母细胞瘤(GBM)的潜在治疗方法,并正在研究针对一系列实体肿瘤,作为优化的裸抗体和作为抗体-药物偶联物(ADC)的一部分,以及新型CAR-T构建体的骨架和双特异性抗体平台。选择性靶向嗜酸性粒细胞受体EMR1的HGEN005,作为优化的裸抗体和新型CAR-T构建体的骨架,正在被研究用于一系列嗜酸性粒细胞疾病的潜在治疗,包括嗜酸性粒细胞白血病。(生物谷Bioon.com)
参考出处:
https://www.globenewswire.com/news-release/2019/05/16/1826585/0/en/Publication-in-blood-Highlights-Potential-for-GM-CSF-Neutralization-as-a-Solution-for-CAR-T-Induced-Neurotoxicity.html
http://www.bloodjournal.org/content/133/20/2114?sso-checked=true
http://www.bloodjournal.org/content/133/20/2212
http://www.bloodjournal.org/content/133/7/697?sso-checked=true
http://www.jbc.org/content/early/2019/02/25/jbc.AC119.007558.abstract
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->