肺动脉高压(PAH)新药!强生Uptravi静脉制剂在美国申请上市:用于暂时无法口服的患者!
来源:本站原创 2020-09-30 20:57
Uptravi口服片剂已于2015年批准上市。

2020年09月30日讯 /生物谷BIOON/ --强生(JNJ)旗下杨森制药近日宣布,已向美国食品和药物管理局(FDA)提交了Uptravi(selexipag,赛乐西帕)静脉制剂(IV)的新药申请(NDA),用于治疗目前已处方口服疗法但暂时无法接受口服疗法、WHO功能分级II-III的肺动脉高压(PAH,WHO组I)成人患者。在PAH患者中,由于疾病的进展性,应避免中断治疗。
Uptravi是一种选择性前列环素IP受体激动剂。2015年,FDA批准口服Uptravi治疗PAH,以延缓疾病进展并降低住院风险。
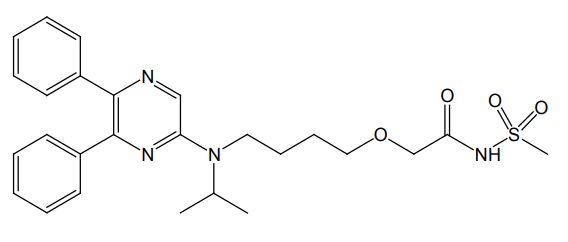
selexipag化学结构式(图片来源:Uptravi说明书)
此次NDA基于一项前瞻性、多中心3期研究的结果。该研究旨在评估PAH患者从口服Uptravi转向Uptravi IV、然后再转回至初始口服剂量的安全性和耐受性。
结果表明,在口服Uptravi不可行的情况下,Uptravi IV适合维持短时间连续给药治疗。口服Uptravi和Uptravi IV之间转换的耐受性良好,没有意外的安全性发现。Uptravi IV的不良反应与Uptravi片剂的不良反应相似,但输液部位反应除外。前列环素相关的不良反应包括头痛、腹泻、恶心、呕吐、下颚疼痛、肌痛、四肢疼痛、潮红和关节痛。
杨森研发公司肺动脉高压全球治疗区域负责人Neil Davie博士表示:“即使是由于暂时不能口服药物而导致的相对短期的PAH治疗中断,也会对患者的健康产生重大的负面影响,我们已经证明了Uptravi持续治疗可以显著改善患者的长期预后。用静脉制剂来防止治疗中断是一个重要的治疗选择,我们很高兴距离把这种重要的治疗方法带给PAH社区又近了一步。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


