CAR-T杀手!CD19靶向新型Fc优化免疫增强抗体Minjuvi(tafasitamab)欧盟即将获批:治疗B细胞瘤(DLBCL)!
来源:本站原创 2021-06-29 02:10
Minjuvi将向市面2款CAR-T细胞疗法发起挑战,该药治疗弥漫性大B细胞淋巴瘤(r/r DLBCL).
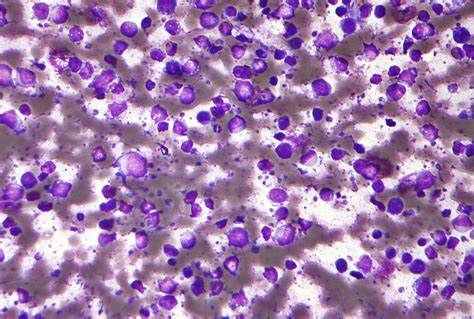
DLBCL(图片来源:meddic.jp)
2021年06月28日讯 /生物谷BIOON/ --MorphoSys和Incyte近日联合宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议附条件批准tafasitamab与来那度胺(lenalidomide)联合治疗、然后是tafasitamab单药治疗,用于治疗不符合自体干细胞移植(ASCT)条件的复发或难治性弥漫性大B细胞淋巴瘤(r/r DLBCL)成人患者。
现在,CHMP的意见将递交至欧盟委员会(EC)审查,后者预计在未来2个月内做出最终审查决定。如果获批,tafasitamab联合来那度胺将为欧盟符合资格的DLBCL患者提供一个重要的新治疗选择。今年5月,tafasitamab联合疗法一线治疗DLBCL关键3期frontMIND研究(NCT04824092)对首例患者进行了给药治疗。

tafasitamab是一种新型人源化Fc结构域优化的溶细胞性CD19靶向性免疫增强单克隆抗体,CD19是多种B细胞恶性肿瘤的一个明确生物标志物。目前,tafasitamab正处于临床开发,用于治疗多种B细胞恶性肿瘤。tafasitamab由Incyte与MorphoSys共同开发,Incyte拥有tafasitamab在美国以外地区的独家商业化权利。在美国,双方共同商业化tafasitamab,品牌名为Monjuvi。在欧盟,如果获得批准,tafasitamab将以品牌名Minjuvi上市销售。
2020年7月底,tafasitamab(Monjuvi)获得美国FDA加速批准,联合来那度胺,用于治疗不符合ASCT条件的r/r DLBCL成人患者,包括源于低级别淋巴瘤的DLBCL。值得一提的是,Monjuvi是第一个获FDA批准用于一线治疗期间或治疗后病情进展的r/r DLBCL成人患者的二线疗法。此前,FDA已授予了Monjuvi快速通道资格、突破性药物资格、优先审查资格。
CHMP积极审查意见,基于2期L-MIND研究的数据。这是一项开放标签、多中心、单臂II期研究,评估了tafasitamab联合来那度胺治疗既往已接受至少一种但不超过3种疗法(包括一种抗CD20靶向疗法,如利妥昔单抗)、没有资格接受大剂量化疗(HDC)和随后的自体干细胞移植(ASCT)的r/r DLBCL患者。
结果显示:tafasitamab+来那度胺联合治疗的总缓解率(ORR)为55%(主要终点),完全缓解率(CR)为37%、部分缓解率(PR)为18%。缓解具有持久性,中位缓解持续时间(mDOR)为21.7个月(关键次要终点)。
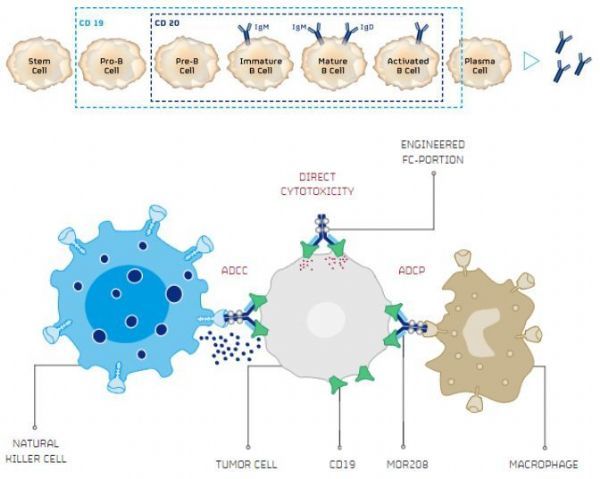
B细胞各发育阶段CD19表达及tafasitamab作用机制
tafasitamab是一种靶向CD19的新型人源化Fc增强单克隆抗体,其Fc结构域进行了修饰(包含2个氨基酸取代S239D和I332E),通过提高对效应细胞上激活型FcγRIIIa的亲和力,显著增强抗体依赖性细胞介导的细胞毒性(ADCC)和抗体依赖性细胞吞噬(ADCP),从而改善肿瘤细胞杀伤的关键机制。临床前模型研究中,tafasitamab已被证实通过结合CD19可诱导癌细胞直接凋亡。
目前,tafasitamab正被开发用于2种B细胞恶性肿瘤,包括慢性淋巴细胞白血病(CLL)和DLBCL。在全球范围内,CLL是成人中最常见的白血病类型,DLBCL是成人中最常见类型的非霍奇金淋巴瘤(NHL),占所有NHL病例的40%。DLBCL是一种影响免疫系统B细胞的侵袭性疾病,其特征是淋巴结、脾脏、肝脏、骨髓或其他器官中的恶性B细胞迅速生长。DLBCL是一种侵袭性疾病,约30%-40%的患者对初始治疗无应答或之后复发,对有效的治疗方法存在着显著未满足的医疗需求。在欧盟,每年约有16000名患者被诊断为复发或难治性DLBCL。
2010年,MorphoSys从Xencor公司授权获得了tafasitamab在全球范围内的独家开发和商业化权利。2020年1月,MorphoSys与Incyte签订一项价值20亿美元的全球合作及许可协议,共同开发和商业化tafasitamab。根据协议,MorphoSys与Incyte将在美国共同商业化Monjuvi(tafasitamab),Incyte拥有美国以外(包括欧洲)的独家商业化权利。
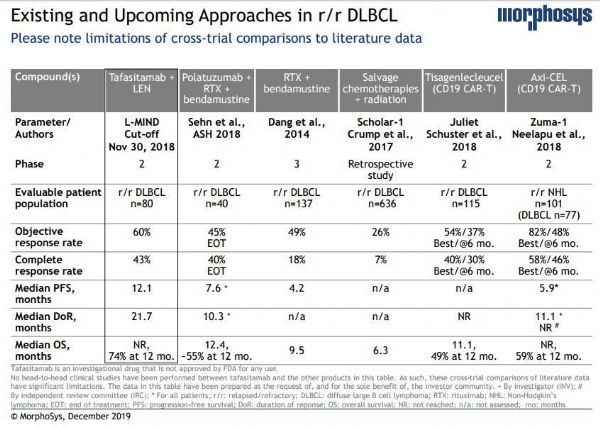
临床疗效数据对比
有分析师指出,Monjuvi上市后将直接挑战市面上治疗R/R DLBCL的2款抗CD19 CAR-T疗法——诺华Kymriah和吉利德Yescarta。CAR-T疗法与常规小分子或生物疗法不同,这是一种活的T细胞治疗产品。Kymriah和Yescarta治疗流程均需分离患者T细胞,并在体外进行基因修饰使T细胞表达一种旨在靶向CD19的嵌合抗原受体(CAR),之后将修饰后的T细胞回输患者体内,寻找表达CD19的癌细胞,发挥治疗作用。
疗效方面,Monjuvi与Kymriah和Yescarta具有可比性。用药方面,Kymriah和Yescarta均需针对每例患者单独制备,需要耗费一定时间,tafasitamab则是一种工业化生产的即用型单抗,随取随用。治疗成本方面,Kymriah和Yescarta均定价数十万美元,而tafasitamab可以控制的非常低。有分析师将tafasitamab比喻为“CAR-T细胞疗法杀手”,该药如果成功上市,势必将对Kymriah和Yescarta带来巨大的冲击。
根据MorphoSys和Incyte的业绩报告,tafasitamab在2020年8月上市后,4个月销售额达到了1850万欧元,与行业观察家预期一致。在2021年,tafasitamab预期销售额将达到1.5-2亿欧元。MorphoSys和Incyte预计,仅在美国市场,在当前已获批的二线治疗复发或难治性DLBCL方面,tafasitamab的峰值销售就将达到5-7亿欧元。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->