多篇重要研究成果聚焦癌细胞耐药研究新进展!
来源:本站原创 2020-09-25 20:40
本文中,小编整理了多篇研究成功,共同解读科学家们在癌细胞耐药研究领域取得的新成果,与大家一起学习!图片来源:CC0 Public Domain【1】JID:研究揭示BRAF耐受性黑色素瘤恶化机制doi:10.1016/j.jid.2020.08.012BRAF-MEK抑制剂的靶向治疗是针对无法手术切除或扩散到身体其他部位的晚期黑色素瘤患者的有效治疗方法。但是
本文中,小编整理了多篇研究成功,共同解读科学家们在癌细胞耐药研究领域取得的新成果,与大家一起学习!

图片来源:CC0 Public Domain
doi:10.1016/j.jid.2020.08.012
BRAF-MEK抑制剂的靶向治疗是针对无法手术切除或扩散到身体其他部位的晚期黑色素瘤患者的有效治疗方法。但是,许多患者对该疗法产生抵抗力,这通常会导致进一步的转移。莫菲特癌症中心的研究人员帮助开发了这种联合疗法,目前正在努力更好地了解导致这种抗药性的原因,以期希望找到解决方法。
在Journal of Investigative Dermatology上发表的一篇新文章中,Moffitt研究人员确定了促红细胞生成素产生的肝细胞受体A2(EphA2)是黑色素瘤转移和BRAF-MEK抑制剂耐药的驱动因素。EphA2是一种酪氨酸激酶受体,有助于在正常细胞中维持稳定的环境。但是,EphA2在许多癌症中通常过表达,并在其生长中起关键作用。它的确切功能取决于信号传导途径:经典的和非经典的。经典途径抑制癌细胞增殖并充当肿瘤抑制剂。非经典途径具有相反的作用,促进肿瘤存活和转移。
doi:10.1073/pnas.2004809117
卡波西氏肉瘤疱疹病毒(KSHV)是已知的七种引起人类癌症的病毒之一,是卡波西氏肉瘤的主要病因。卡波西氏肉瘤是一种与免疫抑制有关的疾病,主要与艾滋病有关。这些肿瘤没有特异性疗法,预后可能很差。
现在,由葡萄牙医学研究所Jo?oLobo Antunes小组负责人Pedro Simas领导的一项新研究发现了病毒蛋白LANA区域是病毒潜伏在人体细胞中并造成持续感染的关键。这些发现最近发表在《PNAS》杂志上,该研究有助于开发KSHV肿瘤的治疗方法,因为预期阻断该LANA区域的功能可消除病毒持久性,从而消除癌细胞。
doi:10.1126/sciadv.aaz4126
近日,一项刊登在国际杂志Science Advances上题为“Mre11 exonuclease activity removes the chain-terminating nucleoside analog gemcitabine from the nascent strand during DNA repli”的研究报告中,来自班戈大学等机构的科学家们通过研究深入揭示了宿主机体对癌症药物产生耐受性的分子机制。
很多癌症药物会通过抑制DNA的复制来杀灭癌细胞,其中一种药物就是吉西他滨(Gemcitabine),其能用来治疗胰腺癌、膀胱癌和肺癌,吉西他滨能模拟DNA中的基本元件—核苷脱氧胞苷(nucleoside deoxycytidine),其能竞争不断整合到癌细胞的DNA中,一旦整合后期就会抑制癌细胞DNA的复制和细胞的分裂。
【4】Nat Commun:细胞压力或会促进癌细胞对疗法产生化疗耐受性
doi:10.1038/s41467-020-16747-y
与化疗耐药相关的机制有很多,其中有很多机制目前研究人员并不清楚,近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自维也纳大学等机构的科学家们通过研究揭示了细胞压力促进癌细胞化疗耐受的分子机制。
研究者表示,这种所谓的细胞压力反应在多种疾病发生和机体对化疗耐受性上扮演着关键角色,细胞压力反应时一组能促进细胞在压力状况下存活的遗传程序;深入理解细胞压力反应或能帮助科学家们开发有效克服化疗耐受性的新型治疗策略,在此背景下,文章中,研究人员利用全面的分析方法深入揭示了未折叠蛋白反应(UPR,Unfolded Protein Response)发生的分子机制,UPR是一种由未折叠蛋白质所诱导的细胞压力反应。
【5】J Med Chem:一种新型策略或有望克服癌细胞对靶向性疗法的耐受性
doi:10.1021/acs.jmedchem.9b01709
近日,一项刊登在国际杂志Journal of Medicinal Chemistry上的研究报告中,来自伦敦癌症研究所等机构的科学家们通过研究开发了一种抑制HSP72蛋白的新方法,HSP72对于帮助癌细胞存活并抵御疗法非常重要,相关研究结果有望帮助研究人员发现靶向作用该蛋白的新型癌症药物。
更重要的是,研究人员还开发了一种检测技术来测定这种新型增强型方法相比早期手段在阻断HSP72活性上的有效性到底有多少,结果发现,新方法在阻断HSP72活性上的有效性是早期手段的100多倍。HSP72,即热激蛋白72,其对于癌细胞生存至关重要,其主要负责沉默让癌细胞自我毁灭的指令,目前研究人员很难找到有效抑制HSP72蛋白功能的新型药物。
图片来源:Guilherme de Oliveira
【6】Nat Commun:DNA的表观遗传学修饰竟会促进乳腺癌对激素疗法产生耐受性
doi:10.1038/s41467-019-14098-x
对激素疗法产生耐受性的乳腺癌细胞中的DNA常常会发生表观遗传学的改变,激素疗法是一种治疗ER+乳腺癌的有效疗法,而ER+乳腺癌在所有诊断的乳腺癌患者中占到了70%的比例;逆转这些表观遗传学改变或许有望帮助降低乳腺癌患者的复发率。
近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自悉尼加文医学研究所等机构的科学家们通过研究发现,对激素疗法耐受的ER+乳腺癌细胞中DNA的3-D结构或许发生了“重新布线”(rewired),其能够改变基因的激活和失活。研究者Clark教授表示,这项研究中我们首次揭示了一种关键的3-D DNA相互作用,其与乳腺癌是否对激素疗法敏感有关,阐明其中的过程或能帮助揭示ER+癌症躲避激素疗法的分子机制,并有望帮助开发新型乳腺癌疗法。
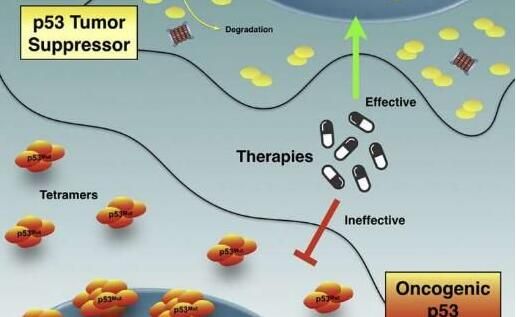
【7】iScience:揭示与p53相关的癌症化疗耐受机制
doi:10.1016/j.isci.2020.100820
在全球,有超过一半以上的癌症病例都与p53基因突变有关,其所产生的蛋白能够保护DNA免于诱发癌症的改变,当该蛋白变形时,其不仅会失去保护能力,还会产生新的功能,其就会扮演“叛徒”的角色, 通过形成可能对化疗产生耐受的蛋白簇,从而促进肿瘤的扩散,目前研究人员并不清楚这种情况发生的机制,以及其是如何产生耐药性的。
近日,一项刊登在国际杂志iScience上的研究报告中,来自巴西国家结构生物学和生物成像科学技术研究所的科学家们通过研究在胶质母细胞瘤所衍生的化疗耐受性细胞中鉴别出了大量“叛徒”蛋白,同时研究者揭示了这些蛋白如何发生变形来抵御疗法,其能形成比健康个体机体中更大尺寸的团块,其中一些还具有淀粉样蛋白的特性(当突变诱发团块时),这项研究中,研究人员首次在活细胞的细胞核中观察到了这些变化。
【8】Oncogene:新型药物组合或能有效抑制黑色素瘤对疗法产生耐受性
新闻阅读:New drug combos may prevent resistance to melanoma treatments
近日,一项刊登在国际杂志Oncogene上的研究报告中,来自密歇根州立大学的科学家们通过研究发现,一种新型药物组合或能有效抑制黑色素瘤对疗法产生耐受性,黑色素瘤是一种致死性的皮肤癌;相关研究结果或能帮助有效治疗大约一半产生药物耐受性的黑色素瘤患者。
据美国癌症协会数据显示,在所有皮肤癌患者中,黑色素瘤患者大约占到了1%的比例,但其却会引发大部分皮肤癌患者的死亡,有超过一半的黑色素瘤患者机体中携带有促癌突变,即BRAF基因突变,在这些患者中,癌症开始会对靶向作用BRAF的药物疗法维罗非尼(vemurafenib)产生反应,但很快其就会产生耐药性,从而促进黑色素瘤扩散。
【9】Cancer Discov:意外发现!免疫治疗可以识别并治疗化疗耐药肿瘤!
doi:10.1158/2159-8290.CD-19-1485
一项新的重大研究表明,可以通过一种引导免疫系统杀死具有特定耐药性的突变癌细胞的免疫疗法来治疗侵袭性癌症。研究发现,耐药突变可以恢复BRCA1或BRCA2基因的活性,从而避免药物治疗的影响,这可能会使肿瘤容易受到免疫治疗的影响。
科学家们研究了那些通过修复BRCA基因来避开铂化疗和PARP抑制剂的癌症,发现这些基因的新版本与健康细胞中的相同基因略有不同。他们相信,这些基因的差异大到足以训练人体的免疫系统识别和杀死修复BRCA基因的癌细胞--这为治疗对现有药物有耐药性的癌症开辟了一种令人兴奋的新方法。伦敦癌症研究所的科学家汇编了一个数据库,其中包括300多个报告的突变案例,这些突变改变了BRCA基因的活性,从而对PARP抑制剂产生耐药性。
【10】EMBO Mol Med:揭示癌症如何学会对化疗耐药!
doi:10.15252/emmm.201911177
根据一项对从人体采集、然后在实验室中培养的细胞进行的研究,化疗可以使卵巢癌细胞对进一步治疗产生耐药性,但阻断特定的细胞通路可能会使它们再次变得敏感。大多数晚期癌症,包括卵巢癌,最终会对治疗产生抗药性。卡罗林斯卡学院(Karolinska Institute)的Kaisa Lehti和她的同事用两种铂类化疗药物中的一种治疗卵巢癌细胞:顺铂或卡铂。他们发现,这些药物激活了一种细胞通路,使肿瘤细胞对治疗产生抗药性。
这种途径是通过在一种叫做EphA2的蛋白质上添加一个磷酸基来调节的。阻断这种化学修饰降低了卵巢癌细胞的生存能力。此外,结合化疗和一种叫做RSK的蛋白质抑制剂,可以导致培养基中以及小鼠身上的癌细胞自毁,这种抑制剂在EphA2的通路中起作用。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


