2019年6月Cell期刊不得不看的亮点研究
来源:本站原创 2019-06-30 23:00
2019年6月30日讯/生物谷BIOON/---2019年6月份即将结束了,6月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:重大突破!开发出DNA显微镜doi:10.1016/j.cell.2019.05.019传统上,科学家们使用光、X射线和电子来观察组织和细胞的内部。如今,科学家们能够在整个大脑中追踪线状的神经纤维,甚至可以观察活的小鼠胚胎如何产生原
2019年6月30日讯/生物谷BIOON/---2019年6月份即将结束了,6月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:重大突破!开发出DNA显微镜
doi:10.1016/j.cell.2019.05.019
传统上,科学家们使用光、X射线和电子来观察组织和细胞的内部。如今,科学家们能够在整个大脑中追踪线状的神经纤维,甚至可以观察活的小鼠胚胎如何产生原始心脏中的跳动细胞。但是这些显微镜无法看到的是:细胞在基因组水平上发生了什么。
如今,在一项新的研究中,美国布罗德研究所生物物理学家Joshua Weinstein、霍华德-休斯医学研究所研究员Aviv Regev和麻省理工学院分子生物学家Feng Zhang发明了一种非传统的称为“DNA显微镜(DNA microscopy)”的成像方法,它能够做到这一点。他们使用DNA“条形码”来协助确定分子在样本中的相对位置,而不依赖于光线(或者任何类型的光学器件)。相关研究结果于2019年6月20日在线发表在Cell期刊上,论文标题为“DNA Microscopy: Optics-free Spatio-genetic Imaging by a Stand-Alone Chemical Reaction”。

Weinstein说,通过使用DNA显微镜,这些研究人员能够构建细胞图像,同时获得大量的基因组信息。“这为我们提供了另一层我们无法观察到的生物学。”
2.Cell:开发出将多种单细胞数据集结合在一起的新工具,有助确定细胞类型
doi:10.1016/j.cell.2019.05.006
在一项新的研究中,美国斯坦利精神病学研究中心准会员Evan Macosko、访问学者Joshua Welch及其团队开发出一种将这些数据集结合在一起的新工具。这种称为基因组实验关系关联推理(Linked Inference of Genomic Experimental Relationships, LIGER)的工具将不同的单细胞数据集整合在一起;将来自不同受试者、物种或分子衡量指标的类似细胞进行分组;针对不同组彼此之间的关系构建图谱。相关研究结果发表在2019年6月13日的Cell期刊上,论文标题为“Single-Cell Multi-omic Integration Compares and Contrasts Features of Brain Cell Identity”。
当这些研究人员在LIGER中加载单细胞数据集时,这种工具使用一种称为“整合性非负矩阵分解(integrative non-negative matrix factorization)”的统计方法,基于两个定义的特征---一组对细胞原始数据集是独特的因子和一组在不同数据集之间都共有的因子(通常对应于生物学上有意义的信号)---来识别和聚类细胞。这种方法使得人们能够更清晰地查看来自不同来源的细胞之间的共有特征和独特特征。
这些研究人员以四种方式测试了LIGER。首先,他们使用这种工具来定量确定不同大脑区域和不同动物之间的小鼠脑细胞类型差异。其次,他们使用LIGER通过比较来自人类和小鼠相同大脑区域的脑细胞来探究不同物种之间的相似性和差异。第三,他们使用这种工具研究单细胞RNA测序(scRNA-seq)和原位RNA测序分析的小鼠脑细胞的空间关系,从而将受测试的细胞与它们的原始大脑位置相匹配在一起。第四,这些研究人员使用LIGER通过将scRNA-seq和DNA甲基化谱合并在一起来研究小鼠脑细胞的表观基因组特征。
3.Cell:阻断肝脏中的酶CerS6功能有望让喜欢吃高脂肪饮食的胖子变瘦
doi:10.1016/j.cell.2019.05.008
吃太多脂肪和糖会导致体重增加和健康状况下降。但为什么会这样,是否有补救措施?在一项新的研究中,德国马克斯-普朗克代谢研究所的Jens Brüning教授及其团队发现改变肝脏中的脂肪代谢能够让吃不健康饮食的肥胖小鼠变瘦。这一过程也改善了这些小鼠的葡萄糖代谢。这是通过关闭一种称为神经酰胺合酶6(ceramide synthase 6, CerS6)的蛋白来实现的。相关研究结果近期发表在Cell期刊上,论文标题为“CerS6-Derived Sphingolipids Interact with Mff and Promote Mitochondrial Fragmentation in Obesity”。
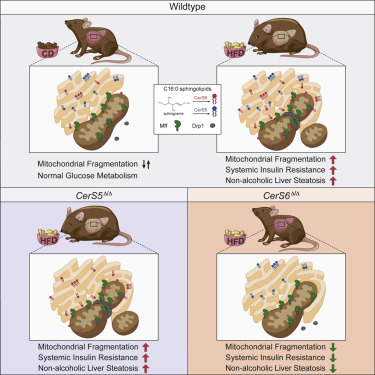
他们发现当小鼠因摄入高脂肪饮食而变得肥胖时,由神经酰胺合酶5(CerS5)和神经酰胺合酶6(CerS6)形成的特定长度的神经酰胺分子在肝脏中堆积。Hammerschmidt解释道,“有趣的是,通过遗传手段仅让小鼠中的CerS6失活才能阻止肥胖、脂肪肝和胰岛素抵抗性产生。但是,缺乏CerS5活性则不会产生这些影响。”
4.Cell:破解奥秘!母亲的免疫力是如何转移到婴儿机体中的?
doi:10.1016/j.cell.2019.05.044
作为世界上最成功的减少传染病的干预措施之一,疫苗接种在保护新生儿患者方面的效果仍然非常有限,近日,一项刊登在国际杂志Cell上的研究报告中,来自美国麻省总医院、MIT和哈佛大学的研究人员通过研究阐明了孕妇进行疫苗接种的免疫力传递给婴儿的分子机制,相关研究结果有望帮助开发更为有效的母源性疫苗。
研究者Galit Alter博士说道,新生儿来到世上的第一天就拥有了全新的免疫系统,其需要学习如何有效应对环境中的有益和有害的微生物。为了帮助新生儿的免疫系统有效区分敌我,母亲会通过胎盘来将抗体转移到胎儿体内,而目前研究人员并不清楚胎盘是如何发挥这一绝对且必要的规则的,如果能够对此进行解码的话,科学家们或许就能获取开发更为有效疫苗来抵御疾病的关键信息。
当抵御诸如麻疹等疾病的母源性抗体通过母体转移到胎儿体内时,其就会为胎儿提供保护力直到孩子长大到可以单独接种疫苗为止,而抵御诸如脊髓灰质炎等严重疾病的抗体并不会从母体有效转移到胎儿体内;为了调查抗体从母体转移到胎儿机体中的分子机制,研究人员利用一种名为系统血清学的新工具比较了来自母体和脐带中血液样本中抵御百日咳的抗体的数量和质量,脐带能够携带来自胎盘的血液、营养物质和免疫因子进入胎儿体内。
研究者表示,胎盘会优先筛选并运输传递给婴儿抗体,这些抗体则会激活自然杀伤细胞(NK细胞),而NK细胞是机体免疫系统的关键元件;虽然新生儿体内多种重要的免疫细胞并没有成熟到足以提供有效的保护效力,但NK细胞是其生命最初几天里最为丰富和功能最强的免疫细胞。研究者发现,胎盘转移的NK细胞激活抗体在抵御流感病毒和呼吸道合胞病毒上似乎有类似的偏好,同时研究者还发现了似乎可以调节胎盘选择的抗体特性,这些特性可能会被植入到下一代疫苗中,从而改善母婴的抗体转移。
5.Cell:非吸烟肺腺癌的基因组重排早在癌症确诊前30年就已存在
doi:10.1016/j.cell.2019.05.013
在一项新的研究中,来自韩国科学技术高级研究院(KAIST)和首尔大学等研究机构的研究人员发现早在童年和青春期发生的灾难性基因组重排可导致非吸烟者在晚年患上肺癌。这一发现发有助于解释一些与非吸烟有关的肺癌是如何产生的。相关研究结果近期发表在Cell期刊上,论文标题为“Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma”。
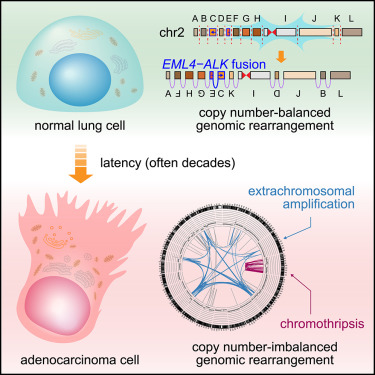
这些研究人员证实非吸烟者体内的基因融合大多较早地发生,有时早在儿童期或青春期,平均而言在肺癌确诊前三十年发生。这项研究表明,这些携带致癌种子(oncogenic seed)的突变肺细胞几十年来一直处于休眠状态,直到进一步的许多其他突变充分积累才进展为肺癌。这是首次揭示肺腺癌基因组结构变异景观的研究。
6.Cell:新药物能够提高癌细胞对化疗的敏感性
doi:10.1016/j.cell.2019.05.028
许多化疗药物通过破坏DNA来杀死癌细胞。然而,一些肿瘤可以通过依赖DNA修复途径来抵抗这种损伤,这种机制不仅可以使它们存活,而且还会引入有助于细胞对未来治疗产生抗性的突变。麻省理工学院和杜克大学的研究人员现在发现了一种可以阻断这种修复途径的潜在药物化合物。当他们用这种化合物和顺铂(一种破坏DNA的药物)治疗小鼠时,肿瘤比仅用顺铂治疗的肿瘤缩小得多。用这种组合治疗的肿瘤预计不会产生可能使它们具有耐药性的新突变。
顺铂作为至少十二种癌症的首选治疗选择,通常可以成功地破坏肿瘤,但它们经常在治疗后复发。研究人员表示,针对诱导这种复发的诱变DNA修复途径的药物不仅有助于提高顺铂的长期有效性,还有助于提高其他能够破坏DNA的化疗药物的长期有效性。
“我们正在努力使治疗效果更好,我们也希望在重复剂量下使肿瘤对治疗反复敏感,”相关结果发表在最近的《Cell》杂志上。
7.Cell:科学家鉴别出人类机体的保护性抗体 有望帮助开发新型有效的抗疟疾疫苗
doi:10.1016/j.cell.2019.05.025
近日,一项刊登在国际杂志Cell上的研究报告中,来自牛津大学等机构的科学家们通过研究鉴别出了一种人类抗体,其或能抑制疟原虫进入血细胞中,相关研究或有望帮助开发出新型高效的疟疾疫苗。
研究者Simon Draper教授说道,当被携带疟原虫的蚊子叮咬后,疟原虫首先会进入人类肝脏组织,随后就会移动到血液中,在宿主机体血液中疟原虫会每隔48小时复制10次,而这是引发感染的血液阶段,随后其就会让感染者致病,且有可能是致命性的。疟原虫携带一种名为RH5的蛋白质,其必须结合到血细胞中名为基础免疫球蛋白(basic immunoglobulin,basigin)的人类蛋白上才能够对宿主进行感染,这项研究中,研究者阐明了哪种人类抗体能够有效阻断RH5与basigin的结合,从而阻断疟原虫通过血液来扩散。
截至目前为止,研究人员并不清楚给人类志愿者接种疫苗能够产生哪类特异性抗体,从而能够有效阻断RH5与红细胞进行结合,当某个人被接种疫苗时,其机体就会产生不同类型的抗体来抵御相同的RH5靶点,因此理解哪类特殊抗体能够有效抵御疟疾就显得尤为重要了。本文研究的另一个关键点就是,研究者鉴别出了一种新型抗体,其能通过减缓RH5与红细胞的结合速度来发挥作用,疟原虫依然能够入侵宿主,但这种抗体能够有效减缓这种入侵作用,这或许就使得阻断RH5的抗体有更多的时间来发挥作用,从而使其变得更加有效,这或许是一个令人非常激动的新发现,因为研究结果表明,无法阻止疟原虫进入红细胞的抗体或许依然能够发挥作用,因为其能通过制造更具潜力的保护性抗体来发挥作用。
8.Cell:首次揭示拟核的大小随着细菌细胞的大小增加而扩大
doi:10.1016/j.cell.2019.05.017
生物扩展(biological scaling)的例子无处不在。小鼠的爪子小于人手。随着我们的发育和成长,我们自己的器官和四肢通常随着我们体型的增加而扩大。在一项新的研究中,来自美国耶鲁大学的研究人员发现在亚细胞水平上,同样的现象也存在于最小的细菌中,在那里,拟核(nucleoid)---包含细菌基因的无膜区域---的大小也随着细菌细胞的大小增加而扩大。相关研究结果近期发表在Cell期刊上,论文标题为“Nucleoid Size Scaling and Intracellular Organization of Translation across Bacteria”。
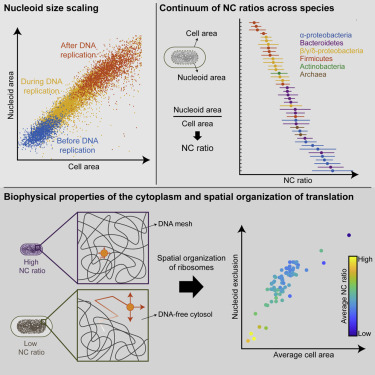
在这项新的研究中,这些研究人员作出结论:在细胞水平上,这种扩展效应存在于不同的细菌种类中,而且细菌细胞在生长上与它们的拟核具有相同的速率,但与DNA含量的变化无关。在耶鲁大学分子、细胞与发育生物学系教授Christine Jacobs-Wagner博士的领导下,这些研究人员证实这种扩展特性可能在数十亿年前就已存在,早于胞内膜结构的产生。
9.Cell: 基因的翻译过程可能比想象的更为复杂
doi:10.1016/j.cell.2019.05.001
来自Hubrecht研究所的Marvin Tanenbaum小组的研究人员表明,DNA的翻译过程比以前想象的要复杂得多。他们的研究发表在最近的《Cell》杂志上。
我们体内的每个细胞都含有相同的DNA,但不同的细胞,如脑细胞或肌肉细胞,具有不同的功能。细胞功能的差异取决于基因的选择性活化。存储在这些基因中的遗传信息由称为核糖体的细胞器翻译。
在最近这项研究中,研究人员开发了一种新方法来可视化我们在活细胞中的遗传信息的解码。他们能够以不同的颜色标记不同的蛋白质,并使用先进的显微镜观察每种蛋白质的翻译过程。
研究人员发现,错误翻译的发生频率惊人。在极端情况下,几乎一半的蛋白质都是通过与预期代码不同的顺序产生的。这些令人惊讶的发现表明,我们DNA中存储的遗传信息比以前认为的要复杂得多。基于这项新研究,我们的DNA可能编码了数千种以前未知的功能未知的蛋白质。“我们的研究揭示了非常重要的问题:所有这些新蛋白质的作用是什么?它们在我们体内是否具有重要功能?”
10.Cell:基质细胞影响胰腺癌细胞的增殖与恶化
doi:10.1016/j.cell.2019.05.012
马萨诸塞州综合医院(MGH)癌症中心的研究人员进行的一项研究表明,肿瘤内基质可以影响个体癌细胞增殖和转移的能力。他们的报告详细描述了肿瘤细胞和基质细胞的相对数量如何改变个体肿瘤细胞内基因表达的模式,并可能为这种难以治疗的癌症提供改进的治疗方法。相关结果发表在最近的《Cell》杂志上。
“我们发现胰腺癌细胞可以根据周围细胞的类型表现出不同的行为,这可以解释为什么有些细胞会对化学疗法和放射疗法做出反应,有些则不能。我们还发现了一种独特的细胞类型,能够同时复制和移动,激活MAPK和STAT3信号通路,并通过联合使用MAPK和STAT3抑制剂杀死,这表明了一种潜在的治疗策略。”
MGH团队最近的研究发现原发肿瘤中的胰腺癌细胞和血流中循环的胰腺癌细胞之间的基因表达存在显着差异,其中一些表达的特征表明增殖特征,另一些表现出更多的转移潜能。肿瘤和基质之间界面处的癌细胞亚群也表达了这些不同的遗传特征,表明它们可能受到基质中CAF的影响。
“我们开发的用于鉴定这些不同肿瘤腺体的检测方法提供了一种策略,可以将其用作生物标志物,根据正常细胞对癌症的反应选择个性化治疗,”哈佛医学院医学助理教授Ting说。“鉴定MAPK和STAT3信号在产生不同类型的PDAC中的作用以及CAF分泌的TGF-β在该信号传导中的作用表明研究不同基质组合物如何确定最佳药物组合的重要性。”(生物谷 Bioon.com)
1.Cell:重大突破!开发出DNA显微镜
doi:10.1016/j.cell.2019.05.019
传统上,科学家们使用光、X射线和电子来观察组织和细胞的内部。如今,科学家们能够在整个大脑中追踪线状的神经纤维,甚至可以观察活的小鼠胚胎如何产生原始心脏中的跳动细胞。但是这些显微镜无法看到的是:细胞在基因组水平上发生了什么。
如今,在一项新的研究中,美国布罗德研究所生物物理学家Joshua Weinstein、霍华德-休斯医学研究所研究员Aviv Regev和麻省理工学院分子生物学家Feng Zhang发明了一种非传统的称为“DNA显微镜(DNA microscopy)”的成像方法,它能够做到这一点。他们使用DNA“条形码”来协助确定分子在样本中的相对位置,而不依赖于光线(或者任何类型的光学器件)。相关研究结果于2019年6月20日在线发表在Cell期刊上,论文标题为“DNA Microscopy: Optics-free Spatio-genetic Imaging by a Stand-Alone Chemical Reaction”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.05.019。
Weinstein说,通过使用DNA显微镜,这些研究人员能够构建细胞图像,同时获得大量的基因组信息。“这为我们提供了另一层我们无法观察到的生物学。”
2.Cell:开发出将多种单细胞数据集结合在一起的新工具,有助确定细胞类型
doi:10.1016/j.cell.2019.05.006
在一项新的研究中,美国斯坦利精神病学研究中心准会员Evan Macosko、访问学者Joshua Welch及其团队开发出一种将这些数据集结合在一起的新工具。这种称为基因组实验关系关联推理(Linked Inference of Genomic Experimental Relationships, LIGER)的工具将不同的单细胞数据集整合在一起;将来自不同受试者、物种或分子衡量指标的类似细胞进行分组;针对不同组彼此之间的关系构建图谱。相关研究结果发表在2019年6月13日的Cell期刊上,论文标题为“Single-Cell Multi-omic Integration Compares and Contrasts Features of Brain Cell Identity”。
当这些研究人员在LIGER中加载单细胞数据集时,这种工具使用一种称为“整合性非负矩阵分解(integrative non-negative matrix factorization)”的统计方法,基于两个定义的特征---一组对细胞原始数据集是独特的因子和一组在不同数据集之间都共有的因子(通常对应于生物学上有意义的信号)---来识别和聚类细胞。这种方法使得人们能够更清晰地查看来自不同来源的细胞之间的共有特征和独特特征。
这些研究人员以四种方式测试了LIGER。首先,他们使用这种工具来定量确定不同大脑区域和不同动物之间的小鼠脑细胞类型差异。其次,他们使用LIGER通过比较来自人类和小鼠相同大脑区域的脑细胞来探究不同物种之间的相似性和差异。第三,他们使用这种工具研究单细胞RNA测序(scRNA-seq)和原位RNA测序分析的小鼠脑细胞的空间关系,从而将受测试的细胞与它们的原始大脑位置相匹配在一起。第四,这些研究人员使用LIGER通过将scRNA-seq和DNA甲基化谱合并在一起来研究小鼠脑细胞的表观基因组特征。
3.Cell:阻断肝脏中的酶CerS6功能有望让喜欢吃高脂肪饮食的胖子变瘦
doi:10.1016/j.cell.2019.05.008
吃太多脂肪和糖会导致体重增加和健康状况下降。但为什么会这样,是否有补救措施?在一项新的研究中,德国马克斯-普朗克代谢研究所的Jens Brüning教授及其团队发现改变肝脏中的脂肪代谢能够让吃不健康饮食的肥胖小鼠变瘦。这一过程也改善了这些小鼠的葡萄糖代谢。这是通过关闭一种称为神经酰胺合酶6(ceramide synthase 6, CerS6)的蛋白来实现的。相关研究结果近期发表在Cell期刊上,论文标题为“CerS6-Derived Sphingolipids Interact with Mff and Promote Mitochondrial Fragmentation in Obesity”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.05.008。
他们发现当小鼠因摄入高脂肪饮食而变得肥胖时,由神经酰胺合酶5(CerS5)和神经酰胺合酶6(CerS6)形成的特定长度的神经酰胺分子在肝脏中堆积。Hammerschmidt解释道,“有趣的是,通过遗传手段仅让小鼠中的CerS6失活才能阻止肥胖、脂肪肝和胰岛素抵抗性产生。但是,缺乏CerS5活性则不会产生这些影响。”
4.Cell:破解奥秘!母亲的免疫力是如何转移到婴儿机体中的?
doi:10.1016/j.cell.2019.05.044
作为世界上最成功的减少传染病的干预措施之一,疫苗接种在保护新生儿患者方面的效果仍然非常有限,近日,一项刊登在国际杂志Cell上的研究报告中,来自美国麻省总医院、MIT和哈佛大学的研究人员通过研究阐明了孕妇进行疫苗接种的免疫力传递给婴儿的分子机制,相关研究结果有望帮助开发更为有效的母源性疫苗。
研究者Galit Alter博士说道,新生儿来到世上的第一天就拥有了全新的免疫系统,其需要学习如何有效应对环境中的有益和有害的微生物。为了帮助新生儿的免疫系统有效区分敌我,母亲会通过胎盘来将抗体转移到胎儿体内,而目前研究人员并不清楚胎盘是如何发挥这一绝对且必要的规则的,如果能够对此进行解码的话,科学家们或许就能获取开发更为有效疫苗来抵御疾病的关键信息。
当抵御诸如麻疹等疾病的母源性抗体通过母体转移到胎儿体内时,其就会为胎儿提供保护力直到孩子长大到可以单独接种疫苗为止,而抵御诸如脊髓灰质炎等严重疾病的抗体并不会从母体有效转移到胎儿体内;为了调查抗体从母体转移到胎儿机体中的分子机制,研究人员利用一种名为系统血清学的新工具比较了来自母体和脐带中血液样本中抵御百日咳的抗体的数量和质量,脐带能够携带来自胎盘的血液、营养物质和免疫因子进入胎儿体内。
研究者表示,胎盘会优先筛选并运输传递给婴儿抗体,这些抗体则会激活自然杀伤细胞(NK细胞),而NK细胞是机体免疫系统的关键元件;虽然新生儿体内多种重要的免疫细胞并没有成熟到足以提供有效的保护效力,但NK细胞是其生命最初几天里最为丰富和功能最强的免疫细胞。研究者发现,胎盘转移的NK细胞激活抗体在抵御流感病毒和呼吸道合胞病毒上似乎有类似的偏好,同时研究者还发现了似乎可以调节胎盘选择的抗体特性,这些特性可能会被植入到下一代疫苗中,从而改善母婴的抗体转移。
5.Cell:非吸烟肺腺癌的基因组重排早在癌症确诊前30年就已存在
doi:10.1016/j.cell.2019.05.013
在一项新的研究中,来自韩国科学技术高级研究院(KAIST)和首尔大学等研究机构的研究人员发现早在童年和青春期发生的灾难性基因组重排可导致非吸烟者在晚年患上肺癌。这一发现发有助于解释一些与非吸烟有关的肺癌是如何产生的。相关研究结果近期发表在Cell期刊上,论文标题为“Tracing Oncogene Rearrangements in the Mutational History of Lung Adenocarcinoma”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.05.013。
这些研究人员证实非吸烟者体内的基因融合大多较早地发生,有时早在儿童期或青春期,平均而言在肺癌确诊前三十年发生。这项研究表明,这些携带致癌种子(oncogenic seed)的突变肺细胞几十年来一直处于休眠状态,直到进一步的许多其他突变充分积累才进展为肺癌。这是首次揭示肺腺癌基因组结构变异景观的研究。
6.Cell:新药物能够提高癌细胞对化疗的敏感性
doi:10.1016/j.cell.2019.05.028
许多化疗药物通过破坏DNA来杀死癌细胞。然而,一些肿瘤可以通过依赖DNA修复途径来抵抗这种损伤,这种机制不仅可以使它们存活,而且还会引入有助于细胞对未来治疗产生抗性的突变。麻省理工学院和杜克大学的研究人员现在发现了一种可以阻断这种修复途径的潜在药物化合物。当他们用这种化合物和顺铂(一种破坏DNA的药物)治疗小鼠时,肿瘤比仅用顺铂治疗的肿瘤缩小得多。用这种组合治疗的肿瘤预计不会产生可能使它们具有耐药性的新突变。
顺铂作为至少十二种癌症的首选治疗选择,通常可以成功地破坏肿瘤,但它们经常在治疗后复发。研究人员表示,针对诱导这种复发的诱变DNA修复途径的药物不仅有助于提高顺铂的长期有效性,还有助于提高其他能够破坏DNA的化疗药物的长期有效性。
“我们正在努力使治疗效果更好,我们也希望在重复剂量下使肿瘤对治疗反复敏感,”相关结果发表在最近的《Cell》杂志上。
7.Cell:科学家鉴别出人类机体的保护性抗体 有望帮助开发新型有效的抗疟疾疫苗
doi:10.1016/j.cell.2019.05.025
近日,一项刊登在国际杂志Cell上的研究报告中,来自牛津大学等机构的科学家们通过研究鉴别出了一种人类抗体,其或能抑制疟原虫进入血细胞中,相关研究或有望帮助开发出新型高效的疟疾疫苗。
研究者Simon Draper教授说道,当被携带疟原虫的蚊子叮咬后,疟原虫首先会进入人类肝脏组织,随后就会移动到血液中,在宿主机体血液中疟原虫会每隔48小时复制10次,而这是引发感染的血液阶段,随后其就会让感染者致病,且有可能是致命性的。疟原虫携带一种名为RH5的蛋白质,其必须结合到血细胞中名为基础免疫球蛋白(basic immunoglobulin,basigin)的人类蛋白上才能够对宿主进行感染,这项研究中,研究者阐明了哪种人类抗体能够有效阻断RH5与basigin的结合,从而阻断疟原虫通过血液来扩散。
截至目前为止,研究人员并不清楚给人类志愿者接种疫苗能够产生哪类特异性抗体,从而能够有效阻断RH5与红细胞进行结合,当某个人被接种疫苗时,其机体就会产生不同类型的抗体来抵御相同的RH5靶点,因此理解哪类特殊抗体能够有效抵御疟疾就显得尤为重要了。本文研究的另一个关键点就是,研究者鉴别出了一种新型抗体,其能通过减缓RH5与红细胞的结合速度来发挥作用,疟原虫依然能够入侵宿主,但这种抗体能够有效减缓这种入侵作用,这或许就使得阻断RH5的抗体有更多的时间来发挥作用,从而使其变得更加有效,这或许是一个令人非常激动的新发现,因为研究结果表明,无法阻止疟原虫进入红细胞的抗体或许依然能够发挥作用,因为其能通过制造更具潜力的保护性抗体来发挥作用。
8.Cell:首次揭示拟核的大小随着细菌细胞的大小增加而扩大
doi:10.1016/j.cell.2019.05.017
生物扩展(biological scaling)的例子无处不在。小鼠的爪子小于人手。随着我们的发育和成长,我们自己的器官和四肢通常随着我们体型的增加而扩大。在一项新的研究中,来自美国耶鲁大学的研究人员发现在亚细胞水平上,同样的现象也存在于最小的细菌中,在那里,拟核(nucleoid)---包含细菌基因的无膜区域---的大小也随着细菌细胞的大小增加而扩大。相关研究结果近期发表在Cell期刊上,论文标题为“Nucleoid Size Scaling and Intracellular Organization of Translation across Bacteria”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.05.017。
在这项新的研究中,这些研究人员作出结论:在细胞水平上,这种扩展效应存在于不同的细菌种类中,而且细菌细胞在生长上与它们的拟核具有相同的速率,但与DNA含量的变化无关。在耶鲁大学分子、细胞与发育生物学系教授Christine Jacobs-Wagner博士的领导下,这些研究人员证实这种扩展特性可能在数十亿年前就已存在,早于胞内膜结构的产生。
9.Cell: 基因的翻译过程可能比想象的更为复杂
doi:10.1016/j.cell.2019.05.001
来自Hubrecht研究所的Marvin Tanenbaum小组的研究人员表明,DNA的翻译过程比以前想象的要复杂得多。他们的研究发表在最近的《Cell》杂志上。
我们体内的每个细胞都含有相同的DNA,但不同的细胞,如脑细胞或肌肉细胞,具有不同的功能。细胞功能的差异取决于基因的选择性活化。存储在这些基因中的遗传信息由称为核糖体的细胞器翻译。
在最近这项研究中,研究人员开发了一种新方法来可视化我们在活细胞中的遗传信息的解码。他们能够以不同的颜色标记不同的蛋白质,并使用先进的显微镜观察每种蛋白质的翻译过程。
研究人员发现,错误翻译的发生频率惊人。在极端情况下,几乎一半的蛋白质都是通过与预期代码不同的顺序产生的。这些令人惊讶的发现表明,我们DNA中存储的遗传信息比以前认为的要复杂得多。基于这项新研究,我们的DNA可能编码了数千种以前未知的功能未知的蛋白质。“我们的研究揭示了非常重要的问题:所有这些新蛋白质的作用是什么?它们在我们体内是否具有重要功能?”
10.Cell:基质细胞影响胰腺癌细胞的增殖与恶化
doi:10.1016/j.cell.2019.05.012
马萨诸塞州综合医院(MGH)癌症中心的研究人员进行的一项研究表明,肿瘤内基质可以影响个体癌细胞增殖和转移的能力。他们的报告详细描述了肿瘤细胞和基质细胞的相对数量如何改变个体肿瘤细胞内基因表达的模式,并可能为这种难以治疗的癌症提供改进的治疗方法。相关结果发表在最近的《Cell》杂志上。
“我们发现胰腺癌细胞可以根据周围细胞的类型表现出不同的行为,这可以解释为什么有些细胞会对化学疗法和放射疗法做出反应,有些则不能。我们还发现了一种独特的细胞类型,能够同时复制和移动,激活MAPK和STAT3信号通路,并通过联合使用MAPK和STAT3抑制剂杀死,这表明了一种潜在的治疗策略。”
MGH团队最近的研究发现原发肿瘤中的胰腺癌细胞和血流中循环的胰腺癌细胞之间的基因表达存在显着差异,其中一些表达的特征表明增殖特征,另一些表现出更多的转移潜能。肿瘤和基质之间界面处的癌细胞亚群也表达了这些不同的遗传特征,表明它们可能受到基质中CAF的影响。
“我们开发的用于鉴定这些不同肿瘤腺体的检测方法提供了一种策略,可以将其用作生物标志物,根据正常细胞对癌症的反应选择个性化治疗,”哈佛医学院医学助理教授Ting说。“鉴定MAPK和STAT3信号在产生不同类型的PDAC中的作用以及CAF分泌的TGF-β在该信号传导中的作用表明研究不同基质组合物如何确定最佳药物组合的重要性。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


