“优化版”赫赛汀!Fc优化免疫增强抗体margetuximab治疗胃癌疗效强劲,再鼎医药引入中国开发!
来源:本站原创 2020-07-11 16:40
在(HER2扩增/HER2高表达/PD-L1阳性)双阳和三阳患者中,总缓解率高达44-60%。

2020年07月11日讯 /生物谷BIOON/ --再鼎医药合作伙伴MacroGenics近日宣布,评估HER2靶向抗体margetuximab联合默沙东抗PD-1疗法Keytruda(可瑞达,通用名:pembrolizumab,帕博利珠单抗)作为一种无化疗方案,治疗HER2阳性晚期胃食管腺癌(GEA)患者疗效和安全性的一项II期研究(CP-MGAH22-0,NCT02689284)的结果已发表于《柳叶刀肿瘤学》(Lancet Oncology)。
这是一项单臂、开放标签、Ib/II期剂量递增和队列扩展研究,在先前至少接受过曲妥珠单抗(trastuzumab)+化疗治疗后病情进展的局部晚期不可切除性或转移性HER2阳性胃癌患者中开展。入组患者为胃癌(GC)或胃食管交界(GEJ)癌症患者,其肿瘤在确诊时为IHC3阳性或IHC2阳性/FISH阳性,不考虑PD-L1表达状态,后者随后在可用的存档肿瘤组织中确定。
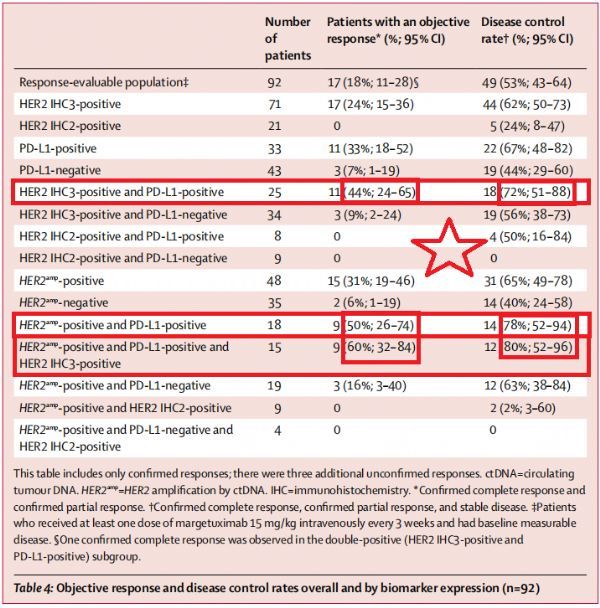
此次发表的数据截止至2019年7月10日。按推荐II期剂量(每3周一次,15mg/kg)接受margetuximab治疗的92例患者可进行疗效评估。中位随访19.9个月,在整个人群中,客观缓解率(ORR)为18%(17/92,部分缓解+完全缓解[PR+CR])、疾病控制率(DCR)为53%(49/92,CR+PR+稳定疾病[SD])。中位无进展生存期(PFS)为2.7个月(95%CI:1.6-4.3)、中位总生存期(OS)为12.5个月(95%CI:9.1-14.1)。
该研究中,margetuximab和Keytruda的活性在关键生物标志物阳性亚组中更为显著。最显著的益处是在诊断时HER2高表达(HER2 IHC3阳性)和PD-L1阳性的患者中观察到。在这个双阳性亚组中,ORR为44%(11/25)、DCR为72%(18/25)、PFS中位数为4.8个月(95%CI:1.6-13.9)、OS中位数为20.5个月(95%CI:8.1-NR)。
最初HER2阳性的GEA患者在曲妥珠单抗(trastuzumab)治疗后可能会失去HER2的表达。在这项二线治疗研究中,42%的患者的循环肿瘤DNA(ctDNA)中未检测到HER2扩增(HER2amp),这表明使用曲妥珠单抗治疗后、margetuximab和Keytruda治疗前HER2缺失。在本研究中,ctDNA中存在HER2amp与较高的缓解率相关。HER2amp阳性/HER2 IHC3阳性/PD-L1阳性患者中,ORR为60%(9/15)、DCR为80%(12/15)。
与先前关于margetuximab在其他肿瘤类型中的研究一致,该研究中对治疗的GEA患者样本进行的相关分析显示抗HER2特异性T细胞免疫增强,提示先天性和适应性免疫反应的参与潜力。
研究中,margetuximab和Keytruda的耐受性是可接受的。20%的患者出现≥3级治疗相关不良事件(TRAE),其中最常见的是贫血(4%)和输液相关反应(3%)。无治疗相关死亡报告。
上述结果表明,在曲妥珠单抗难治的二线患者中的这些数据,为正在进行的II/III期MAHOGANY临床试验(NCT04082364)提供了理论依据。MAHOGANY研究正在评估margetuximab联合免疫检查点抑制剂、联用或不联用化疗,一线治疗HER2阳性胃癌(GC)或胃食管交界癌(GEJC)患者,该研究由MacroGenics和再鼎医药在全球多个临床中心开展,再鼎医药将进行该产品在中国的临床开发。
MacroGenics临床开发高级副总裁兼首席医疗官Stephen Eck医学博士表示:“目前,转移性胃食管腺癌(GEA)患者的治疗标准很大程度上依赖于细胞毒性化疗。已发表的数据表明,结合margetuximab的免疫增强特性和检查点阻断的一种无化疗方案,可能改善某些转移性HER2阳性胃食管腺癌一线患者的临床结果,并为正在进行的II/III期MAHOGANY研究提供了有力的理论依据。”
胃癌(GC)或胃食管交界癌(GEJC)统称为胃食管腺癌(GEA),是全球第五、中国第二常见肿瘤类型。大部分GC和GEJC患者在确诊时已是晚期,因此预后很差,5年生存率为5-20%。化疗是一线治疗的标准疗法,HER2阳性患者可以采用化疗与曲妥珠单抗联合患者,这类患者约占20%。
2018年11月底,再鼎医药(ZLAB)与MacroGenics达成广泛战略合作协议,获得了3款免疫肿瘤学产品在中国大陆、香港、澳门和台湾地区的开发和商业化独家授权。
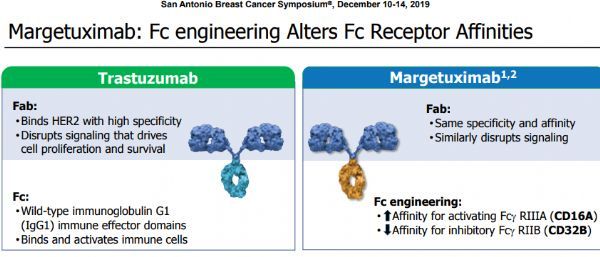
margetuximab是一款靶向人表皮生长因子受体2(HER2)的Fc优化单抗。HER2在乳腺癌、胃食管癌和其他实体瘤中均有表达。margetuximab被设计用于提供HER2阻断作用,具有与曲妥珠单抗类似的HER2结合和抗增殖效应。
此外,margetuximab已通过MacroGenics的Fc优化技术进行了工程设计,以增强其免疫系统的参与度,并通过抗体依赖性细胞介导的细胞毒性作用(ADCC)提高对癌细胞的杀伤力。除了胃食管腺癌, margetuximab也正被开发与化疗联用,用于治疗既往已接受抗HER2靶向疗法治疗的转移性HER2阳性乳腺癌患者。
2019年12月,MacroGenics向美国FDA提交了margetuximab联合化疗方案治疗转移性HER2阳性乳腺癌患者的生物制品许可申请(BLA),该BLA正在接受FDA审查,处方药用户收费法(PDUFA)目标日期为2020年12月18日。今年6月,FDA还授予了margetuximab治疗胃癌和胃食管交界癌的孤儿药资格(ODD)。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->