AZ抗CTLA-4单抗终迎曙光 贯续治疗肝癌mOS超18个月
来源:新浪医药新闻 2020-06-03 07:24
阿斯利康的肿瘤免疫疗法抗CTLA-4单抗tremelimumab经历了一系列的临床失败,这些失败使该药至今仍无法上市。然而,来自一项新的II期研究结果显示,该公司可能能够以一种新的方式来使用这款药物。上周末,阿斯利康在ASCO虚拟年会上公布了一项II期研究,该研究在先前接受过治疗的肝细胞癌患者中开展,评估了单次300mg初始剂量的tremelimumab、随
阿斯利康的肿瘤免疫疗法抗CTLA-4单抗tremelimumab经历了一系列的临床失败,这些失败使该药至今仍无法上市。然而,来自一项新的II期研究结果显示,该公司可能能够以一种新的方式来使用这款药物。
上周末,阿斯利康在ASCO虚拟年会上公布了一项II期研究,该研究在先前接受过治疗的肝细胞癌患者中开展,评估了单次300mg初始剂量的tremelimumab、随后进行抗PD-1疗法Imfinzi(duravulumab)治疗。
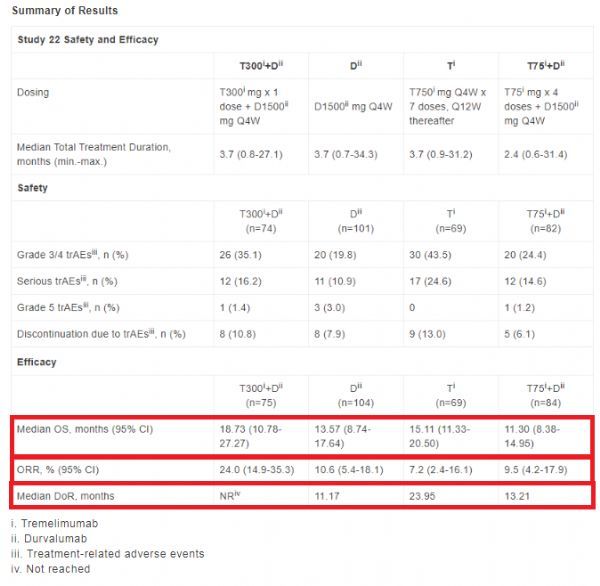
数据显示,这种贯续治疗方案的中位总生存期(OS)达到了18.7个月。这一数字远高于Imfinzi单药的13.6个月中位OS数据,也高于tremelimumab单药的15.1个月中位OS数据。而Imfinzi和tremelimumab联合用药方案(tremelimumab剂量为75mg,简称T75+D)在延长生存期方面表现最差,中位OS仅为11.3个月。
此外,高剂量的tremelimumab方案(简称T300+D)在缓解率方面也领先于其他方案,客观缓解率(ORR)达到了24%,中位缓解持续时间(DOR)尚未达到。而Imfinzi单药、tremelimumab单药、T75+D方案的ORR分别为10.6%、7.2%、9.5%。
在过去几年,很少看到tremelimumab能够改善一种治疗方案的效果。在2017年,tremelimumab与Imfinzi一线治疗非小细胞肺癌(NSCLC)III期MYSTIC试验失败,使得该组合无法进入利润丰厚的一线转移性NSCLC市场。之后,tremelimumab也在包括膀胱癌和小细胞肺癌等多个肿瘤适应症中遭遇失败。
阿斯利康肿瘤业务部执行副总裁兼全球负责人Dave Fredrickson指出,虽然将tremelimumab作为一种触发剂的治疗方法与我们在其他一些研究中采用的tremelimumab治疗方法不同,并且这项研究规模较小,但我们看到了非常好的疗效迹象。
目前,阿斯利康正在开展另一项一线治疗肝细胞癌III期HIMALAYA研究,预计今年下半年公布结果。该研究聚焦于先前未接受过治疗的患者身上,这一群体在过去多年来被证明难以治疗。在这项研究中,也采用了T300+D方案。Dave Fredrickson表示,来自II期研究的最新数据,为HIMALAYA研究提供了令人鼓舞的信号,希望这些结果能够得到复制。
如果HIMALAYA研究获得成功,阿斯利康将有机会在一线治疗肝细胞癌方面与罗氏展开直接竞争。上周五,罗氏的Tecentriq-Avastin组合疗法获得FDA批准,成为第一个一线治疗肝癌的癌症免疫治疗方案。另一方面,默沙东的Keytruda-Lenvima组合也已获得了FDA的突破性药物资格,并且在ASCO年会上公布了令人鼓舞的数据(ORR=36%)。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->