B细胞肿瘤靶向新药!PI3Kδ抑制剂ME-401获美国FDA快速通道资格,治疗3类肿瘤总缓解率75-100%
来源:本站原创 2020-04-03 11:31
2020年04月03日讯 /生物谷BIOON/ --MEI Pharma是一家处于后期临床阶段的生物制药公司,致力于开发用于癌症治疗的创新疗法。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其口服选择性磷脂酰肌醇-3-激酶δ(PI3Kδ)抑制剂ME-401快速通道资格(FTD),用于治疗已接受至少2种系统疗法的复发或难治性滤泡性淋巴瘤(R/R FL)

2020年04月03日讯 /生物谷BIOON/ --MEI Pharma是一家处于后期临床阶段的生物制药公司,致力于开发用于癌症治疗的创新疗法。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其口服选择性磷脂酰肌醇-3-激酶δ(PI3Kδ)抑制剂ME-401快速通道资格(FTD),用于治疗已接受至少2种系统疗法的复发或难治性滤泡性淋巴瘤(R/R FL)成人患者。
ME-401是一款在研口服磷脂酰肌醇3-激酶(PI3K)δ抑制剂。PI3Kδ抑制剂通常在癌细胞中过度表达,并在血液肿瘤的增殖及存活中起着关键作用。ME-401对PI3Kδ亚型呈现出很高的选择性,且与其他PI3Kδ抑制剂具有不同的药物特性,该药具有成为同类最佳(best-in-class)PI3Kδ抑制剂的潜力。其临床特征表明,作为一种单药疗法或与其他癌症药物联合用药,有机会解决一系列B细胞恶性肿瘤。目前,MEI公司正在评估ME-401治疗各种B细胞恶性肿瘤患者。
快速通道资格(FTD)旨在加速针对严重疾病的药物开发和快速审查,以解决关键领域严重未获满足的医疗需求。实验性药物获得快速通道资格,意味着药企在研发阶段可以与FDA进行更频繁的互动,在提交上市申请后如果符合相关标准则有资格进行加速审批和优先审查,此外也有资格进行滚动审查。
目前,MEI公司正在开展一项全球性II期TIDAL临床试验,评估ME-401作为单药疗法用于已接受过至少2种系统疗法(包括化疗和抗CD20抗体)治疗失败的R/R FL成人患者。该试验的结果,将用于支持向美国FDA申请加速批准ME-401上市。
除了TIDAL试验之外,MEI公司也正在开展一项多臂、开放标签、Ib期剂量递增和扩展试验,评估ME-401作为单药疗法、与其他疗法(如利妥昔单抗)或药物(如Brukinsa[zanubrutinib,泽布替尼],百济神州BTK抑制剂)联合用药,治疗复发或难治性B细胞恶性肿瘤,包括滤泡性淋巴瘤(FL)、慢性淋巴细胞白血病/小细胞淋巴瘤(CLL/SLL)、边缘区淋巴瘤(MZL)、套细胞淋巴瘤(MCL)、弥漫性大B细胞淋巴瘤(DLBCL)。
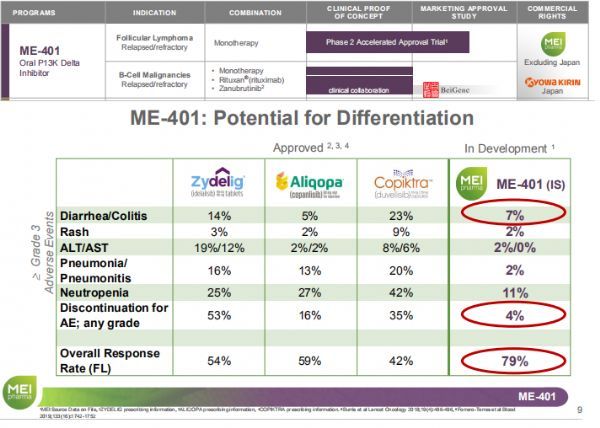
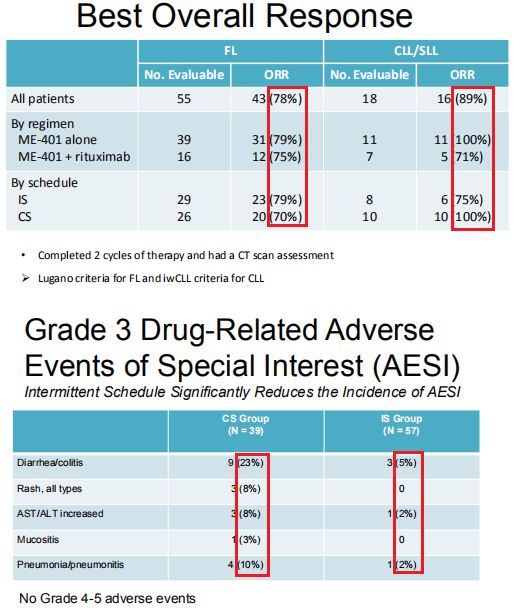
去年10月,MEI公司上公布了Ib期研究的更新数据。结果显示,接受ME-401治疗的所有患者组(FLL+CLL/SLL)的总缓解率(ORR)在75-100%,具体而言:(1)所有FL患者中ORR为78%(n=43/55)、ME-401单药治疗组ORR为79%、ME-401+利妥昔单抗联合治疗组ORR为75%。(2)所有CLL/SLL患者中ORR为89%(n=16/18)、ME-401单药治疗组ORR为100%、ME-401+利妥昔单抗联合治疗组ORR为71%。
该研究中,ME-401连续给药方案(CS)和间歇给药方案(IS)在FL和CLL/SLL患者中均表现出高缓解率和持久缓解,但IS方案组观察到的ME-401治疗相关3级不良事件的发生率比CS方案组较低。例如,3级腹泻/结肠炎发生率,IS方案组为5%,CS方案组为23%。
2018年11月,百济神州与MEI制药公司达成非独家临床合作,评估ME-401与Brukinsa联合治疗B细胞恶性肿瘤的潜力。目前,ME-401+Brukinsa联合治疗方案已被纳入上述多臂、开放标签Ib期研究,评估治疗FL、MCL、DLBCL的潜力。
Brukinsa(泽布替尼,zanubrutinib)是百济神州的一款BTK抑制剂,于2019年11月获得美国FDA加速批准,用于治疗既往接受过至少一项疗法的成年套细胞淋巴瘤(MCL)患者。特别值得一提的是,Brukinsa是首款由百济神州自主研发获批上市的产品,标志着该公司发展历程中的一个重大里程碑,同时也标志着第一款完全由中国企业自主研发、在美国FDA批准上市的抗癌新药,实现中国原研新药出海“零的突破”。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->