肿瘤免疫研究进展一览
来源:本站原创 2020-04-02 02:04
本期为大家带来的肿瘤免疫治疗领域的相关研究进展,希望读者朋友们能够喜欢。
2020年4月2日讯/生物谷BIOON/---本期为大家带来的肿瘤免疫治疗领域的相关研究进展,希望读者朋友们能够喜欢。


根据在内分泌学会年会上发表的一项新的研究,接受免疫检查点抑制剂治疗癌症后会出现更加普遍的甲状腺功能异常症状。
癌症免疫疗法,尤其是免疫检查点抑制剂的治疗手段,已成为治疗某些类型癌症的重要组成部分,并为特定群体患者提供了持续性的治疗效果。免疫检查点抑制剂作为靶向免疫系统的“刹车”的药物,有助于免疫系统识别和攻击癌细胞。目前,免疫检查点抑制剂被批准用于治疗某些患有多种癌症的患者,包括乳腺癌,膀胱癌,宫颈癌,结肠癌,头颈癌,肝癌,肺癌,皮肤癌,胃癌和直肠癌等等。
除了上述好处外,当免疫系统攻击正常的非癌细胞时,可能会产生一系列的副作用,包括与免疫有关的不良事件。其中,甲状腺水平异常,尤其是甲状腺功能减退(甲状腺功能低下)是一种较常见但轻度的副作用。
研究作者,加州大学圣迭戈分校的首席研究员Zoe Quandt称:“了解是什么引起了这些与免疫有关的不良事件,相关发生机制以及对治疗反应的影响,对于优化我们使用免疫检查点抑制剂具有重要意义。”
在该研究中,研究人员分析了加利福尼亚大学旧金山分校的电子健康记录数据,该数据涵盖了2012年至2018年期间接受免疫检查点抑制剂治疗癌症的每位患者。
他们排除了患有甲状腺癌的患者。对于其余的1,146位患者,他们筛选了患有某种甲状腺功能障碍的患者。在筛选得到的样本中,黑色素瘤是最常见的治疗癌症(32%),其次是非小细胞肺癌(13%)。
总体而言,暴露于免疫检查点抑制剂的患者中有19%出现甲状腺功能障碍。相比之下,对一项临床试验的审查发现,其发病率要低得多:6.6%的免疫检查点抑制剂患者出现甲状腺功能减退,而2.9%的患者甲状腺功能亢进或甲状腺功能亢进。
新研究发现,甲状腺疾病因癌症类型而异。甲状腺功能异常的发生率范围从脑肿瘤胶质母细胞瘤患者的10%到肾细胞癌的40%。尽管甲状腺功能不全和特定的免疫检查点抑制剂之间无显著相关性,但在接受nivolumab(Opdivo)和ipilimumab(Yervoy)联合使用(31%)的患者中,与任何单独药物治疗患者相比,甲状腺功能障碍更为常见。(pembrolizumab(Keytruda)(18%),nivolumab(18%)或ipilimumab(15%)。)
最后,PD-1+肿瘤ILC2和PD-1+ T细胞都存在于大多数人PDAC中。这些研究结果确定ILC2为一种用于PDAC免疫治疗的抗癌免疫细胞。更广泛地说,ILC2可增强组织特异性的抗癌免疫反应,可增强抗PD-1免疫疗法的功效。
DOI: 10.1084/jem.20191869
根据丹麦奥尔胡斯大学的研究人员最近发表的一项新研究,通过去除腹腔网膜脂肪组织中的巨噬细胞,有可能阻止卵巢癌的扩散并减少肿瘤的发生。
相关结果发表在最近的《Journal of experimental medicine》杂志上。

Anders Etzerodt是奥尔胡斯大学生物医学系癌症免疫学助理教授,也是这项研究的主要作者。他解释说,卵巢癌最常发生在输卵管中,但往往会脱落并且转移至腹腔。“我们的研究表明,当肿瘤细胞移入网膜脂肪时,这里的巨噬细胞会改变性状。从而支持疾病的发展。” Etzerodt说。
“存在于网膜脂肪组织中的一种巨噬细胞帮助肿瘤进一步扩散至腹腔中的其他器官。与此同时,第二种来自血液的巨噬细胞,被募集过来并且有助于抑制宿主杀伤肿瘤细胞的免疫反应。通过这种方式,有助于肿瘤的进一步生长。”
在这项研究中,研究人员最初尝试去除组织中已经发现的第一类巨噬细胞,他们发现,这一处理可以抑制癌症在腹腔中的扩散,尽管网膜脂肪中的肿瘤不会变小。当研究人员同时从血液中清除第二类巨噬细胞时,既减少了癌细胞的扩散,又使得肿瘤缩小。
“我们正在做的也是免疫疗法,但它专注于免疫系统的另一部分。我们的结果描述了不同来源的巨噬细胞如何影响肿瘤的发展,以及巨噬细胞如何抑制肿瘤的发生。
Etzerodt还解释说,他和他的同事使用单细胞测序发现了新型的巨噬细胞,该方法为研究人员提供了有关每个单个细胞发生过程的非常详细的信息。
doi:10.1126/scitranslmed.aav7431.

这些数据表明,PD-L1阻断可重新激活树突细胞的功能,从而产生强有效的抗癌T细胞免疫反应。
DOI: 10.1038/s43018-020-0038-2
免疫系统中的某些细胞,例如T淋巴细胞,能够攻击癌细胞,基于这一现象,增强免疫系统可以达到有效杀伤癌症的效果。2018年的诺贝尔生理学与医学奖便是授予了癌症的免疫疗法。
在他们的研究中,科学家还证明,成功渗入肿瘤的T淋巴细胞的数量与产生的细胞因子的数量有关,并决定了肿瘤细胞反应的程度。黑色素瘤患者细胞的研究支持了免疫细胞的这种远程作用模型。因此,刺激这种集体反应可能代表未来免疫治疗方法的关键目标。
肿瘤已经找到各种方法来防止免疫系统攻击它们。就医学本身而言,医学已经用癌症免疫疗法进行了反击。主要的方法是使用检查点抑制剂,这种药物可以帮助免疫系统识别外来癌细胞。另一种方法,CAR T细胞疗法,直接改造人们的T细胞来有效地识别癌细胞并杀死它们。
但并不是所有的患者都能从这些方法中受益,这些方法只适用于少数癌症类型,CAR T细胞疗法有很大的风险。波士顿儿童医院(Boston Children's Hospital) 3月11日在《Nature》杂志上发表的一项新研究,为这个"兵工厂"增加了另一种策略,这种策略有可能在更多类型的癌症中发挥作用。它能重新激活一种叫做gasdermin E的基因,利用我们已经有的免疫反应攻击癌细胞,但这种免疫反应在许多癌症中被抑制。
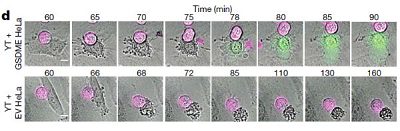
"Gasdermin E是一种非常有效的肿瘤抑制基因,但在大多数肿瘤组织中,它要么没有表达,要么发生了突变,"研究的通讯作者、细胞和分子医学项目(PCMM)的医学博士Judy Lieberman说道。"当你在肿瘤中重新激活gasdermin E时,它可以将一个免疫系统无法识别的'冷'肿瘤转变成一个免疫系统可以控制的'热'肿瘤。"
在这项研究中,Lieberman及其同事们发现他们测试的22种癌症相关突变中有20种导致了Gasdermin E功能的降低。当他们在小鼠模型中重新引入Gasdermin E时,他们能够触发癌细胞焦亡并抑制多种肿瘤的生长(三阴性乳腺肿瘤、结直肠肿瘤和黑色素瘤)。
该团队还在小鼠肿瘤细胞系中展示了Gasdermin E的工作原理。正常情况下,细胞死亡,包括大多数癌细胞,是通过一个叫做凋亡的过程发生的--一个安静的、程序性的死亡。但是如果Gasdermin E存在并起作用,癌细胞就会在炎症中倒下,通过一种叫做焦亡的高度炎症性细胞死亡形式。
正如Lieberman的研究小组在活老鼠身上发现的那样,细胞焦亡会发出一种强有力的免疫警报,它会招募杀伤T细胞来抑制肿瘤。该团队目前正在研究诱导Gasdermin E产生抗肿瘤免疫反应的治疗策略。
Lieberman说:"我们的建议是,如果我们能打开危险信号,也就是炎症,我们就能比使用其他免疫疗法更充分地激活淋巴细胞,从而获得可能更广泛的免疫。将肿瘤中的炎症激活与已批准的检查点抑制剂药物联合使用,可能比单独使用这两种方法效果更好。"
DOI: 10.3389/fphar.2020.00143
作者在《Frontiers in Pharmacology》杂志上发表的一篇文章中分享了这些发现。
加州大学医学院的教授Laura Conforti等人对从患有头颈癌的患者血液中提取的称为细胞毒性T细胞的白细胞进行了实验。研究结果发现,癌症患者免疫细胞中钙调蛋白的分子与离子通道(KCa3.1)之间的相互作用降低,这在细胞功能降低中起重要作用。
“细胞毒性T细胞就像我们免疫系统的士兵一样,是我们机体抵御癌性肿瘤的第一道防线,” Conforti实验室的第一作者Ameet Chimote说。 “这些具有细胞毒性的T细胞有望通过在肿瘤团块内迁移然后分泌细胞因子杀死这些肿瘤细胞而穿透实体瘤。然而,由于某些原因,这些细胞在癌症患者中不能正常发挥作用,它们不能穿透肿瘤并攻击肿瘤细胞,从而导致癌性肿瘤无法控制地生长。”
Conforti说:“识别这种潜在功能障碍的机制可以帮助我们识别可以用药物靶向的分子,并最终恢复这些细胞进入并杀死肿瘤的能力。在这项研究中,我们能够证明癌症患者T细胞中这些通道的功能降低,从而导致实体肿瘤中T细胞积累的减少。”
研究小组使用多种复杂的显微镜成像技术对从癌症患者血液中分离的T细胞进行了研究,发现与健康人的T细胞相比,癌症T细胞的膜中钙调蛋白分子更少。Conforti说:“这意味着钙调蛋白与癌症患者T细胞通道的结合能力下降。如果钙调蛋白不与之结合,则这些通道不起作用。因此,来自癌症患者的T细胞中钙调蛋白的结合减少导致功能降低,并导致肿瘤浸润和癌细胞杀伤减少。”
抗癌疗法令人沮丧的一点就是,目前并没有一种药物适合所有癌症患者,大多数药物都能对某些患者群体有效,但对相同类型癌症的其它患者似乎并没有治疗效果,近日,一篇发表在国际杂志Nature Communications上的研究报告中,来自魏茨曼科学研究所等机构的科学家们通过研究识别出了新型的标志物,其或能帮助预测哪些患者对免疫疗法能产生更为积极的反应。
该研究所识别出的两个亚单位及特殊的HLA结合肽类是否能够作为免疫治疗成功的预测因子呢?研究结果表明,在亚单位过量表达的肿瘤细胞中,能够直接靶向作用癌症的多种免疫系统组分或许更为普遍且活跃;实际上,当回顾了数据库中关于癌症患者的详细信息后,研究者表示,这两个亚单位的表达水平要比肿瘤突变负担能更好地预测患者的预后,而肿瘤突变是目前临床中使用的一种生物标志物;研究者表示,免疫蛋白酶体的表达或能作为一种生物标志物来更好地预测黑色素瘤患者的预后状况,当与突变负荷检测相结合时,或能改善患者与当前可用的免疫疗法之间的匹配程度。(生物谷 Bioon.com)


癌症免疫疗法,尤其是免疫检查点抑制剂的治疗手段,已成为治疗某些类型癌症的重要组成部分,并为特定群体患者提供了持续性的治疗效果。免疫检查点抑制剂作为靶向免疫系统的“刹车”的药物,有助于免疫系统识别和攻击癌细胞。目前,免疫检查点抑制剂被批准用于治疗某些患有多种癌症的患者,包括乳腺癌,膀胱癌,宫颈癌,结肠癌,头颈癌,肝癌,肺癌,皮肤癌,胃癌和直肠癌等等。
除了上述好处外,当免疫系统攻击正常的非癌细胞时,可能会产生一系列的副作用,包括与免疫有关的不良事件。其中,甲状腺水平异常,尤其是甲状腺功能减退(甲状腺功能低下)是一种较常见但轻度的副作用。
研究作者,加州大学圣迭戈分校的首席研究员Zoe Quandt称:“了解是什么引起了这些与免疫有关的不良事件,相关发生机制以及对治疗反应的影响,对于优化我们使用免疫检查点抑制剂具有重要意义。”
在该研究中,研究人员分析了加利福尼亚大学旧金山分校的电子健康记录数据,该数据涵盖了2012年至2018年期间接受免疫检查点抑制剂治疗癌症的每位患者。
他们排除了患有甲状腺癌的患者。对于其余的1,146位患者,他们筛选了患有某种甲状腺功能障碍的患者。在筛选得到的样本中,黑色素瘤是最常见的治疗癌症(32%),其次是非小细胞肺癌(13%)。
总体而言,暴露于免疫检查点抑制剂的患者中有19%出现甲状腺功能障碍。相比之下,对一项临床试验的审查发现,其发病率要低得多:6.6%的免疫检查点抑制剂患者出现甲状腺功能减退,而2.9%的患者甲状腺功能亢进或甲状腺功能亢进。
新研究发现,甲状腺疾病因癌症类型而异。甲状腺功能异常的发生率范围从脑肿瘤胶质母细胞瘤患者的10%到肾细胞癌的40%。尽管甲状腺功能不全和特定的免疫检查点抑制剂之间无显著相关性,但在接受nivolumab(Opdivo)和ipilimumab(Yervoy)联合使用(31%)的患者中,与任何单独药物治疗患者相比,甲状腺功能障碍更为常见。(pembrolizumab(Keytruda)(18%),nivolumab(18%)或ipilimumab(15%)。)
doi:10.1038/s41586-020-2015-4.

先天淋巴细胞(innate lymphoid cells, ILC),也被称作固有免疫细胞,是一类不同于T细胞和B细胞的淋巴细胞亚群,位于肠道粘膜表面中,增强免疫反应,维持粘膜完整性和促进淋巴器官形成。它们缺乏克隆性的抗原受体,在分化过程中也没有经历Rag基因的重排过程。在感染之后的数小时之内,ILC就能够活化产生保护性的效应。
根据细胞因子表达谱的不同,ILC能够分为三大类群:ILC1、ILC2和ILC3,其中ILC1类似于Th1,主要表达IFN-g,这类细胞主要针对胞内细菌与寄生虫感染;ILC2和与Th2类似,表达IL-5、IL-13等细胞因子,它们对于寄生虫感染以及过敏反应产生有效的保护措施;ILC3表达IL-17A与IL-22,它们参与了肠道的细菌感染反应。一旦遭受有害的应激,它们就会产生大量的细胞因子效应物。这些ILC在调节I型、2型和3型(或者说Th17细胞)免疫反应中发挥着至关重要的作用,这些免疫反应控制着宿主保护性免疫反应和肠道稳态。
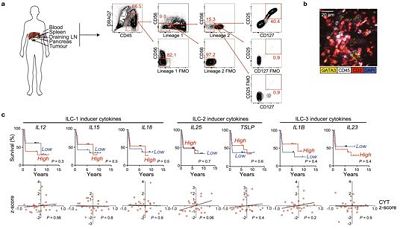
ILC2调节哺乳动物组织中的炎症和免疫力。尽管在这些组织的癌症中发现了ILC2,但是它们在抗癌免疫反应和免疫治疗中的作用尚不清楚。在一项新的研究中,来自美国纪念斯隆凯特琳癌症中心等研究机构的研究人员发现ILC2浸润到胰腺导管腺癌(PDAC)中以激活组织特异性的抗肿瘤免疫反应。白介素-33(IL33)激活小鼠原位胰腺肿瘤中的肿瘤ILC2和CD8+ T细胞,但不激活小鼠异位皮肤肿瘤中的肿瘤ILC2和CD8+ T细胞,从而抑制胰腺特异性的肿瘤生长。相关研究结果近期发表在Nature期刊上,论文标题为“ILC2s amplify PD-1 blockade by activating tissue-specific cancer immunity”。
静止和活化的肿瘤ILC2表达抑制性检查点受体PD-1。抗体介导的PD-1阻断可减轻ILC2细胞固有的PD-1抑制,从而使得肿瘤ILC2扩大、增加抗肿瘤免疫力并增强肿瘤控制,因此这将活化的肿瘤ILC2确定为抗PD-1免疫疗法的靶标。
鉴于ILC2和T细胞共存于人类癌症中,并具有相同的刺激途径和抑制途径,因此共同靶向抗癌ILC2和T细胞的免疫治疗策略可能具有广泛的应用价值。
根据丹麦奥尔胡斯大学的研究人员最近发表的一项新研究,通过去除腹腔网膜脂肪组织中的巨噬细胞,有可能阻止卵巢癌的扩散并减少肿瘤的发生。
相关结果发表在最近的《Journal of experimental medicine》杂志上。

“存在于网膜脂肪组织中的一种巨噬细胞帮助肿瘤进一步扩散至腹腔中的其他器官。与此同时,第二种来自血液的巨噬细胞,被募集过来并且有助于抑制宿主杀伤肿瘤细胞的免疫反应。通过这种方式,有助于肿瘤的进一步生长。”
在这项研究中,研究人员最初尝试去除组织中已经发现的第一类巨噬细胞,他们发现,这一处理可以抑制癌症在腹腔中的扩散,尽管网膜脂肪中的肿瘤不会变小。当研究人员同时从血液中清除第二类巨噬细胞时,既减少了癌细胞的扩散,又使得肿瘤缩小。
“我们正在做的也是免疫疗法,但它专注于免疫系统的另一部分。我们的结果描述了不同来源的巨噬细胞如何影响肿瘤的发展,以及巨噬细胞如何抑制肿瘤的发生。
Etzerodt还解释说,他和他的同事使用单细胞测序发现了新型的巨噬细胞,该方法为研究人员提供了有关每个单个细胞发生过程的非常详细的信息。

在正常情况下,为了阻止活化的T细胞破坏正常的人体细胞,免疫系统能够通过激活PD-1/PD-L1等免疫检查点来控制T细胞的活化进程,防止T细胞错误地攻击正常的细胞。然而,癌细胞通过表达表面蛋白PD-L1特异性地识别T细胞表面上的PD-1,窃取这种控制机制,从而激活免疫检查点来抑制T细胞的免疫活性,这就会导致癌细胞逃避免疫识别和茁壮生长,如图2所示。这就为癌症治疗开创了全新的免疫治疗思路——通过免疫检查点抑制剂阻断CTLA-4或PD-1等免疫检查点,阻止癌细胞窃取这种控制机制,从而释放免疫系统自身的能力来攻击癌症。
免疫检查点抑制剂治疗通过抑制免疫检查点活性,释放肿瘤微环境中的免疫刹车,重新激活T 细胞对肿瘤的免疫应答效应,从而达到抗肿瘤的作用。PD-1的天然配体有两个,分别为PD-L1和PD-L2。目前研究和应用最广泛的免疫检查点抑制剂之一就是PD-1/PD-L1 的抑制剂。
目前,实际上只有约20%~40%的患者能够从PD-1/PD-L1抑制剂治疗中获益,两个重要因素是免疫抑制性的肿瘤微环境中缺乏肿瘤特异性T细胞和T细胞经历功能性耗竭。
尽管PD-1/PD-L1阻断抗体已被证实可治疗多种人类癌症,但是它们仅能够增强一部分癌症患者的抗肿瘤免疫力,因此要将这种治疗益处扩展给更多的患者,将需要更好地了解这类疗法如何引发抗癌免疫力。
尽管PD-1/PD-L1轴通常与T细胞功能相关,但是在一项新的研究中,瑞士苏黎世罗氏创新中心、巴塞尔罗氏创新中心、德国慕尼黑罗氏创新中心、荷兰莱顿大学医疗中心和美国基因泰克公司的研究人员描述了树突细胞表面上的各种配体,并证实树突细胞(DC)是PD-L1阻断抗体的一个重要靶标。PD-L1结合两个受体:PD-1和B7.1(CD80)。在癌症患者的外周血树突细胞和肿瘤相关树突细胞表面上,PD-L1比B7.1更丰富地表达。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“Dendritic cells dictate responses to PD-L1 blockade cancer immunotherapy”。
树突细胞表面上的PD-L1可以与同一细胞表面上的B7.1结合,从而有可能阻止T细胞表面上的PD-1与PD-L1的结合或T细胞表面上的CD28与B7.1的结合。
阻断树突细胞表面上的PD-L1可以减轻PD-L1对B7.1的隔离作用,从而使得B7.1/CD28的相互作用增强T细胞的激活。与这一点相一致的是,在接受阿特珠单抗(atezolizumab , 一种PD-L1阻断抗体)治疗的肾细胞癌或非小细胞肺癌患者中,具有较高树突细胞基因标签的患者更可能对PD-L1阻断作出反应,即较高的树突细胞基因标签与改善的总生存率密切相关。
免疫系统如何限制肿瘤的发展?近日,来自巴斯德研究所(Institut Pasteur)和英瑟姆研究所(Inserm)的科学家使用体内成像工具描述了局部和远处肿瘤浸润性T淋巴细胞的时空活动特征。他们的研究发表在最近的《Nature Cancer》杂志上。

然而,T淋巴细胞在肿瘤中的作用到底如何? T淋巴细胞是杀伤细胞,能够通过直接接触浸润肿瘤并破坏癌细胞。癌细胞的这种破坏是高度局部的现象,仅发生在杀伤细胞的附近。但是在这些接触过程中,T淋巴细胞也会产生称为细胞因子的可溶性分子。巴斯德研究所(Institut Pasteur and Inserm)的科学家着手了解这些细胞因子之一,即干扰素-γ(IFN-γ)对肿瘤微环境的影响。
他们使用了功能强大的成像技术,可以在小鼠中实时和体内观察T淋巴细胞的行为以及肿瘤内IFN-γ的作用。科学家观察到,细胞因子不仅仅在局部起作用,而是在肿瘤内迅速扩散,并影响可能与T细胞距离较远的癌细胞。主要作者Philippe Bousso解释说:“这种在肿瘤内的远程作用非常有趣,因为它使T淋巴细胞能够作用于大量癌细胞,尤其是那些可能具有逃避免疫系统机制的癌细胞。
DOI: 10.1038/s41586-020-2071-9
但并不是所有的患者都能从这些方法中受益,这些方法只适用于少数癌症类型,CAR T细胞疗法有很大的风险。波士顿儿童医院(Boston Children's Hospital) 3月11日在《Nature》杂志上发表的一项新研究,为这个"兵工厂"增加了另一种策略,这种策略有可能在更多类型的癌症中发挥作用。它能重新激活一种叫做gasdermin E的基因,利用我们已经有的免疫反应攻击癌细胞,但这种免疫反应在许多癌症中被抑制。

在这项研究中,Lieberman及其同事们发现他们测试的22种癌症相关突变中有20种导致了Gasdermin E功能的降低。当他们在小鼠模型中重新引入Gasdermin E时,他们能够触发癌细胞焦亡并抑制多种肿瘤的生长(三阴性乳腺肿瘤、结直肠肿瘤和黑色素瘤)。
提高免疫反应
正如Lieberman的研究小组在活老鼠身上发现的那样,细胞焦亡会发出一种强有力的免疫警报,它会招募杀伤T细胞来抑制肿瘤。该团队目前正在研究诱导Gasdermin E产生抗肿瘤免疫反应的治疗策略。
Lieberman说:"我们的建议是,如果我们能打开危险信号,也就是炎症,我们就能比使用其他免疫疗法更充分地激活淋巴细胞,从而获得可能更广泛的免疫。将肿瘤中的炎症激活与已批准的检查点抑制剂药物联合使用,可能比单独使用这两种方法效果更好。"
加州大学的研究人员发现了一个新型的机制,该机制可以解释癌症患者免疫功能下降的原因,并可能成为头颈癌患者免疫治疗的新靶标。

作者在《Frontiers in Pharmacology》杂志上发表的一篇文章中分享了这些发现。
加州大学医学院的教授Laura Conforti等人对从患有头颈癌的患者血液中提取的称为细胞毒性T细胞的白细胞进行了实验。研究结果发现,癌症患者免疫细胞中钙调蛋白的分子与离子通道(KCa3.1)之间的相互作用降低,这在细胞功能降低中起重要作用。
“细胞毒性T细胞就像我们免疫系统的士兵一样,是我们机体抵御癌性肿瘤的第一道防线,” Conforti实验室的第一作者Ameet Chimote说。 “这些具有细胞毒性的T细胞有望通过在肿瘤团块内迁移然后分泌细胞因子杀死这些肿瘤细胞而穿透实体瘤。然而,由于某些原因,这些细胞在癌症患者中不能正常发挥作用,它们不能穿透肿瘤并攻击肿瘤细胞,从而导致癌性肿瘤无法控制地生长。”
Conforti说:“识别这种潜在功能障碍的机制可以帮助我们识别可以用药物靶向的分子,并最终恢复这些细胞进入并杀死肿瘤的能力。在这项研究中,我们能够证明癌症患者T细胞中这些通道的功能降低,从而导致实体肿瘤中T细胞积累的减少。”
研究小组使用多种复杂的显微镜成像技术对从癌症患者血液中分离的T细胞进行了研究,发现与健康人的T细胞相比,癌症T细胞的膜中钙调蛋白分子更少。Conforti说:“这意味着钙调蛋白与癌症患者T细胞通道的结合能力下降。如果钙调蛋白不与之结合,则这些通道不起作用。因此,来自癌症患者的T细胞中钙调蛋白的结合减少导致功能降低,并导致肿瘤浸润和癌细胞杀伤减少。”
doi:10.1038/s41467-020-14639-9
研究者表示,学习预测哪种疗法最有可能发挥作用或许是开发个体化疗法来治疗癌症的第一步,文章中,研究人员重点对黑色素瘤进行研究,黑色素瘤是一种难以治疗的皮肤癌,其包含了携带数百种不同突变的肿瘤细胞,近些年来,研究人员能利用名为检查点抑制剂的免疫疗法成功治疗特定比例的黑色素瘤患者,检查点抑制剂能通过移除阻碍宿主自身免疫系统的内部障碍来发挥作用,从而有效抵御黑色素瘤,但很不幸的是,对于其它黑色素瘤患者而言,这些药物并没有什么效果。

为了理解不同人群对疗法产生反应的差异,研究人员首先对来自“癌症基因组图谱”计划中的470名黑色素瘤患者的数据进行分析,他们尤其感兴趣“免疫蛋白酶体”过表达的特定亚群患者与低表达的亚群患者在生存率上的差异,蛋白酶体亚单位的变异通常会在大多数细胞中进行表达(免疫细胞除外),蛋白酶体是一种蛋白质复合体,其扮演着“切割器”的角色,能将长蛋白切割为短肽,随后这些肽类会被HLA(人类白细胞抗原,human leucocyte antigens)分子呈现在细胞表面,HLA肽类基本上是展现在细胞外部的小分子信息,其能够报告新的威胁来让免疫系统进行评估和应对。
免疫蛋白酶体由改变的亚单位组装而成,从而就能产生特殊的HLA肽类集,研究者认为,HLA肽类库的特殊改变和过量表达可能会通过免疫系统更好地识别肿瘤细胞,从而更好的消灭癌细胞。为了检测这一观点,研究人员对来自黑色素瘤患者机体的肿瘤细胞系进行培养,这些细胞能够过量表达免疫蛋白酶体亚单位,同时还能在每种情况下识别HLA肽类,通过对来自相同患者的免疫细胞的反应进行检测,研究者发现,相比没有过量表达的细胞所呈现HLA肽类而言,新形成的HLA肽类的确更具有反应性。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


