重磅!辉瑞Vyndaqel(tafamidis)欧盟获批,转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)治疗药物!
来源:本站原创 2020-02-19 13:10
2020年02月19日讯 /生物谷BIOON/ --辉瑞(Pfizer)近日宣布,欧盟委员会(EC)已批准Vyndaqel(tafamidis),该药是一种每日一次的61mg口服胶囊,用于治疗野生型或遗传型转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)成人患者。值得一提的是,Vyndaqel是首个也是唯一一个在欧盟被批准治疗ATTR-CM的药物。

2020年02月19日讯 /生物谷BIOON/ --辉瑞(Pfizer)近日宣布,欧盟委员会(EC)已批准Vyndaqel(tafamidis),该药是一种每日一次的61mg口服胶囊,用于治疗野生型或遗传型转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)成人患者。在此次批准之前,ATTR-CM患者的治疗方案仅限于症状管理,在少数情况下,还包括心脏(或心脏和肝脏)移植。ATTR-CM是一种罕见的危及生命的疾病,其特征是在心脏中积聚一种称为淀粉样蛋白的错误折叠蛋白,其定义为限制性心肌病和进行性心力衰竭。平均而言,患者在确诊后只能存活2-3.5年。
2011年,欧盟批准了一种不同类型的Vyndaqel(tafamidis meglomene)20mg胶囊,用于治疗1期症状性多发性神经病成人患者的转甲状腺素蛋白淀粉样变性(ATTR-PN),以延缓周围神经功能损害。对于ATTR-CM,tafamidis 61mg胶囊相当于80mg的tafamidis meglomene剂量(4片20mg胶囊),是为了方便患者而开发的一种胶囊,以便每日服用一粒。这2款药物具有相同的活性成分tafamidis,但由于推荐剂量不同,不可相互替代。
值得一提的是,Vyndaqel是首个也是唯一一个在欧盟被批准治疗ATTR-CM的药物、唯一一个被证明可降低野生型或遗传型ATTR-CM患者死亡率和心血管相关住院率的药物。在欧盟,Vyndaqel也是首个可同时治疗ATTR-CM和1期症状性转甲状腺素蛋白淀粉样变性多发性神经病(ATTR-PN)的药物。
在美国,Vyndaqel(tafamidis meglumine)和Vyndamax(tafamidis)2019年5月初获得FDA批准,成为首个也是唯一一个治疗ATTR-CM的药物。2款药物是首创的(first-in-class)转甲状腺素蛋白(transthyretin)稳定剂tafamidis的两种口服制剂。
辉瑞罕见病全球总裁Paul Levesque表示:“此前,欧盟还没有批准的药物用来治疗ATTR-CM患者。今天的批准,对这些患者来说是一个重大里程碑,反映了我们向罕见病患者提供突破性药物的坚定承诺。此外,随着今天的里程碑,Vyndaqel现在是欧盟批准的第一个有2种配方治疗转甲状腺素蛋白淀粉样变性表现的药物:一种用于心肌病,一种用于1期多发性神经病。”
法国心脏病学会心力衰竭和心肌病组织前任主席、法国心脏淀粉样变性转诊中心协调员Thibaud Damy表示:“在今天之前,欧洲转甲状腺素蛋白淀粉样变性共同体迫切需要新的治疗方案,以改善心肌病患者的预后。Vyndaqel对患者来说是一个重大进步,因为它可以显著降低野生型或遗传型ATTR-CM患者的全因死亡率和心血管相关住院频率。”
欧盟委员会批准Vyndaqel,基于关键性III期临床研究ATTR-ACT的数据,这是调查一种ATTR-CM药理学疗法方面第一个也是唯一一个成功完成的全球性、双盲、随机、安慰剂对照临床试验。该研究共入组了441例患者,包括变异型或遗传型ATTR-CM患者,以及野生型ATTR-CM患者(指不是遗传的,而是可能随年龄增长而发生的)。
主要分析结果显示,在30个月治疗期间:(1)与安慰剂相比,Vyndaqel(tafamidis meglomene)显著降低了野生型和遗传型ATTR-CM患者的全因死亡和心血管相关住院率(p=0.0006)。(2)与安慰剂组相比,Vyndaqel将全因死亡率和全因住院率分别降低30%(p=0.026)和32%(p<0.0001)。(3)与安慰剂相比,Vyndaqel降低了所有亚组(野生型,遗传型,NYHA-I、-II、-III功能分级)的全因死亡风险:野生型亚组(HR=0.71,95%CI:0.474-1.052)和遗传型亚组(HR=0.69,95%CI:0.408-1.167)中死亡风险分别降低29%和31%。(4)横跨野生型和遗传型亚组,与安慰剂相比,Vyndaqel使6分钟步行试验(6MWT)评价的患者活动能力和堪萨斯城心肌病问卷(KCCQ)评价的患者生活质量各个方面的降低表现出一致的减少。(5)研究中,Vyndaqel的耐受性良好,并与安慰剂具有可比的安全性。
该批准还基于来自游离酸类型的tafamidis 61mg的一项评估结果。该评估结果表明,一粒61mg的tafamidis游离酸胶囊相当于80mg剂量tafamidis meglomene(4粒20mg胶囊)。在ATTR-ACT中未评估61mg剂量的安全性。tafamidis 61mg胶囊是为了方便患者使用而研制的,可用于日常服用。
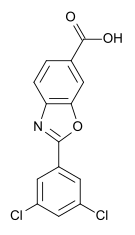
tafamidis分子结构(来自维基百科)
ATTR淀粉样变性是一种罕见的进行性疾病,其特征是由错误折叠的转甲状腺素蛋白组成的淀粉样沉积在人体器官和组织中的异常堆积。淀粉样变性可影响身体的许多器官和组织,包括外周神经系统,以及心脏、肾脏、胃肠道和眼睛等器官。ATTR-CM和ATTR-PN是该病的两种表现。
ATTR-CM是一种罕见的、致命的、严重诊断不足的疾病,与渐进性心力衰竭相关。ATTR-CM是由名为转甲状腺素蛋白(TTR)的转运蛋白不稳定而引起的,该转运蛋白由4个相同的亚单元(四聚体)组成。在ATTR-CM中,不稳定的四聚体解离时发生心力衰竭,导致错误折叠的蛋白质聚集成淀粉样纤维并主要沉积在心脏中。
tafamidis是一种口服小分子药物,可稳定TTR。在美国和欧盟,tafamidis于2011年被授予治疗ATTR-CM的孤儿药资格。在2017年,FDA还授予了tafamidis快速通道地位;2018年3月,日本卫生劳动福利部(MHLW)授予tafamidis SAKIGAKE资格;2018年5月,FDA授予了tafamidis突破性药物资格。(生物谷Bioon.com)
原文出处:European Commission approves VYNDAQEL®, the First Treatment in the EU for Transthyretin Amyloid Cardiomyopathy (ATTR-CM)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


