国产新型激酶抑制剂!和黄医药索凡替尼获美国FDA孤儿药资格认定,治疗胰腺神经内分泌瘤!
来源:本站原创 2019-11-29 19:00
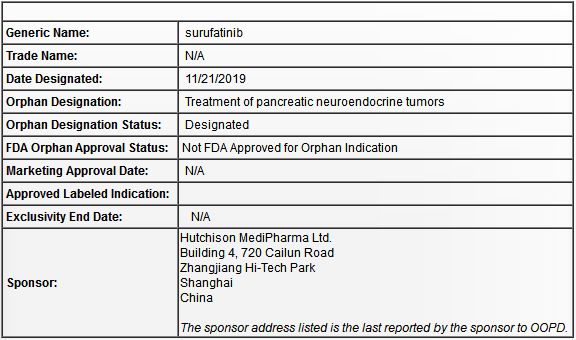
2019年11月29日讯 /生物谷BIOON/ --和黄中国医药科技有限公司(Chi-Med,简称“和黄医药”)近日宣布,美国食品和药物管理局(FDA)已授予新型口服酪氨酸激酶抑制剂索凡替尼(surufatinib,前称HMPL-012或sulfatinib)治疗胰腺神经内分泌肿瘤(NET)的孤儿药资格(ODD)。孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又

2019年11月29日讯 /生物谷BIOON/ --和黄中国医药科技有限公司(Chi-Med,简称“和黄医药”)近日宣布,美国食品和药物管理局(FDA)已授予新型口服酪氨酸激酶抑制剂索凡替尼(surufatinib,前称HMPL-012或sulfatinib)治疗胰腺神经内分泌肿瘤(NET)的孤儿药资格(ODD)。
孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物上市后针对所批准适应症为期7年的市场独占期。
和黄医药首席执行官贺隽(Christian Hogg)表示:“目前神经内分泌肿瘤的治疗中仍存在许多尚未满足的需求。现时的治疗方法非常有限。此次获得FDA授予孤儿药资格认定,对患者来说是积极的一步,并进一步强调了我们研发工作的重要性,以将索凡替尼带给更多有需要的患者。”
索凡替尼(surufatinib)是由和黄医药自主研发的一种新型的口服酪氨酸激酶抑制剂,具有抗血管生成和免疫调节双重活性。索凡替尼可通过抑制血管内皮生长因子受体(VEGFR)和成纤维细胞生长因子受体(FGFR)以阻断肿瘤血管生成,并可抑制集落刺激因子-1受体(CSF-1R),通过调节肿瘤相关巨噬细胞,促进机体对肿瘤细胞的免疫应答。因为具有抗肿瘤血管生成和免疫调节的双重机制,索凡替尼可能非常适合与其他免疫疗法联合使用。目前,索凡替尼正在中国及美国作为单药治疗或与其他肿瘤免疫疗法联合治疗开展针对多种实体瘤的研究。和黄医药目前拥有索凡替尼在全球范围内的所有权利。
索凡替尼是和黄医药第二款自主研发并成功完成III期临床试验的创新肿瘤药物。索凡替尼用于晚期非胰腺NET的新药上市申请(NDA)已提交,并于2019年11月11日获中国国家药品监督管理局(NMPA)受理。目前,晚期非胰腺NET尚无有效治疗方法。
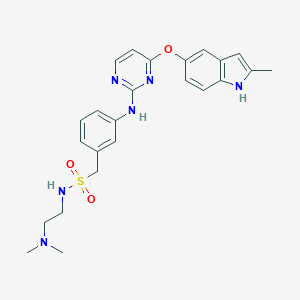
surufatinib分子结构式(图片来源:pubchem)
此次NDA基于成功完成的关键III期临床研究SANET-ep(NCT02588170)的阳性数据。这是一项随机、双盲、安慰剂对照、多中心的III期研究,在没有有效治疗方法的中低级别晚期非胰腺NET患者中开展,评估了每日口服索凡替尼与安慰剂的疗效和安全性。该研究的阳性结果已在2019年9月29日举行的欧洲肿瘤内科学会(ESMO)年会上以口头报告的形式公布。
数据显示,与安慰剂相比,索凡替尼将疾病进展或死亡风险显著降低67%。根据研究者评估,索凡替尼治疗组患者的中位无进展生存期(PFS)为9.2个月,安慰剂组患者为3.8个月(HR=0.334;95%CI:0.223-0.499;p<0.0001)。在所有亚组中均观察到了索凡替尼的治疗疗效,并且这些治疗疗效得到了包括客观缓解率(ORR)、疾病控制率(DCR)、到达疾病缓解的时间(TTR)、缓解持续时间(DoR)等次要疗效终点指标的显著改善的统计数据的支持。经评估后,这些治疗疗效还得到了盲态独立影像学审查委员会(BIIRC)的支持。总生存率(“OS”)数据尚不成熟 ,截至数据截止日的OS事件仅佔18.7%。该研究中,索凡替尼在总体上耐受性良好,且安全性特征与既往临床试验中的观察结果保持一致。(生物谷Bioon.com)
原文出处:Chi-Med Announces Surufatinib Granted FDA Orphan Drug Designation for Pancreatic Neuroendocrine Tumors
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


