新适应症!STELARA®获批治疗成年溃疡性结肠炎
来源:本站原创 2019-10-22 00:52
强生旗下的杨森制药今天宣布其产品STELARA®(ustekinumab)获得FDA批准用于治疗患有中度至重度活动性溃疡性结肠炎的成年患者。 溃疡性结肠炎是一种严重,慢性和进行性大肠免疫介导的炎症性疾病,在美国影响了大约910,000人。 STELARA是针对溃疡性结肠炎的首个也是唯一获得批准的针对白介素(IL)-12和IL-23细胞因子的生物疗法。 已经证明I
强生旗下的杨森制药今天宣布其产品STELARA®(ustekinumab)获得FDA批准用于治疗患有中度至重度活动性溃疡性结肠炎的成年患者。
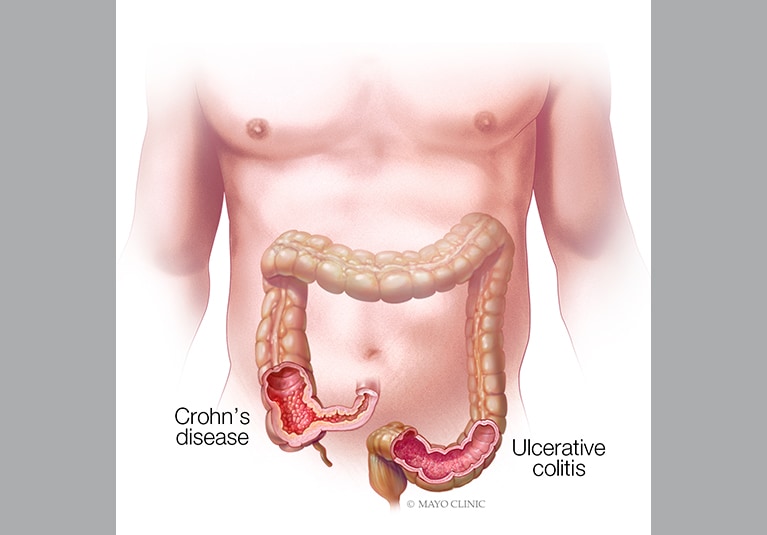
溃疡性结肠炎是一种严重,慢性和进行性大肠免疫介导的炎症性疾病,在美国影响了大约910,000人。 STELARA是针对溃疡性结肠炎的首个也是唯一获得批准的针对白介素(IL)-12和IL-23细胞因子的生物疗法。 已经证明IL-12和IL-23细胞因子在炎性和免疫应答中起重要作用。
关键性试验包括一项初始诱导研究(UNIFI-I),其中患者接受单剂量STELARA 6 mg/kg静脉内(IV)输注。 8周后进行了一项维持性研究(UNIFI-M),其中患者每8周接受STELARA 90 mg皮下(SC)注射,持续44周。两项研究均证明了STELARA作为中度至重度活动性溃疡性结肠炎患者的治疗中的安全性和有效性,该设计和完整结果最近发表在《新英格兰医学杂志》上。
在归纳研究中,接受STELARA的患者中有19%在短短8周内达到了临床缓解。此外,STELARA为患者提供了快速缓解的症状,因为接受STELARA的患者中有58%在第8周经历了临床反应。
在维持性研究中,接受STELARA的患者中有45%的患者在一年后缓解。 STELARA还帮助患者无需使用皮质类固醇即可实现临床缓解。一年后,接受STELARA治疗的患者中有43%处于临床缓解期,未接受类固醇治疗。

自2009年9月获得治疗中度至重度斑块状牛皮癣成人的批准以来,STELARA已获得其他四个适应症的批准:青少年中度至重度斑块状牛皮癣,成年活动性银屑病关节炎,成年中度至重度活动的克罗恩氏病(CD),现在可用于成年中度至重度活动性溃疡性结肠炎。(生物谷/bioon.com)
原文出处:杨森官网
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



