肠道微生物组研究进展(第6期)
来源:本站原创 2019-08-31 07:50
2019年8月30日讯/生物谷BIOON/---肠道是人体最大的消化和排毒器官,其回旋盘转的结构被形象地称为人体第二大脑。肠道中寄生着数以计亿的细菌,它们是人体内最重要的一种外环境,各种微生物按一定比例组合,相互制约,相互依存,在质和量上形成一种生态平衡。然而肠道菌群并不都是人类的朋友,按特性来讲,它们可分为3大类,即好菌、坏菌和中性菌。当人体肠道中好菌比例下降而坏菌数量上升时,人体免疫力下降,极
2019年8月30日讯/生物谷BIOON/---肠道是人体最大的消化和排毒器官,其回旋盘转的结构被形象地称为人体第二大脑。肠道中寄生着数以计亿的细菌,它们是人体内最重要的一种外环境,各种微生物按一定比例组合,相互制约,相互依存,在质和量上形成一种生态平衡。然而肠道菌群并不都是人类的朋友,按特性来讲,它们可分为3大类,即好菌、坏菌和中性菌。当人体肠道中好菌比例下降而坏菌数量上升时,人体免疫力下降,极易导致多种疾病的发生。
研究表明,肠道菌群紊乱与多种疾病的发生密切相关,如消化系统疾病、内分泌系统疾病、精神系统疾病、自身免疫性疾病以及一些感染性疾病。基于此,小编针对肠道微生物组最新研究进展,进行一番梳理,以飨读者。
1.Cell Rep:肠道微生物可以保护小鼠免受流感病毒感染
doi:10.1016/j.celrep.2019.05.105
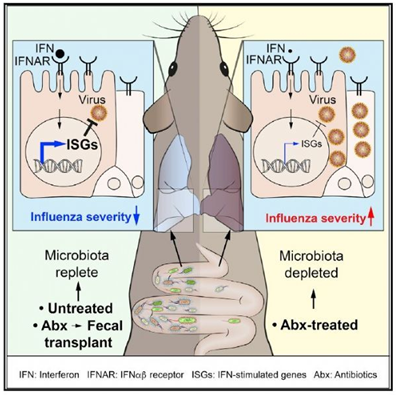
研究人员近日在《Cell Reports》杂志上发表报告称,肠道微生物刺激非免疫肺细胞中的抗病毒信号,以在感染初期抵御流感病毒。增强的基线I型干扰素(IFNα/β)信号驱动了抗病毒反应,减少了小鼠流感病毒复制和体重减轻,但随着抗生素治疗这种保护作用会减弱。
"这项研究支持了以下观点:服用抗生素不当不仅会促进抗生素耐药性、消除有用的保护性益生菌,还可能使你更容易受到病毒感染。"来自英国弗朗西斯·克里克研究所的该研究通讯作者Andreas Wack说道。"在一些国家,畜牧业大量使用抗生素,用于预防感染,因此接受治疗的动物可能更容易受到病毒感染。"
Wack和他的团队利用由于突变增加IFNα/β受体的表达水平的小鼠进行了研究,这些小鼠的基线IFNα/β信号升高了。这些小鼠对流感病毒感染更有抵抗力,体重减轻较少,感染8小时后病毒基因表达降低,两天后流感病毒复制减少。鉴于病毒载量控制较早,因此随后IFNα/β信号和抗病毒免疫反应没有完全启动。结果表明,调节IFNα/β受体的表达水平可以精准调控肺部的IFNα/β信号。基线IFNα/β信号增强的保护作用在抗生素治疗2-4周后降低了,主要在肺间质细胞的IFNα/β信号降低了--这是一群组成结构组织器官的非免疫细胞。相反,粪便移植逆转了抗生素引起的对流感病毒感染的易感性,这表明肠道微生物可能发挥了作用。
总的来说,结果表明微生物群增加了肺间质细胞的IFNα/β信号,从而提高了抵御流感病毒感染的能力。这项新发现与之前的研究结果一致,之前的研究表明,口服抗生素治疗的小鼠更容易感染病毒,包括甲型流感病毒。
2.Science子刊:肠道微生物群影响小鼠骨骼肌的质量和功能
doi:10.1126/scitranslmed.aan5662
一个国际研究小组发现,小鼠肠道微生物群在骨骼肌质量维持和功能方面发挥着重要作用。在发表于《Science Translational Medicine》杂志上的论文中,该小组描述了他们在野生和实验室饲养的小鼠上的实验,以及他们的最新发现。
在过去的几年里,科学家们发现人类和其他动物的肠道微生物群在维持健康方面所起的作用比之前认为的要大得多。除了加工食物,肠道微生物群在免疫和调节胆固醇和甘油三酯方面发挥着重要作用。肠道微生物群失衡与克罗恩病、肠易激综合征和其他炎症性疾病有关。现在,从事这项新工作的研究人员发现了新证据,表明肠道微生物群在维持适量的骨骼肌及其功能方面也发挥着作用--至少在老鼠身上是这样。
为了进一步了解微生物群对骨骼肌质量的可能影响,研究人员获得了几只野生小鼠,并将它们的微生物群与无菌小鼠(完全没有微生物群的小鼠)进行了比较。与野生小鼠相比,无菌小鼠骨骼肌萎缩。它们表达的支持肌肉生长的化学物质更少。研究人员发现,缺乏微生物组的老鼠体内的多种氨基酸水平高于正常水平,这是肝脏问题的迹象。他们还发现,老鼠体内的乙酰胆碱前体水平较低。乙酰胆碱是一种神经递质,参与骨骼肌和神经之间的信号传输。
研究人员还发现,将含有野生小鼠肠道微生物的物质移植到无菌小鼠的肠道中,可以增加肌肉质量和功能。他们发现,给予无菌小鼠肠道微生物正常产生的脂肪酸,也能部分恢复肌肉质量。
3.Science重大突破:肠道细菌竟然可以预防肥胖!
doi:10.1126/science.aat9351
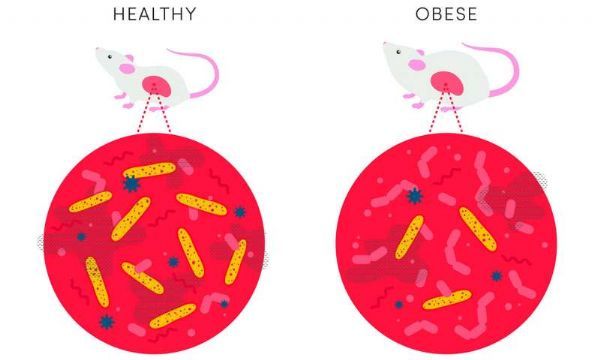
犹他大学健康学院的研究人员发现,肠道中有一种特定的细菌可以防止老鼠变胖,这表明这些细菌也可以控制人类的体重。这种有益的细菌被称为梭状芽孢杆菌(Clostridia),是微生物群落的一部分--肠道内共有数万亿的细菌和其他微生物。
近日发表在《Science》杂志上的这项研究表明,健康的老鼠体内有大量梭状芽孢杆菌(一种由20到30种细菌组成的细菌),但那些免疫系统受损的老鼠随着年龄的增长会失去这些微生物。即使喂食健康的食物,老鼠也不可避免地会变胖。把这类微生物还给这些动物可以让它们保持苗条。
这项研究的结果已经指向这个方向。Petersen和他的同事发现梭状芽孢杆菌通过阻断肠道吸收脂肪的能力来防止体重增加。实验中,梭状芽孢杆菌是小鼠肠道中唯一的细菌,与完全没有微生物群的小鼠相比,梭状芽孢杆菌的小鼠更瘦,脂肪更少。他们还拥有较低水平的CD36基因,该基因控制着身体对脂肪酸的吸收。
Round说,这些发现可能会导致一种治疗方法,它比粪便移植和益生菌更有优势--目前正被广泛研究作为恢复健康微生物群的方法。基于将活菌群转移到肠道的治疗方法并不适用于所有人,因为不同的饮食和其他因素会影响哪些细菌能够存活和繁殖。
4.Cell:震惊!肿瘤微生物组竟能决定癌症患者的生死
doi:10.1016/j.cell.2019.07.008
在一项新的研究中,来自美国德克萨斯大学MD安德森癌症研究中心的研究人员发现少数长期存活的胰腺癌患者与许多对所有治疗方案都无效的胰腺癌患者之间的一个关键区别在于他们的肿瘤中的细菌群落刺激或抑制免疫反应。相关研究结果发表在2019年8月8日的Cell期刊上,论文标题为“Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes”。
这些研究人员还发现来自长期存活者的粪便菌群移植(fecal microbiota transplant, FMT)通过改变肿瘤中的细菌---肿瘤微生物组,促进小鼠模型中的免疫反应和抑制肿瘤。
论文通讯作者、德克萨斯大学MD安德森癌症研究中心临床癌症预防助理教授Florencia McAllister博士说道,“FMT实验的结果代表着通过改变肿瘤免疫微环境来改善胰腺癌治疗的重要治疗机会。这是有前景的,但我们还有很多研究工作要做。”
5.Nat Commun:高脂肪饮食导致糖尿病,肠道微生物或是罪魁祸首
doi:10.1038/s41467-019-11370-y
越来越多的研究表明,在肥胖期间,我们的免疫系统经常对通过肠道组织"渗漏"并导致炎症的细菌成分做出反应。反过来,炎症会导致胰岛素抵抗,从而使人容易患糖尿病。在一项近日发表在《Nature Communications》上的新研究中,多伦多综合医院研究所和病理学系大学健康网络(UHN)的Dan Winer博士和他的团队强调了高脂肪饮食如何影响肠道免疫系统中的B细胞,特别是那些生产一种叫做IgA的蛋白质的B细胞。
研究报告的主要撰写人Helen Luck说:"我们发现,在肥胖期间,肠道中有一种B细胞的水平较低,这种细胞能产生一种名为IgA的抗体。IgA是由我们的身体自然产生的,对调节我们肠道中的细菌至关重要。它作为一种防御机制,帮助中和利用环境变化的潜在危险细菌,比如当我们摄入不平衡或脂肪含量高的食物时。"
在他们的实验中,他们还观察到缺乏IgA的临床前模型(即缺乏保护的IgA)在喂食高脂肪食物时使血糖水平恶化。此外,将这些缺IgA模型中的肠道细菌移植到没有肠道细菌的模型中能够导致疾病,这表明IgA可以在与饮食相关的肥胖期间调节肠道中有害细菌的数量。
在Johane Allard博士和Herbert Gaisano博士领导的UHN减肥外科研究团队的合作下,该团队发现,减肥手术后不久,患者粪便中的IgA水平就会升高,这表明了IgA和肠道免疫系统对肥胖患者的重要性。
6.Nat Biotechnol:开发出混合宏基因组装配器OPERA-MS,更准确地组装复杂的微生物群落
doi:10.1038/s41587-019-0191-2
通过高通量宏基因组测序已实现了对微生物组的表征。然而,现有方法并不是将来自短读取技术和长读取技术的读取片段结合在一起。在一项新的研究中,来自新加坡国立大学、新加坡基因组研究院、新加坡陈笃生医院、南洋理工大学和克罗地亚萨格勒布大学的研究人员开发出一种称为OPERA-MS的混合宏基因组装配器,它将基于装配的宏基因组聚类与重复识别的精确支架结合在一起,以准确地组装复杂的微生物群落。相关研究结果发表在2019年8月的Nature Biotechnology期刊上,论文标题为“Hybrid metagenomic assembly enables high-resolution analysis of resistance determinants and mobile elements in human microbiomes”。
通过使用确定的体外和虚拟肠道微生物组进行的评估结果显示OPERA-MS组装宏基因组具有比长读取技术更高的碱基对准确度(> 5×; Canu),比短读取技术更高的连续性(~10× NGA50; MEGAHIT, IDBA-UD, metaSPAdes),而且比非宏基因组混合装配器发生更少的装配错误(2×; hybridSPAdes)。 OPERA-MS在同一物种的多个基因组存在下提供菌株区分性的组装,以大约9倍长读取覆盖率提供稀有物种的高质量参考基因组(<1%),并且以更高的覆盖率提供接近完整的基因组。
这些研究人员利用OPERA-MS组装了28个抗生素治疗患者的肠道宏基因组,并发现整合纳米孔长读取技术产生更为连续性的组装(比短读取组装提高200倍),包括80多个闭合质粒或噬菌体序列和一个新的263 kbp巨型噬菌体。
7.JEM:对肠道菌群精准化编辑有望降低结直肠癌患病风险
doi:10.1084/jem.20181939
近日,一项刊登在国际杂志Journal of Experimental Medicine上的研究报告中,来自西南医学中心的科学家们通过研究发现,对肠道菌群进行精准编辑或能降低小鼠炎性相关的结直肠癌风险,相关研究结果有望为慢性肠道炎症患者开发新型癌症预防策略。
除了结直肠癌外,长期的炎性肠病也与肠道中细菌群落的失衡直接相关,研究人员表示,我们的肠道中聚集着多种细菌,其中很多是有益菌群,能够改善机体总体健康;然而在特定状况下,这些微生物群落的正常功能也会被干扰,特定微生物的过度充裕与个体患包括特定癌症在内的多种疾病的风险增加有关。
本文研究中,研究者使用的策略能够靶向作用特殊的代谢通路,这些通路仅在肠道炎症和某些细菌中处于激活状态,这或许就能够减少细菌的丰度;基于此前研究结果,研究人员发现,这种新方法能够帮助抑制或降低结肠炎小鼠模型机体的炎症表现,同时并不会对携带平衡细菌菌群的健康对照动物产生明显效应。Winter博士说道,比如,大部分的大肠杆菌都是无害的,其能够保护机体肠道组织免于其它病原体的入侵,比如沙门氏菌,然而,有一类大肠杆菌却会产生毒素诱导DNA损伤并引发实验动物出现结肠癌;这项研究中,研究人员开发了一种简便的方法(给予小鼠水溶性钨盐使其易于出现炎症)来改变有害细菌产生能量促进其生长的方式,限制这些细菌的生长就能够降低机体肠道的炎症,并降低两种结直肠癌小鼠模型中肿瘤的发生率。
8.Nature突破:肠道微生物可能会影响ALS的进程
doi:10.1038/s41586-019-1443-5
魏茨曼科学研究所的研究人员在老鼠身上进行的研究发现,肠道微生物(统称肠道微生物群)可能会影响肌萎缩侧索硬化症(ALS)的进程,也被称为卢伽雷氏症。研究人员发现,小鼠接受了某些肠道微生物株或已知由这些微生物分泌的物质后,一种类似ALS的疾病的进展变慢,初步结果表明,该菌群调节功能的发现可能适用于ALS患者,相关研究成果于近日发表在《Nature》上,题为"Potential roles of gut microbiome & metabolites in modulation of murine ALS"。
科学家们开始在一系列实验中证明,在转基因小鼠中使用广谱抗生素清除其大部分微生物群后,一种类似ALS的疾病的症状会恶化。此外,科学家们还发现,在无菌条件下培育这些易患ALS的小鼠非常困难,因为这些小鼠很难在无菌环境中生存。综上所述,这些结果暗示了微生物群的改变与遗传上易患ALS的小鼠疾病加速发展之间的潜在联系。
接下来,利用先进的计算方法,科学家们对易患ALS的小鼠体内微生物组的组成和功能进行了表征,并将它们与正常小鼠进行了比较。他们鉴定出11种微生物菌株,这些菌株在易患ALS的小鼠中随着疾病的进展而发生变化,甚至在小鼠出现明显的ALS症状之前就发生了变化。当科学家们分离出这些微生物菌株,并在抗生素治疗后以类似益生菌的补充物的形式,一个接一个地给易患ALS的小鼠服用时,其中一些菌株对这种类似ALS的疾病产生了明显的负面影响。但有一种叫Akkermansia muciniphila的菌株显着减缓了小鼠的疾病进展,延长了它们的存活时间。
为了揭示该细菌产生这种效果的机理,科学家们检测了肠道微生物分泌的数千个小分子。他们将注意力集中在一种叫做烟酰胺(NAM)的分子上:抗生素治疗后,易患ALS的小鼠血液和脑脊液中的烟酰胺水平降低,而在补充了能够分泌这种分子的Akkermansia后,烟酰胺水平升高。为了证实NAM确实是一种能够阻碍ALS进程的微生物分泌分子,科学家们不断地向易患ALS的小鼠体内注入NAM。这些小鼠的临床状况明显改善。对他们大脑中基因表达的详细研究表明,NAM能改善他们运动神经元的功能。
9.Nat Med重大突破!粪菌群移植延长早衰小鼠寿命!
doi:10.1038/s41591-019-0504-5
肠道微生物群正在成为多种代谢、免疫和神经内分泌通路的关键调节因子。肠道微生物群失调与肥胖、2型糖尿病、心血管疾病、非酒精性脂肪酸性肝病和癌症等主要疾病有关,但其在衰老中的确切作用仍有待阐明。而近日来自西班牙奥维耶多大学的科学家们对这一问题进行了研究,发现在衰老与肠道微生物群之间存在联系,相关研究成果发表在《Nature Medicine》上,题为“Healthspan and lifespan extension by fecal microbiota transplantation into progeroid mice”。
该研究中,作者发现两种不同的早衰小鼠模型的特点是肠道失调,改变包括变形菌和蓝藻菌的丰度增加,疣微菌门细菌的丰度减少。与这些发现相一致的是研究人员还发现人类早衰症患者也表现出肠道失调,长寿的人肠道中疣微菌门细菌大量增加、变形杆菌显着减少。
研究人员还发现野生型小鼠粪便菌群移植在两种早衰型小鼠模型中均能延长健康寿命和寿命,而单纯移植疣微菌门细菌Akkermansia muciniphila就足以发挥有益作用。此外,通过对回肠内容物进行代谢组学分析,研究人员发现次生胆汁酸的恢复可能是重建健康微生物群的有益作用机制。
10.Nat Med:北大科学家发现肠道菌群调控多囊卵巢综合征的新机制
doi:10.1038/s41591-019-0509-0
多囊卵巢综合征(Polycystic ovary syndrome,PCOS)以雄激素过多、排卵功能障碍和多囊卵巢为特征,常伴有胰岛素抵抗性。而目前研究人员还不清楚PCOS患者发生排卵功能障碍和胰岛素抵抗的机制,这严重限制了相关药物和治疗方法的发展。
此前的研究发现代谢健康的改善与较高的微生物群基因含量和微生物多样性增加有关。因此,来自包括北京大学第三医院的乔杰院士与庞艳莉副研究员、北京大学医学部基础医学院姜长涛研究员在内的合作团队研究了肠道微生物群及其代谢产物对PCOS相关卵巢功能障碍和胰岛素抵抗的调节作用,相关研究成果于2019年7月22日发表在《Nature Medicine》上,题为"Gut microbiota-bile acid-interleukin-22 axis orchestrates polycystic ovary syndrome"。
该研究中,研究人员发现PCOS患者肠道菌群普通类杆菌(B. vulgatus)的含量显着升高,同时伴有糖脱氧胆酸和牛磺酸脱氧胆酸水平降低。研究人员给正常小鼠移植了患有多囊卵巢综合征(PCOS)或B. vulgatus感染小鼠的粪便微生物群后,会导致卵巢功能紊乱、胰岛素抵抗、胆汁酸代谢改变、白细胞介素-22分泌减少和不孕。
通过进一步研究,研究人员发现糖脱氧胆酸通过GATA结合蛋白3诱导肠道第3组先天淋巴细胞IL-22分泌,IL-22进而改善PCOS表型。这一发现与多囊卵巢综合征患者IL-22水平的降低一致。(生物谷 Bioon.com)
研究表明,肠道菌群紊乱与多种疾病的发生密切相关,如消化系统疾病、内分泌系统疾病、精神系统疾病、自身免疫性疾病以及一些感染性疾病。基于此,小编针对肠道微生物组最新研究进展,进行一番梳理,以飨读者。
1.Cell Rep:肠道微生物可以保护小鼠免受流感病毒感染
doi:10.1016/j.celrep.2019.05.105
研究人员近日在《Cell Reports》杂志上发表报告称,肠道微生物刺激非免疫肺细胞中的抗病毒信号,以在感染初期抵御流感病毒。增强的基线I型干扰素(IFNα/β)信号驱动了抗病毒反应,减少了小鼠流感病毒复制和体重减轻,但随着抗生素治疗这种保护作用会减弱。

图片来源:Cell Reports。
"这项研究支持了以下观点:服用抗生素不当不仅会促进抗生素耐药性、消除有用的保护性益生菌,还可能使你更容易受到病毒感染。"来自英国弗朗西斯·克里克研究所的该研究通讯作者Andreas Wack说道。"在一些国家,畜牧业大量使用抗生素,用于预防感染,因此接受治疗的动物可能更容易受到病毒感染。"
Wack和他的团队利用由于突变增加IFNα/β受体的表达水平的小鼠进行了研究,这些小鼠的基线IFNα/β信号升高了。这些小鼠对流感病毒感染更有抵抗力,体重减轻较少,感染8小时后病毒基因表达降低,两天后流感病毒复制减少。鉴于病毒载量控制较早,因此随后IFNα/β信号和抗病毒免疫反应没有完全启动。结果表明,调节IFNα/β受体的表达水平可以精准调控肺部的IFNα/β信号。基线IFNα/β信号增强的保护作用在抗生素治疗2-4周后降低了,主要在肺间质细胞的IFNα/β信号降低了--这是一群组成结构组织器官的非免疫细胞。相反,粪便移植逆转了抗生素引起的对流感病毒感染的易感性,这表明肠道微生物可能发挥了作用。
总的来说,结果表明微生物群增加了肺间质细胞的IFNα/β信号,从而提高了抵御流感病毒感染的能力。这项新发现与之前的研究结果一致,之前的研究表明,口服抗生素治疗的小鼠更容易感染病毒,包括甲型流感病毒。
2.Science子刊:肠道微生物群影响小鼠骨骼肌的质量和功能
doi:10.1126/scitranslmed.aan5662
一个国际研究小组发现,小鼠肠道微生物群在骨骼肌质量维持和功能方面发挥着重要作用。在发表于《Science Translational Medicine》杂志上的论文中,该小组描述了他们在野生和实验室饲养的小鼠上的实验,以及他们的最新发现。
在过去的几年里,科学家们发现人类和其他动物的肠道微生物群在维持健康方面所起的作用比之前认为的要大得多。除了加工食物,肠道微生物群在免疫和调节胆固醇和甘油三酯方面发挥着重要作用。肠道微生物群失衡与克罗恩病、肠易激综合征和其他炎症性疾病有关。现在,从事这项新工作的研究人员发现了新证据,表明肠道微生物群在维持适量的骨骼肌及其功能方面也发挥着作用--至少在老鼠身上是这样。
为了进一步了解微生物群对骨骼肌质量的可能影响,研究人员获得了几只野生小鼠,并将它们的微生物群与无菌小鼠(完全没有微生物群的小鼠)进行了比较。与野生小鼠相比,无菌小鼠骨骼肌萎缩。它们表达的支持肌肉生长的化学物质更少。研究人员发现,缺乏微生物组的老鼠体内的多种氨基酸水平高于正常水平,这是肝脏问题的迹象。他们还发现,老鼠体内的乙酰胆碱前体水平较低。乙酰胆碱是一种神经递质,参与骨骼肌和神经之间的信号传输。
研究人员还发现,将含有野生小鼠肠道微生物的物质移植到无菌小鼠的肠道中,可以增加肌肉质量和功能。他们发现,给予无菌小鼠肠道微生物正常产生的脂肪酸,也能部分恢复肌肉质量。
3.Science重大突破:肠道细菌竟然可以预防肥胖!
doi:10.1126/science.aat9351
犹他大学健康学院的研究人员发现,肠道中有一种特定的细菌可以防止老鼠变胖,这表明这些细菌也可以控制人类的体重。这种有益的细菌被称为梭状芽孢杆菌(Clostridia),是微生物群落的一部分--肠道内共有数万亿的细菌和其他微生物。
近日发表在《Science》杂志上的这项研究表明,健康的老鼠体内有大量梭状芽孢杆菌(一种由20到30种细菌组成的细菌),但那些免疫系统受损的老鼠随着年龄的增长会失去这些微生物。即使喂食健康的食物,老鼠也不可避免地会变胖。把这类微生物还给这些动物可以让它们保持苗条。
图片来源:Luat Nguyen, University of Utah Health
这项研究的结果已经指向这个方向。Petersen和他的同事发现梭状芽孢杆菌通过阻断肠道吸收脂肪的能力来防止体重增加。实验中,梭状芽孢杆菌是小鼠肠道中唯一的细菌,与完全没有微生物群的小鼠相比,梭状芽孢杆菌的小鼠更瘦,脂肪更少。他们还拥有较低水平的CD36基因,该基因控制着身体对脂肪酸的吸收。
Round说,这些发现可能会导致一种治疗方法,它比粪便移植和益生菌更有优势--目前正被广泛研究作为恢复健康微生物群的方法。基于将活菌群转移到肠道的治疗方法并不适用于所有人,因为不同的饮食和其他因素会影响哪些细菌能够存活和繁殖。
4.Cell:震惊!肿瘤微生物组竟能决定癌症患者的生死
doi:10.1016/j.cell.2019.07.008
在一项新的研究中,来自美国德克萨斯大学MD安德森癌症研究中心的研究人员发现少数长期存活的胰腺癌患者与许多对所有治疗方案都无效的胰腺癌患者之间的一个关键区别在于他们的肿瘤中的细菌群落刺激或抑制免疫反应。相关研究结果发表在2019年8月8日的Cell期刊上,论文标题为“Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes”。
这些研究人员还发现来自长期存活者的粪便菌群移植(fecal microbiota transplant, FMT)通过改变肿瘤中的细菌---肿瘤微生物组,促进小鼠模型中的免疫反应和抑制肿瘤。
论文通讯作者、德克萨斯大学MD安德森癌症研究中心临床癌症预防助理教授Florencia McAllister博士说道,“FMT实验的结果代表着通过改变肿瘤免疫微环境来改善胰腺癌治疗的重要治疗机会。这是有前景的,但我们还有很多研究工作要做。”
5.Nat Commun:高脂肪饮食导致糖尿病,肠道微生物或是罪魁祸首
doi:10.1038/s41467-019-11370-y
越来越多的研究表明,在肥胖期间,我们的免疫系统经常对通过肠道组织"渗漏"并导致炎症的细菌成分做出反应。反过来,炎症会导致胰岛素抵抗,从而使人容易患糖尿病。在一项近日发表在《Nature Communications》上的新研究中,多伦多综合医院研究所和病理学系大学健康网络(UHN)的Dan Winer博士和他的团队强调了高脂肪饮食如何影响肠道免疫系统中的B细胞,特别是那些生产一种叫做IgA的蛋白质的B细胞。
研究报告的主要撰写人Helen Luck说:"我们发现,在肥胖期间,肠道中有一种B细胞的水平较低,这种细胞能产生一种名为IgA的抗体。IgA是由我们的身体自然产生的,对调节我们肠道中的细菌至关重要。它作为一种防御机制,帮助中和利用环境变化的潜在危险细菌,比如当我们摄入不平衡或脂肪含量高的食物时。"
在他们的实验中,他们还观察到缺乏IgA的临床前模型(即缺乏保护的IgA)在喂食高脂肪食物时使血糖水平恶化。此外,将这些缺IgA模型中的肠道细菌移植到没有肠道细菌的模型中能够导致疾病,这表明IgA可以在与饮食相关的肥胖期间调节肠道中有害细菌的数量。
在Johane Allard博士和Herbert Gaisano博士领导的UHN减肥外科研究团队的合作下,该团队发现,减肥手术后不久,患者粪便中的IgA水平就会升高,这表明了IgA和肠道免疫系统对肥胖患者的重要性。
6.Nat Biotechnol:开发出混合宏基因组装配器OPERA-MS,更准确地组装复杂的微生物群落
doi:10.1038/s41587-019-0191-2
通过高通量宏基因组测序已实现了对微生物组的表征。然而,现有方法并不是将来自短读取技术和长读取技术的读取片段结合在一起。在一项新的研究中,来自新加坡国立大学、新加坡基因组研究院、新加坡陈笃生医院、南洋理工大学和克罗地亚萨格勒布大学的研究人员开发出一种称为OPERA-MS的混合宏基因组装配器,它将基于装配的宏基因组聚类与重复识别的精确支架结合在一起,以准确地组装复杂的微生物群落。相关研究结果发表在2019年8月的Nature Biotechnology期刊上,论文标题为“Hybrid metagenomic assembly enables high-resolution analysis of resistance determinants and mobile elements in human microbiomes”。

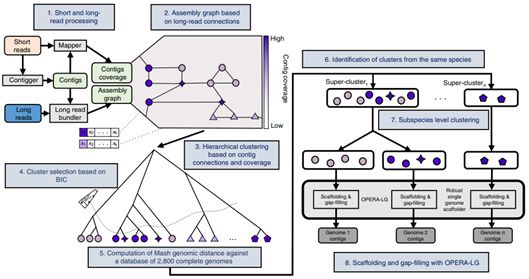
图片来自Nature Biotechnology, 2019, doi:10.1038/s41587-019-0191-2。
通过使用确定的体外和虚拟肠道微生物组进行的评估结果显示OPERA-MS组装宏基因组具有比长读取技术更高的碱基对准确度(> 5×; Canu),比短读取技术更高的连续性(~10× NGA50; MEGAHIT, IDBA-UD, metaSPAdes),而且比非宏基因组混合装配器发生更少的装配错误(2×; hybridSPAdes)。 OPERA-MS在同一物种的多个基因组存在下提供菌株区分性的组装,以大约9倍长读取覆盖率提供稀有物种的高质量参考基因组(<1%),并且以更高的覆盖率提供接近完整的基因组。
这些研究人员利用OPERA-MS组装了28个抗生素治疗患者的肠道宏基因组,并发现整合纳米孔长读取技术产生更为连续性的组装(比短读取组装提高200倍),包括80多个闭合质粒或噬菌体序列和一个新的263 kbp巨型噬菌体。
7.JEM:对肠道菌群精准化编辑有望降低结直肠癌患病风险
doi:10.1084/jem.20181939
近日,一项刊登在国际杂志Journal of Experimental Medicine上的研究报告中,来自西南医学中心的科学家们通过研究发现,对肠道菌群进行精准编辑或能降低小鼠炎性相关的结直肠癌风险,相关研究结果有望为慢性肠道炎症患者开发新型癌症预防策略。
除了结直肠癌外,长期的炎性肠病也与肠道中细菌群落的失衡直接相关,研究人员表示,我们的肠道中聚集着多种细菌,其中很多是有益菌群,能够改善机体总体健康;然而在特定状况下,这些微生物群落的正常功能也会被干扰,特定微生物的过度充裕与个体患包括特定癌症在内的多种疾病的风险增加有关。
本文研究中,研究者使用的策略能够靶向作用特殊的代谢通路,这些通路仅在肠道炎症和某些细菌中处于激活状态,这或许就能够减少细菌的丰度;基于此前研究结果,研究人员发现,这种新方法能够帮助抑制或降低结肠炎小鼠模型机体的炎症表现,同时并不会对携带平衡细菌菌群的健康对照动物产生明显效应。Winter博士说道,比如,大部分的大肠杆菌都是无害的,其能够保护机体肠道组织免于其它病原体的入侵,比如沙门氏菌,然而,有一类大肠杆菌却会产生毒素诱导DNA损伤并引发实验动物出现结肠癌;这项研究中,研究人员开发了一种简便的方法(给予小鼠水溶性钨盐使其易于出现炎症)来改变有害细菌产生能量促进其生长的方式,限制这些细菌的生长就能够降低机体肠道的炎症,并降低两种结直肠癌小鼠模型中肿瘤的发生率。
8.Nature突破:肠道微生物可能会影响ALS的进程
doi:10.1038/s41586-019-1443-5
魏茨曼科学研究所的研究人员在老鼠身上进行的研究发现,肠道微生物(统称肠道微生物群)可能会影响肌萎缩侧索硬化症(ALS)的进程,也被称为卢伽雷氏症。研究人员发现,小鼠接受了某些肠道微生物株或已知由这些微生物分泌的物质后,一种类似ALS的疾病的进展变慢,初步结果表明,该菌群调节功能的发现可能适用于ALS患者,相关研究成果于近日发表在《Nature》上,题为"Potential roles of gut microbiome & metabolites in modulation of murine ALS"。
科学家们开始在一系列实验中证明,在转基因小鼠中使用广谱抗生素清除其大部分微生物群后,一种类似ALS的疾病的症状会恶化。此外,科学家们还发现,在无菌条件下培育这些易患ALS的小鼠非常困难,因为这些小鼠很难在无菌环境中生存。综上所述,这些结果暗示了微生物群的改变与遗传上易患ALS的小鼠疾病加速发展之间的潜在联系。
接下来,利用先进的计算方法,科学家们对易患ALS的小鼠体内微生物组的组成和功能进行了表征,并将它们与正常小鼠进行了比较。他们鉴定出11种微生物菌株,这些菌株在易患ALS的小鼠中随着疾病的进展而发生变化,甚至在小鼠出现明显的ALS症状之前就发生了变化。当科学家们分离出这些微生物菌株,并在抗生素治疗后以类似益生菌的补充物的形式,一个接一个地给易患ALS的小鼠服用时,其中一些菌株对这种类似ALS的疾病产生了明显的负面影响。但有一种叫Akkermansia muciniphila的菌株显着减缓了小鼠的疾病进展,延长了它们的存活时间。
为了揭示该细菌产生这种效果的机理,科学家们检测了肠道微生物分泌的数千个小分子。他们将注意力集中在一种叫做烟酰胺(NAM)的分子上:抗生素治疗后,易患ALS的小鼠血液和脑脊液中的烟酰胺水平降低,而在补充了能够分泌这种分子的Akkermansia后,烟酰胺水平升高。为了证实NAM确实是一种能够阻碍ALS进程的微生物分泌分子,科学家们不断地向易患ALS的小鼠体内注入NAM。这些小鼠的临床状况明显改善。对他们大脑中基因表达的详细研究表明,NAM能改善他们运动神经元的功能。
9.Nat Med重大突破!粪菌群移植延长早衰小鼠寿命!
doi:10.1038/s41591-019-0504-5
肠道微生物群正在成为多种代谢、免疫和神经内分泌通路的关键调节因子。肠道微生物群失调与肥胖、2型糖尿病、心血管疾病、非酒精性脂肪酸性肝病和癌症等主要疾病有关,但其在衰老中的确切作用仍有待阐明。而近日来自西班牙奥维耶多大学的科学家们对这一问题进行了研究,发现在衰老与肠道微生物群之间存在联系,相关研究成果发表在《Nature Medicine》上,题为“Healthspan and lifespan extension by fecal microbiota transplantation into progeroid mice”。
该研究中,作者发现两种不同的早衰小鼠模型的特点是肠道失调,改变包括变形菌和蓝藻菌的丰度增加,疣微菌门细菌的丰度减少。与这些发现相一致的是研究人员还发现人类早衰症患者也表现出肠道失调,长寿的人肠道中疣微菌门细菌大量增加、变形杆菌显着减少。
研究人员还发现野生型小鼠粪便菌群移植在两种早衰型小鼠模型中均能延长健康寿命和寿命,而单纯移植疣微菌门细菌Akkermansia muciniphila就足以发挥有益作用。此外,通过对回肠内容物进行代谢组学分析,研究人员发现次生胆汁酸的恢复可能是重建健康微生物群的有益作用机制。
10.Nat Med:北大科学家发现肠道菌群调控多囊卵巢综合征的新机制
doi:10.1038/s41591-019-0509-0
多囊卵巢综合征(Polycystic ovary syndrome,PCOS)以雄激素过多、排卵功能障碍和多囊卵巢为特征,常伴有胰岛素抵抗性。而目前研究人员还不清楚PCOS患者发生排卵功能障碍和胰岛素抵抗的机制,这严重限制了相关药物和治疗方法的发展。
此前的研究发现代谢健康的改善与较高的微生物群基因含量和微生物多样性增加有关。因此,来自包括北京大学第三医院的乔杰院士与庞艳莉副研究员、北京大学医学部基础医学院姜长涛研究员在内的合作团队研究了肠道微生物群及其代谢产物对PCOS相关卵巢功能障碍和胰岛素抵抗的调节作用,相关研究成果于2019年7月22日发表在《Nature Medicine》上,题为"Gut microbiota-bile acid-interleukin-22 axis orchestrates polycystic ovary syndrome"。
该研究中,研究人员发现PCOS患者肠道菌群普通类杆菌(B. vulgatus)的含量显着升高,同时伴有糖脱氧胆酸和牛磺酸脱氧胆酸水平降低。研究人员给正常小鼠移植了患有多囊卵巢综合征(PCOS)或B. vulgatus感染小鼠的粪便微生物群后,会导致卵巢功能紊乱、胰岛素抵抗、胆汁酸代谢改变、白细胞介素-22分泌减少和不孕。
通过进一步研究,研究人员发现糖脱氧胆酸通过GATA结合蛋白3诱导肠道第3组先天淋巴细胞IL-22分泌,IL-22进而改善PCOS表型。这一发现与多囊卵巢综合征患者IL-22水平的降低一致。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->