罕见肝病新药!PPARα/δ激动剂elafibranor获孤儿药资格,治疗原发性胆汁性胆管炎(PBC)
来源:本站原创 2019-07-30 21:24
2019年07月30日讯 /生物谷BIOON/ --Genfit是一家处于后期临床阶段的生物制药公司,致力于发现和开发创新的治疗和诊断解决方案,用于代谢和肝脏相关疾病领域。近日,该公司宣布,美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)已授予其先导候选药物PPARα/δ双重激动剂elafibranor治疗原发性胆汁性胆管炎(PBC)的孤儿药资格。孤儿药是指用于预防、治疗、诊断罕见病的药品

2019年07月30日讯 /生物谷BIOON/ --Genfit是一家处于后期临床阶段的生物制药公司,致力于发现和开发创新的治疗和诊断解决方案,用于代谢和肝脏相关疾病领域。近日,该公司宣布,美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)已授予其先导候选药物PPARα/δ双重激动剂elafibranor治疗原发性胆汁性胆管炎(PBC)的孤儿药资格。
孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物获批上市后为期7年的市场独占期。在欧洲,罕见病是指发病率不超过万分之五的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,协助临床设计、减免欧盟监管备案费用等,获得欧盟的基金支持,以及产品获批上市后为期10年的市场独占期。
今年4月,FDA还授予了elafibranor突破性药物资格(BTD),用于治疗对熊去氧胆酸(UDCA)反应不足的PBC成人患者。此次BTD授予,基于一项随机、双盲、安慰剂对照II期临床研究的数据,该研究在对UDCA反应不足的PBC成人患者中开展。详细结果已在今年4月举行的2019年欧洲肝脏研究协会年会/国际肝病大会(ILC2019/EASL)上公布。
数据显示,elafibranor显著降低了碱性磷酸酶(ALP)水平,与安慰剂相比在主要终点方面表现出了显著的治疗效果,同时也达到了用于药物注册的复合终点。除了ALP显著降低之外,2组患者的其他PBC标志物,包括γ-谷氨酰转移酶(GGT)、脂质标记物(总胆固醇、低密度脂蛋白和甘油三酯)和抗炎标记物(IgM、CRP、结合珠蛋白和纤维蛋白原)也表现出改善。研究中,2种剂量elafibranor治疗具有良好的耐受性。Genfit公司计划在2019年启动III期临床研究,进一步评估elafibranor治疗PBC的疗效和安全性。
Genfit公司副首席医疗官Pascal Birman表示:“PBC是一种毁灭性的肝病,几乎没有治疗选择,迫切需要新的疗法。在II期研究中,elafibranor显示出良好的抗胆汁淤积作用,同时显示出减少瘙痒的趋势。这些数据为PBC患者及其家属提供了希望。我们预计将在今年晚些时候启动III期临床试验,进一步证明elafibranor在治疗PBC方面的安全性和有效性。”
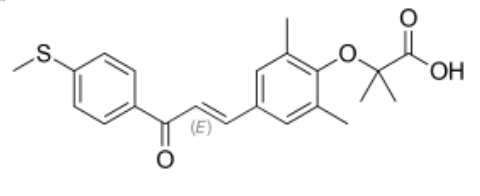
elafibranor分子结构式(图片来源:Wikipedia)
elafibranor是一种首创的(first-in-class)过氧化物酶体增殖物激活受体α和δ(PPARα/δ)双重激动剂,在II期研究中治疗UDCA反应不足的PBC成人患者已获得了积极的安全性和疗效结果。目前,elafibranor也正在III期临床研究中评估治疗非酒精性脂肪性肝炎(NASH)的潜力。
PBC是一种罕见的肝脏疾病,主要是因胆管(功能为将胆汁运出肝脏)遭到自身免疫性破坏,导致胆汁淤积,抑制肝脏清除体内毒素的能力,并导致肝组织瘢痕化,即肝硬化。NASH是非酒精性脂肪肝的一种极端发展形式,定义为伴随有炎症及肝细胞损伤的脂肪变性现象的出现,该病可导致晚期肝脏纤维化、肝硬化、肝衰竭及肝脏肿瘤的产生。elafibranor被认为能解决NASH的多方面问题,包括炎症、胰岛素敏感性、脂质/代谢特征和肝脏标记物。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


