罕见病新药!凯瑞康宁新型嗜睡症药物XWL-008获美国FDA授予孤儿药资格
来源:本站原创 2019-06-25 09:01
2019年06月25日讯 /生物谷BIOON/ --凯瑞康宁有限公司(XW Laboratories Inc,简称“凯瑞康宁”)是一家临床阶段的生物制药公司,专注于开发治疗神经系统疾病的创新药物。近日,该公司宣布,美国食品和药物管理局(FDA)已授予XWL-008用于治疗发作性睡病(又称嗜睡症)的孤儿药资格(ODD)。孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称

2019年06月25日讯 /生物谷BIOON/ --凯瑞康宁有限公司(XW Laboratories Inc,简称“凯瑞康宁”)是一家临床阶段的生物制药公司,专注于开发治疗神经系统疾病的创新药物。近日,该公司宣布,美国食品和药物管理局(FDA)已授予XWL-008用于治疗发作性睡病(又称嗜睡症)的孤儿药资格(ODD)。
孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物获批上市后为期7年的市场独占期。
发作性睡病(又称嗜睡症)是一种慢性神经系统睡眠障碍疾病,患者神经细胞因缺乏下丘脑泌素(hypocretin)导致出现睡眠-觉醒周期调节异常。这种疾病的典型特征是白天过度嗜睡(EDS)和猝倒(由情绪引发的肌肉突然失去控制能力)。在美国发作性睡病的发病率约为1/2000,全世界有约有300万人患有这种疾病。
当前,大多数治疗嗜睡症的药物都是针对一个症状,而那些同时治疗EDS和猝倒的药物可能与不可忍受的副作用和不方便的给药方案相关。XWL-008是凯瑞康宁管线中的下一代小分子药物,不仅有望有效治疗嗜睡症的主要症状,而且有望提高耐受性和给药便利性。
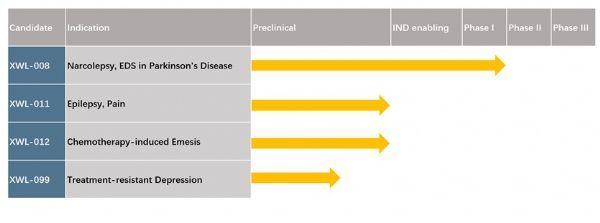
凯瑞康宁创始人、首席执行官向家宁博士表示:“我们很高兴收到XWL-008用于治疗发作性睡病的孤儿药资格认证。我们将继续致力于XWL 008的临床开发,使其成为这种罕见疾病的潜在一线治疗用药。我们最近成功完成XWL-008临床I期研究,这是公司的一个重要里程碑。临床I期数据显示,XWL-008具有良好的安全性、耐受性和药代动力学特征。我们目前正在准备开展临床III期研究并将实施505(b)(2) NDA申报途径,尽快将这种新型候选药物带给全球发作性睡病患者。”
凯瑞康宁主要研发工作在中国大陆的武汉市和台湾的新北市进行,该公司在药物研发设计方面的优势及其多个药物研发平台使其能够缩短用于确定同类最佳临床候选药物的开发时间而取得至关重要的竞争优势。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->