科学家们在胃癌研究领域取得的重要研究成果!
来源:本站原创 2019-04-16 21:55
胃癌是最常见的一种消化道肿瘤,目前全球每年约有100万人患病,而我国就占到了一半。在所有癌症中,胃癌与吃的关系最为密切,可以说是病从口入。那么近年来科学家们在胃癌研究领域取得了哪些研究成果呢?本文中,小编就对相关研究进行了整理,分享给大家!【1】PNAS:特殊药物或能通过诱发幽门螺杆菌基因突变来有效抑制胃癌发生doi:10.1073/pnas.1814497116近日,一项刊登在国际杂志Proce
胃癌是最常见的一种消化道肿瘤,目前全球每年约有100万人患病,而我国就占到了一半。在所有癌症中,胃癌与吃的关系最为密切,可以说是病从口入。那么近年来科学家们在胃癌研究领域取得了哪些研究成果呢?本文中,小编就对相关研究进行了整理,分享给大家!

【1】PNAS:特殊药物或能通过诱发幽门螺杆菌基因突变来有效抑制胃癌发生
doi:10.1073/pnas.1814497116
近日,一项刊登在国际杂志Proceedings of the National Academy of Sciences上的研究报告中,来自范德堡大学医学中心的科学家们通过研究发现,目前作为一种化疗制剂治疗多种类型的药物或许在治疗胃癌上也表现出了巨大潜力;研究者发现,除了已知能阻断癌细胞的生长外,名为DFMO(二氟甲基鸟氨酸)的药物还能直接作用幽门螺杆菌降低其毒力,幽门螺杆菌的感染是引发胃癌的主要原因。
胃癌是引发癌症患者死亡的第三大原因,本文研究结果支持了研究者们进一步研究DFMO如何预防胃癌的发生;幽门螺杆菌会感染一半人群的胃部组织,但仅有大约1%的感染者会发展成胃癌,尽管我们可以通过治疗感染的方式来预防胃癌发生,但研究人员并不清楚该选择谁来治疗,此外,幽门螺杆菌还会产生一些有益的效果—食管返流疾病,哮喘和其它过敏性疾病更常发生于未感染幽门螺杆菌的人群中。
doi:10.1158/0008-5472.CAN-18-2095
近日,一项刊登在国际杂志Cancer Research上的研究报告中,来自卡迪夫大学的科学家们通过研究阐明了胃癌发生的新型分子机制,相关研究或为开发新型胃癌疗法提供了新的线索和希望。研究者指出,未来他们或能通过剔除参与干细胞功能的特殊细胞表面受体来阻断胃部细胞的分裂和生长。
研究者Toby Phesse博士表示,胃癌患者的预后较差,而且患者的治疗选择也非常有限,因此临床上就急需开发出应对胃癌的新型疗法。有些胃癌患者机体中会携带某些基因突变,这些基因主要参与Wnt信号通路的调节(Wnt信号通路与细胞分裂有关),而这些基因突变会驱动癌症的发生和进展。
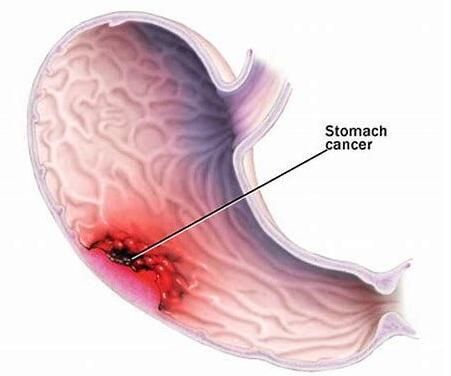
新闻阅读:Explainer: what is Helicobacter pylori?
1982年,来自澳大利亚的两位科学家:Robin Warren和Barry Marshall在人类的胃里发现了一种奇怪的细菌,随后他们深入研究后发现,这种细菌会引发胃炎,即让患者出现胃部炎症;当时这种观点并未得到临床医生的认可,为了说服怀疑的人,研究者利用这些细菌感染了自己,随后他患上了胃炎。
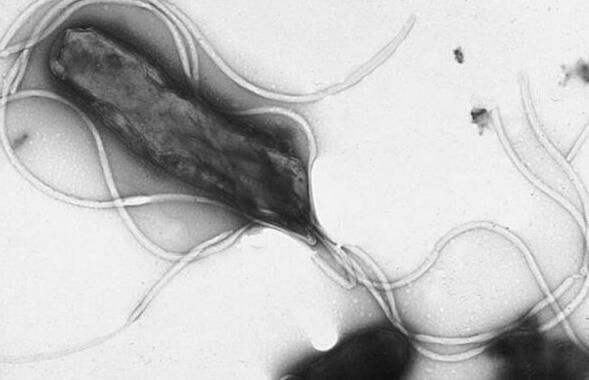
这些被称之为幽门螺杆菌的特殊细菌有着曲杆样的结构,菌体一侧有鞭毛,这些鞭毛能像手臂一样摆动,推动细菌在胃部组织中活动;全球大约一半人都被幽门螺杆菌感染过,尽管感染状况在不同国家和年龄组中是不同的,但老年人群中的发病率仍然较高,目前大约15%的澳大利亚人群都感染过幽门螺杆菌。
通常情况下,幽门螺杆菌会感染儿童的胃部组织,并永远在胃部中生存;在诸如澳大利亚等发达国家中,这种细菌似乎会通过口-口传播,或者从母亲身上扩散到孩子体内,而在发展中国家,幽门螺杆菌会通过被污染的水来传播(尽管这一论断并未被证实)。
【4】Oncogene:中国学者发现胃癌诊断潜在标志物 或有助于胃癌诊断治疗
doi:10.1038/s41388-018-0402-1
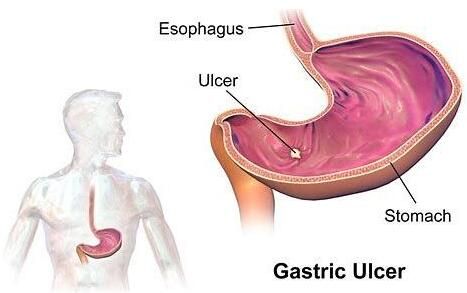
胃癌是一种常见的癌症类型,也是癌症相关死亡中第二大类型,尽管目前已经在胃癌治疗方面取得很大进展,但胃癌病人的预后情况仍不乐观,如何提早诊断及时治疗并能够防止癌症复发是治疗胃癌的重大难题。
代谢紊乱是胃癌的一个显著特征,在最近发表在国际学术期刊Oncogene上的一项研究中,来自香港中文大学的研究人员发现在胃癌中CAB39L是肿瘤代谢的一个新调控因子。CAB39L在胃癌细胞系和胃癌组织中因启动子甲基化而发生沉默。
研究人员发现过表达CAB39L能够抑制胃癌细胞和胃癌小鼠模型的生长和进展,而敲低CAB39L则会促进肿瘤发生,这表明CAB39L作为肿瘤抑制因子发挥功能。从机制上来说,CAB39L能够与LKB1-STRAD复合体发生相互作用,诱导LKB1表达,导致AMPBα/β的磷酸化和激活。LKB1-AMPK在胃癌细胞系中激活具有肿瘤抑制作用,并且二甲双胍(AMPK激活剂)能够抑制缺失了CAB39L的胃癌细胞的生长。
【5】Oncogene:南京医科大学学者发现促进胃癌进展的重要lncRNA
doi:10.1038/s41388-018-0308-y
近年来大量研究表明长非编码RNA(LncRNA)在基因组印记以及染色质修饰,转录激活,转录干扰等多个生物学过程中发挥重要的调控作用并且在多种癌症中出现表达失调。虽然关于lncRNA的研究取得众多进展,但绝大部分lncRNA的功能仍然是不清楚的。
来自南京医科大学第一附属医院的束永前等人对在胃癌中发挥重要调控作用的lncRNA进行了深入分析,并对FOXD2-AS1在胃癌进展中发挥的功能以及调控的相关生物学机制进行了深入了解。相关研究结果发表在国际学术期刊Oncogene上。
【6】Nat Commun:人工智能帮助找到导致胃癌的基因突变!
doi:10.1038/s41467-018-03828-2
在一项开创性研究中,来自新加坡基因组研究所(GIS)科技研究局的研究人员开发了一种全新的机器学习计算机模型(一种人工智能模型,AI)来准确寻找肿瘤突变。他们还发现了一个非编码DNA的新基因突变可能导致了胃癌。这项研究开发出的新技术将在未来帮助研究人员探索其他肿瘤中非编码DNA突变的影响。
癌症是全球最大的致死因之一,而胃癌是全球第四最致命的癌症。癌症由于DNA突变导致细胞异常生长所致。我们基因组中那2%的可编码DNA已经得到了充分的研究,但是其他98%的非编码DNA仍然处于无人所知的状态。非编码DNA可以调节基因活性,而越来越多的证据表明这些基因区域的基因突变也会促使癌症的发生发展。
doi:10.1016/j.ccell.2017.11.018
最近,来自杜克大学医学院的研究者们利用基因组分析手段深入理解了肠道组织病变(intestinal metaplasia,IM)对于胃癌发生的影响。众所周知,IM是胃癌发生的重要风险因子,患有IM的患者患胃癌的几率是其他人群的六倍。这项研究则着重于其中的机制,相关结果发表在最近一期的《Cancer Cell》杂志上。这项研究同时能够帮助幽门螺杆菌感染的患者诊断癌症的发生风险。
根据WHO的数据,胃癌是世界上死亡风险第三高的癌症,这类疾病被认为是由幽门螺杆菌感染引发,不过如果治疗及时,还是能够治愈的。不幸的是,三分之二以上的胃癌患者被诊断时已经处于晚期阶段。
doi:10.1016/j.chom.2017.09.005
胃癌是五种最为致命的癌症之一。根据世界卫生组织(WHO)的统计,每年大约有75万患者死于这种疾病。这种疾病的主要原因被认为是幽门螺旋杆菌(Helicobacter pylori)感染。目前,人们尚没有有效地治疗胃癌的方法,而且抗生素耐药性的不断扩散也使得治疗这种细菌感染变得更加复杂。如今,在一项新的研究中,来自德国埃尔朗根-纽伦堡大学(Friedrich-Alexander-Universit?t Erlangen-Nürnberg, FAU)的研究人员鉴定出这种细菌能够导致胃癌的两种机制。他们的发现可能导致人们开发出新的治疗方法。
FAU微生物学系主任Nicole Tegtmeyer博士领导的一个国际科学家小组研究了幽门螺旋杆菌如何破坏胃部的保护层。这个保护层由紧密排列的上皮细胞组成,从而保护胃部不受胃酸的影响。
如今,这些研究人员发现幽门螺旋杆菌分泌一种被称作HtrA的蛋白酶,它的作用就像一种武器那样能够穿透这个保护层。HtrA切割三种蛋白:闭合蛋白(occludin)、紧密连接蛋白-8(claudin-8)和上皮钙黏蛋白(E-cadherin),从而破坏这个上皮细胞保护层。

【9】Nature:颠覆常规!揭示幽门螺旋杆菌感染导致胃癌新机制
doi:10.1038/nature23642
胃癌是癌症相关死亡的最为常见的病因之一,主要是因为大多数患者处于这种疾病的晚期阶段。这种癌症的主要原因在于长期感染着大约一半人类的幽门螺旋杆菌(Helicobacter pylori)。然而,不同于致癌病毒的是,细菌不会在它们的宿主细胞中储存转化基因,而且它们如何能够导致癌症迄今为止仍然是个谜。
如今,在一项新的研究中,来自德国马克斯普朗克感染生物学研究所和美国斯坦福大学等医研究机构的研究人员发现幽门螺旋杆菌让胃部中的干细胞更新过度运转。很多科学家之前已猜测干细胞周转在癌症产生中发挥着作用。通过证实胃部含有两种不同的对相同的驱动信号作出不同反应的干细胞群体,这些研究人员发现一种新的组织可塑性机制,这就允许调整组织更新来应对细菌感染。
【10】Nat Cell Biol:胃癌产生新机制-表达Lgr5的主细胞转化为干细胞,不过争论依旧存在
doi:10.1038/ncb3541
在健康人体内,在胃体腺(corpus gland)底部发现的主细胞(chief cell)产生消化酶。然而,根据一项新的研究,如果肠道经历损伤或基因突变,那么这些主细胞能够转化为导致胃癌产生的干细胞。研究者表示,这是首次明确证实一部分主细胞容易发生癌变,而且能够作为胃癌的起源。胃癌形成细胞的身份一直是充满争议的,而且并不是所有的人都信服Barker的研究已解决了这一争论。
肠胃病学上长期存在的一种理论是胃部中的干细胞是在胃峡(isthmus)中产生的。胃峡是位于胃体腺中间附近的一个区域。这些干细胞迁移到胃体腺的顶部和底端,补充丢失的细胞,从而维持胃部动态平衡。很多科学家认为,这些干细胞发生的突变能够导致癌前病变,如组织化生(metaplasia,即组织中的异常变化)。
然而,近年来,一种新的假设出现了。基于对表达解痉多肽的化生组织(spasmolytic polypeptide-expressing metaplasia, SPEM)的观察结果,美国范德堡大学的James Goldenring和同事们已提出胃部中的这种特定的组织化生起源自已转化为或转分化为一种不同细胞类型的主细胞。Barker说,“观察到这种情形发生是非常困难的,而且人们对它是否真地在人体中发生提出质疑。它是充满争议的。”(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


