胃肠道间质瘤新药!KIT/PDGFRα激酶抑制剂ripretinib展现强劲疗效,再鼎医药引入中国开发
来源:本站原创 2019-11-04 16:32
2019年11月04日讯 /生物谷BIOON/ --再鼎医药合作伙伴Deciphera Pharmaceuticals是一家专注于解决肿瘤耐药关键机制的临床阶段生物制药公司。近日,Deciphera公司公布了广谱KIT和PDGFRα抑制剂ripretinib一项正在进行的I期研究的最新数据,该研究评估了ripretinib用于二线、三线、≥四线治疗胃肠道间质瘤(GIST)患者。最新结果来自接受每日

2019年11月04日讯 /生物谷BIOON/ --再鼎医药合作伙伴Deciphera Pharmaceuticals是一家专注于解决肿瘤耐药关键机制的临床阶段生物制药公司。近日,Deciphera公司公布了广谱KIT和PDGFRα抑制剂ripretinib一项正在进行的I期研究的最新数据,该研究评估了ripretinib用于二线、三线、≥四线治疗胃肠道间质瘤(GIST)患者。
最新结果来自接受每日一次(QD)150mg剂量ripretinib作为起始治疗的142例GIST患者的数据,该剂量目前正用于注册研究INVICTUS和INTRIGUE。截至2019年8月10日,采用实体瘤疗效评价标准1.1版(RECIST v1.1)确定的客观缓解率(ORR)、中位缓解持续时间(DOR)、中位无进展生存期(mPFS)和平均治疗时间如下表所示:
研究中,ripretinib的耐受性良好,更新的不良事件与之前公布的I期研究中GIST患者的数据一致。发生在>5%患者中的3级或4级治疗引起的不良事件(TEAE)为脂肪酶水平升高(n=25,18%)、贫血(n=11,8%)和腹痛(n=11,8%)。
上述结果表明,在晚期GIST患者中,ripretinib在推荐剂量150mg QD下显示出令人鼓舞的临床治疗效果,二线或多线治疗具有良好的耐受性。
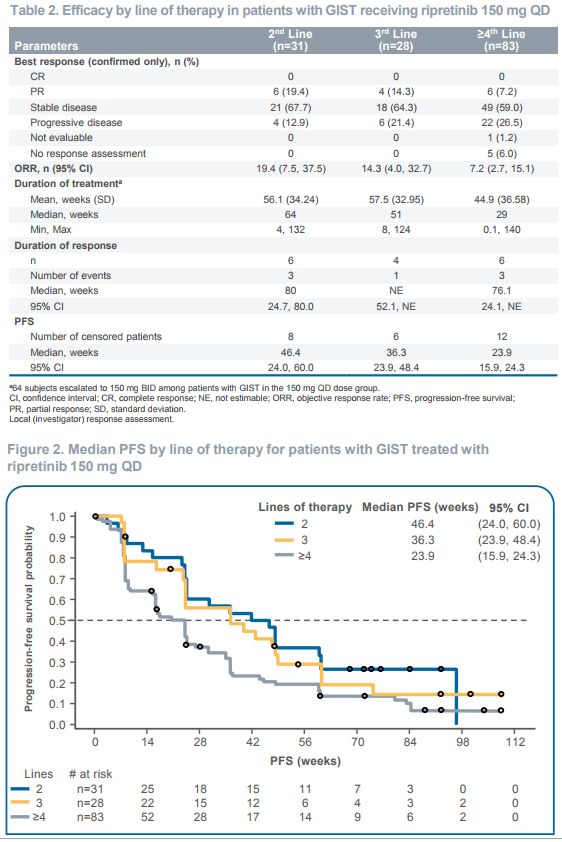
来自I期扩展研究2线患者的数据显示中位PFS为46.4周,支持了正在进行的III期INTRIGUE研究,该研究正在比较ripretinib和舒尼替尼(sunitinib)二线治疗GIST患者。
来自I期扩展研究≥4线患者的数据,支持了关键性III期INVICTUS研究(NCT03353753)并与ESMO 2019大会上公布的INVICTUS研究的阳性结果一致。该研究评估了ripretinib作为≥4线疗法治疗129例晚期GIST患者(ripretinib n=85,安慰剂n=44),结果显示研究达到了主要终点:与安慰剂组相比,ripretinib治疗组疾病进展或死亡风险显著降低了85%(HR=0.15,p<0.0001)、无进展生存期显著延长(中位PFS:6.3个月[27.6周] vs 1.0个月[4.1周])。次要终点总缓解率(ORR)方面,ripretinib治疗组与安慰剂组相比大幅提高(ORR:9.4% vs 0%,p=0.0504),但没有达到统计学显著性。在次要终点总生存期(OS)方面,ripretinib治疗组与安慰剂组相比显著改善(中位OS:15.1个月 vs 6.6个月,HR=0.36,名义p=0.0004)。由于ORR没有达到统计学显著性,因此没有对OS进行正式检验。安慰剂组的OS数据包括接受安慰剂治疗病情进展后转向ripretinib治疗的患者数据。
基于INVICTUS研究结果,Deciphera公司计划在2020年第一季度向美国FDA提交一份新药申请(NDA),寻求批准ripretinib用于先前已接受过伊马替尼、舒尼替尼、瑞戈非尼治疗的晚期GSIT患者。今年6月,美国FDA授予了ripretinib治疗既往已接受过伊马替尼、舒尼替尼、瑞戈非尼治疗的晚期GIST患者的快速通道资格。
Decriphera公司执行副总裁兼首席医疗官Matthew L.Sherman医学博士表示:“这些最新结果继续强调了我们候选产品ripretinib的潜力,表明该药继续在已接受伊马替尼治疗的GIST患者中显示出强大的临床效益,特别是在二线治疗中。这些结果增强了我们对正在进行的关键III期临床研究INTRIGUE的信心,该研究旨在支持ripretinib用于二线GIST患者的潜在监管批准。”

ripretinib分子结构(图片来源:medchemexpress.cn)
ripretinib是一款KIT/PDGFRα激酶开关调控抑制剂,用于治疗KIT/PDGFRα驱动的胃肠道间质瘤(GIST)、系统性肥大细胞增多症(SM)以及其他癌症。ripretinib特别设计通过抑制KIT和PDGFRα的广谱突变来改善胃肠道间质瘤患者的治疗。 ripretinib可阻断胃肠道间质瘤中涉及的第9、11、13、14、17、18外显子中的起始和继发KIT突变以及SM中发现的原发性KIT第17号外显子D816V突变。 ripretinib还抑制第12、14、18外显子中的原发性PDGFRα突变,包括涉及第18外显子D842V突变的胃肠道间质瘤。
今年6月,再鼎医药从Deciphera公司获得ripretinib在大中华区(中国大陆、香港、澳门和台湾)开发和推广的独家许可。根据协议条款,Deciphera公司将获得2,000万美元的现金预付款,并有资格获得最高达1.85亿美元的潜在开发和商业里程碑付款。此外,再鼎医药将根据ripretinib在大中华区的年度净销售额向Deciphera支付特许权使用费。
值得一提的是,去年6月,基石药业与Blueprint达成独家合作及授权协议,获得了在三款化合物(avapritinib、BLU-554、BLU-667)在大中华区开发和商业化的独家权利。其中,avapritinib也是一款强效、高度选择性KIT和PDGFRA抑制剂。在美国和欧盟,avapritinib已经提交上市申请,治疗:(1)携带PDGFRA基因18号外显子突变的GIST患者,不论之前接受的疗法如何;(2)四线GIST患者。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


