T细胞疗法预防/治疗病毒性疾病!同种异体多病毒特异性T细胞疗法Viralym-M获优先药物资格(PRIME)
来源:本站原创 2020-02-13 15:33
2020年02月13日讯 /生物谷BIOON/ --AlloVir是一家处于后期临床阶段的T细胞免疫治疗公司。近日,该公司宣布,欧洲药品管理局(EMA)已授予Viralym-M(ALVR105)优先药物资格(PRIME),这是一种同种异体、即用型(off-the-shelf)、多病毒特异性T细胞疗法,用于异基因造血干细胞移植(HSCT)受者,治疗BK病毒、巨

2020年02月13日讯 /生物谷BIOON/ --AlloVir是一家处于后期临床阶段的T细胞免疫治疗公司。近日,该公司宣布,欧洲药品管理局(EMA)已授予Viralym-M(ALVR105)优先药物资格(PRIME),这是一种同种异体、即用型(off-the-shelf)、多病毒特异性T细胞疗法,用于异基因造血干细胞移植(HSCT)受者,治疗BK病毒、巨细胞病毒、人疱疹病毒6型、EB病毒和/或腺病毒的严重感染。
此前,美国食品和药物管理局(FDA)已授予Viralym-M再生医学先进疗法(RMAT)资格,用于治疗接受同种异体HSCT后成人和儿童患者中由BK病毒引起的出血性膀胱炎(HC)。AlloVir公司拥有Viralym-M的全球开发和商业化权利。AlloVir致力于为遭受威胁生命的病毒性疾病的患者开发和提供变革性细胞疗法。
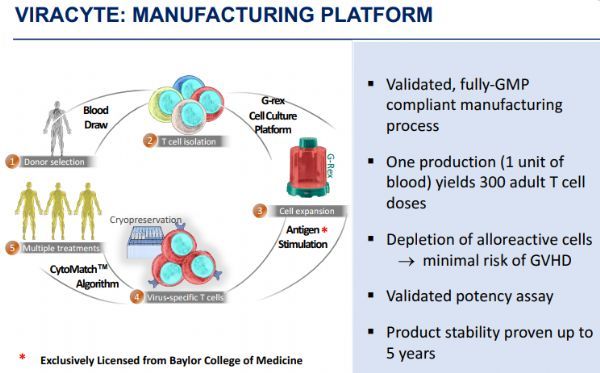
病毒特异性T细胞制备流程
PRIME是EMA在2016年3月推出的一个快速审批项目,与美国FDA的突破性药物资格(BTD)项目相似,旨在加速医药短缺领域重点药品的审评进程,尽早使患者受益。入围PRIME的实验性药物,将在临床试验及药品开发方面获得EMA的大力支持,以加速真正创新药物的开发及审批,来满足对有前景新药的医疗需求。获得PRIME资格的药物,必须有初步临床证据和非临床证据表明该药与现有治疗药物相比能够实质性改善病情。
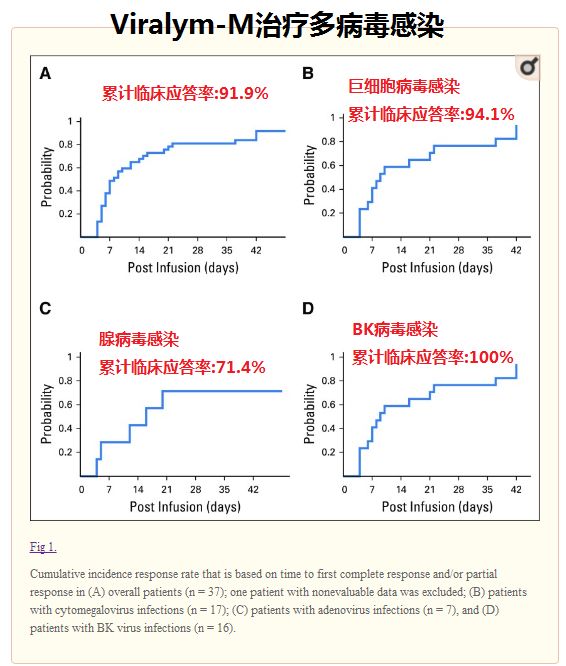
EMA授予Viralym-M PRIME资格认定,基于一项II期概念验证研究的积极数据。该研究结果已发表于《临床肿瘤学杂志》(Tzannou,JCO,2017)。数据显示,接受常规治疗失败的患者,接受Viralym-M治疗后,超过90%的患者根据预定标准病情表现出完全或部分临床反应,大多数患者表现出主要临床症状的完全缓解。
AlloVir公司已计划在2020年启动Viralym-M的关键III期研究以及针对6种常见破坏性病毒病原体的II期概念验证研究。
在健康的个体中,来自身体自然防御系统的病毒特异性T细胞(VST)提供了对多种致病病毒的保护。然而,在免疫系统减弱的患者中,这些病毒可能无法控制。病毒性疾病是常见的,对免疫功能低下的患者有潜在的毁灭性和危及生命的后果。例如,高达90%的患者在异基因干细胞移植后至少会激活一种病毒,其中三分之二的患者会激活一种以上的病毒,导致严重和长期的发病率、住院和过早死亡。通常,当病毒感染免疫功能低下的患者时,标准的抗病毒治疗不能解决免疫系统减弱的根本问题,因此,许多患者会遭受危及生命的后果,如多器官损伤和衰竭,甚至死亡。
Viralym-M是AlloVir公司异基因、off-the shelf、多病毒特异性T细胞疗法管线中的一种先导研究性疗法,旨在治疗免疫功能低下患者(包括HSCT、实体器官移植患者或原发性免疫缺陷、癌症或HIV患者)的活动性病毒病。Viralym-M有潜力在患者免疫功能受损的情况下,对抗或预防一系列严重且危及生命的病毒性疾病,通过大幅度降低或预防疾病发病率和显著改善预后,从根本上改变病毒性疾病患者的生活。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->