CD19 CAR-T细胞疗法!吉利德Yescarta在美国进入审查:二线治疗复发/难治性大细胞淋巴瘤(LBCL)!
来源:本站原创 2021-10-15 20:07
今年6月,Yescarta(阿基仑赛注射液,奕凯达)获批,是第一个在中国上市的CAR-T细胞疗法。
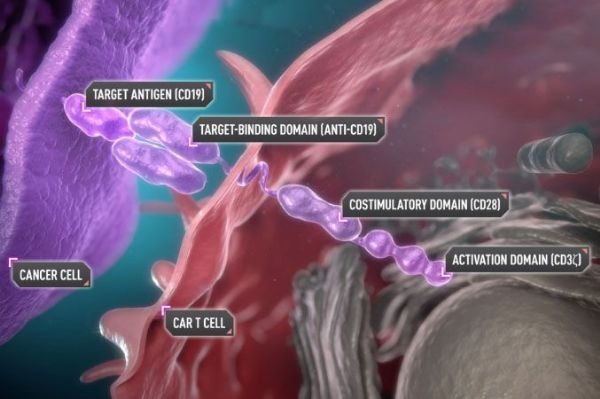
Yescarta作用机制(图片来源:yescartahcp.com)
2021年10月15日讯 /生物谷BIOON/ --吉利德(Gilead)旗下细胞治疗公司凯特制药(Kite Pharma)近日宣布,已向美国食品和药物管理局(FDA)提交了CD19 CAR-T细胞疗法Yescarta(Axicabtagene Ciloleucel,Axi-Cel)的一份补充生物制品许可申请(sBLA),以扩大其目前的适应症:纳入二线治疗复发或难治性大B细胞淋巴瘤(LBCL)成人患者。如果获得批准,Yescarta将成为第一个用于先前一线治疗后复发或一线治疗无效的LBCL成人患者的CAR-T细胞疗法。
此次sBLA基于里程碑ZUMA-7研究的结果,该研究是第一项在二线治疗中将CAR-T与标准护理(SOC)进行对比的随机临床试验,也是任何3期CAR-T试验中随访数据最长(2年)的一项试验。结果显示,在二线治疗复发或难治性LBCL方面,Yescarta与SOC相比显示出高度统计学意义和临床意义的治疗益处。
由于癌症复发或对治疗方案变得无效,大约40%的LBCL患者需要二线治疗。二线R/R LBCL的标准护理分为2步:重新引入免疫化疗,如果患者有反应并能耐受进一步治疗,则继续进行大剂量化疗和干细胞移植。里程碑ZUMA-7研究的顶线结果描绘了治疗LBCL的潜在范式转变。该研究显示,在一线化疗后病情复发或难治的LBCL患者中,与长期的二线标准护理(化疗和巩固性自体移植)相比,接受单次输注Yescarta的患者,预后有显著改善。
ZUMA-7是一项随机、开放标签、全球性、多中心3期研究,在二线复发或难治性大B细胞淋巴瘤(2nd-line R/R LBCL)成人患者中开展,将Yescarta(一次性输注)与现行标准护理(SOC:化疗+干细胞移植)进行了对比。ZUMA-7研究于2017年启动,在全球77个中心招募了359名患者(年龄范围:22岁至81岁),其中30%的患者年龄在65岁或以上。该研究的主要终点是无事件生存期(EFS),定义为从随机分组到疾病进展、开始新的淋巴瘤治疗或因任何原因死亡的时间。ZUMA-7研究是根据与美国FDA达成的一项特别协议(SPA)开展的,根据该协议,试验设计、临床终点和统计分析事先与FDA达成一致。
来自ZUMA-7试验的结果代表着二线R/R LBCL方面最长的随访时间,中位随访时间为2年。结果显示,研究达到了EFS主要终点:Yescarta与SOC相比在二线R/R LBCL治疗方面显示出优越性,将EFS事件风险降低了60%(HR=0.398,p<0.0001),具有临床意义。此外,该研究也达到了客观缓解率(ORR)关键次要终点。对总生存期(OS)的中期分析显示有利于Yescarta的趋势,但目前数据还不成熟,计划在未来开展进一步分析。
该研究的安全性结果与Yescarta三线治疗LBCL的已知安全性相一致或更低。6%的患者出现3级或更高级别的细胞因子释放综合征(CRS),中位发病时间为3天,21%的患者出现3级或更高级别的神经事件(NE)。二线治疗中没有发现新的安全问题。
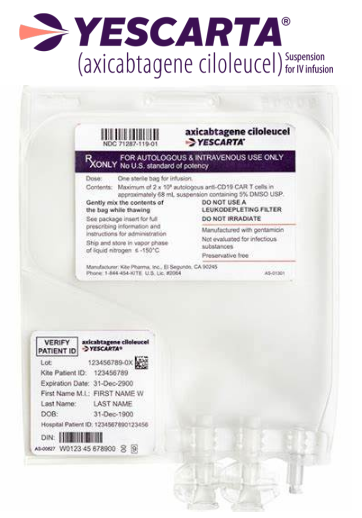
Yescarta(Axicabtagene Ciloleucel,Axi-Cel)是一款CD19 CAR-T细胞疗法,由吉利德豪掷119亿美元收购Kite获得。在美国,Yescarta于2017年10月获FDA批准,是第一个治疗复发或难治性大B细胞淋巴瘤(R/R LBLC)成人患者的CAR-T细胞疗法。
2021年3月,Yescarta获FDA批准一个新的适应症:用于治疗先前已接受过2种或多种系统疗法的复发性或难治性(R/R)滤泡性淋巴瘤(FL)成人患者。根据这项最新批准,Yescarta是第一款被批准用于治疗FL的CAR-T细胞疗法。
在中国,今年6月,国家药品监督管理局(NMPA)通过优先审评审批程序批准复星凯特生物科技有限公司(FOSUN Kite)申报的阿基仑赛注射液 (商品名:奕凯达)上市。该药品为我国首个批准上市的细胞治疗类产品,用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者(包括弥漫性大B细胞淋巴瘤非特指型、原发纵膈大B细胞淋巴瘤、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的弥漫性大B细胞淋巴瘤)。
阿基仑赛注射液(奕凯达)是根据凯特制药Yescarta(Axicabtagene Ciloleucel,Axi-Cel)经技术转移并拟在中国境内(不包括港澳台)进行本地化生产。该产品由复星凯特从凯特制药引进、获得在中国大陆、香港特别行政区和澳门特别行政区的技术及商业化权利。
该产品是复星凯特在中国推进商业化的第一个CAR-T细胞治疗产品,也是国家药品监督管理局(NMPA)正式批准上市的第一个CAR-T细胞治疗产品。作为一种全新的肿瘤治疗手段,阿基仑赛注射液(奕凯达)能够为中国接受了二线或以上系统性治疗后复发或难治的大B细胞淋巴瘤患者带来新生的希望和机会。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->