白血病(CLL)新药!阿斯利康BTK抑制剂Calquence单药一线治疗4年总缓解率(ORR)高达97%!
来源:本站原创 2020-06-14 16:27
Calquence单药一线治疗初治CLL患者4年总缓解率(ORR)高达97%、治疗复发/难治CLL患者18个月生存率高达88%,并显示出长期的良好安全性。

2020年06月14日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)近日在欧洲血液学协会(EHA)第25届年会上公布了靶向抗癌药Calquence(acalabrutinib)一线单药治疗慢性淋巴细胞白血病(CLL)患者II期单臂ACE-CL-001试验的详细结果,以及Calquence治疗复发或难治性CLL患者III期ASCEND试验的长期疗效和耐受性数据。结果显示,Calquence单药一线治疗初治CLL患者4年总缓解率(ORR)高达97%、治疗复发/难治CLL患者18个月生存率高达88%,并显示出长期的良好安全性。
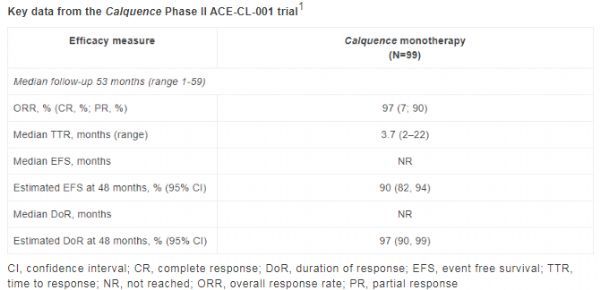
ACE-CO-001试验在先前未治疗的CLL患者中开展,调查了Calquence(100mg每日2次[n=62],或200mg每日一次[n=37])的疗效和安全性。在2015年5月1日,接受200mg给药方案的患者改为100mg给药方案。
数据显示,中位随访超过4年(4.4年),有86%的CLL患者仍在接受Calquence作为一线单药治疗。数据显示,总缓解率(ORR)为97%(完全缓解率[CR]=7%,部分缓解率[PR]=90%),在具有高危疾病特征的亚组患者中ORR为100%,包括基因组畸变(17p缺失[n=9]和TP53突变[n=9])、免疫球蛋白突变状态(未突变IGHV[n=57])、复杂核型(n=12)。所有患者(n=97)的淋巴结疾病均减少。安全性结果显示没有新的长期问题。
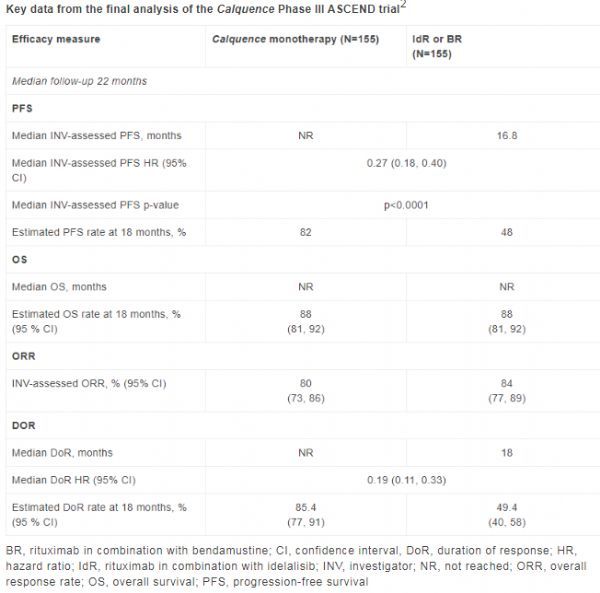
ASCEND研究是一项全球性、随机、多中心、开放标签III期试验,在复发或难治性(R/R)CLL患者中开展,调查了Calquence(100mg,每日2次)与研究员选择的利妥昔单抗联合idelalisib(IdR)方案或利妥昔单抗联合苯达莫司汀(BR)方案的疗效和安全性。
该研究的最终分析显示:治疗第18个月时,Calquence治疗组估计有82%的CLL患者仍存活且无疾病进展,而利妥昔单抗联合idelalisib或苯达莫司汀治疗的患者中比例估计为48%。详细结果如下:
威尔康奈尔医学院CLL研究中心主任Richard R.Furman表示:“这些数据表明Calquence没有新的安全性问题,并证实了该药能够安全地为初治(一线治疗)、复发或难治性CLL患者提供有意义的长期临床益处。Calquence将为CLL患者群体提供一个重要而合理的治疗选择。”
阿斯利康肿瘤研发执行副总裁José Baselga表示:“这些长期数据重申,Calquence将为CLL患者提供一个具有良好安全性的持久缓解。CLL患者通常是70岁或70岁以上的合并症患者,而且往往需要长期治疗,这使得持续的安全性和有效性与他们的生活质量高度相关。”
II期ACE-CL-001试验的结果为关键III期ELEVATE TN试验的开展提供了依据,该试验与III期ASCEND试验的结果一起,奠定了美国FDA批准Calquence治疗CLL或小淋巴细胞淋巴瘤(SLL)的基础。
Calquence:年销售额有望超过50亿美元的BTK抑制剂
Calquence的活性药物成分为acalabrutinib,这是一种高度选择性、强效、共价Bruton酪氨酸激酶(BTK)抑制剂,通过永久性结合抑制BTK发挥作用。BTK是B细胞受体(BCR)信号通路的关键调节因子,在不同类型血液系统恶性肿瘤中广泛表达,参与B细胞的增殖、运输、趋化和粘附,因此是治疗血液系统恶性肿瘤的重要靶点。在临床前研究中,acalabrutinib表现出极小的脱靶效应。
Calquence于2017年10月获美国FDA加速批准上市,当前适应症包括:(1)用于既往已接受至少一种疗法的复发性或难治性套细胞淋巴瘤(MCL)成人患者;(2)治疗CLL/SLL成人患者。目前,Calquence正被开发用于多种B细胞血液癌症,包括CLL、MCL、弥漫性大B细胞淋巴瘤、Waldenstrom巨球蛋白血症(WM)、滤泡性淋巴瘤(FL)、多发性骨髓瘤及其他血液学恶性肿瘤。阿斯利康对Calquence的商业期望极高,预期该药的销售峰值可达到50亿美元!
Calquence的作用机制与艾伯维/强生的重磅血癌药物Imbruvica(ibrutinib,依鲁替尼)相同,后者是全球获批的首个BTK抑制剂。自2013年11月首次获批以来,截至目前,Imbruvica已获批6种疾病领域多达10个治疗适应症,全球销售额呈直线上升。医药市场调研机构EvaluatePharma此前发布报告预测,在2024年,Imbruvica的全球销售额将达到95亿美元,成为全球第五大畅销药。(生物谷Bioon.com)
原文出处:Calquence showed long-term efficacy and tolerability for patients with chronic lymphocytic leukaemia in two trials
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->