近期科学家们在阿尔兹海默病研究领域取得的新成果!
来源:本站原创 2021-05-30 23:01
《世界阿尔兹海默症2018年报告》显示,全球大约每3秒就有一位痴呆症患者,全球目前至少有5,000万痴呆患者,预计2050年这个数字将达到1.5亿;其中,有约60%-70%为阿尔兹海默症患者。截至2019年,中国阿尔兹海默症患病人数超过1000万,是全球阿尔兹海默症(AD)患者数量最多的国家。近年来,科学家们 在阿尔兹海默病研究领域进行了大量研究,本文中,小
《世界阿尔兹海默症2018年报告》显示,全球大约每3秒就有一位痴呆症患者,全球目前至少有5,000万痴呆患者,预计2050年这个数字将达到1.5亿;其中,有约60%-70%为阿尔兹海默症患者。截至2019年,中国阿尔兹海默症患病人数超过1000万,是全球阿尔兹海默症(AD)患者数量最多的国家。近年来,科学家们 在阿尔兹海默病研究领域进行了大量研究,本文中,小编就整理了近期他们在阿尔兹海默病研究领域取得的新成果!分享给大家!
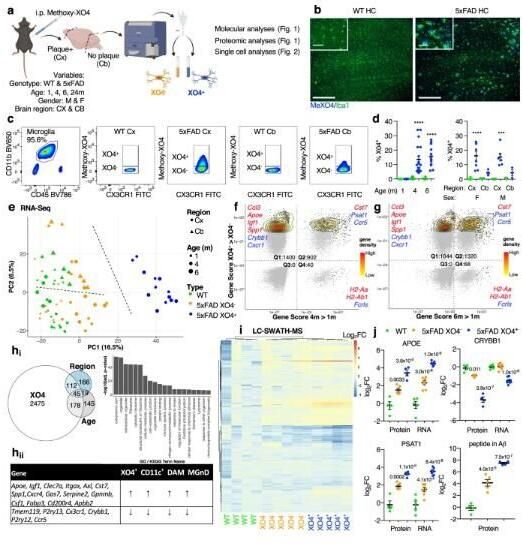
甲氧基-XO4能在5xFAD小鼠机体中标记了分子不同的噬菌体群体。
图片来源:Grubman, A., et al. Nat Commun 12, 3015 (2021).doi:10.1038/s41467-021-23111-1
【1】Nat Commun:科学家发现阿尔兹海默病发病过程中负责摄入淀粉样斑块的小胶质细胞的关键基因特征
doi:10.1038/s41467-021-23111-1
小胶质细胞是大脑中的专业免疫哨兵细胞,其会对“陌生人”或危险信号作出反应,并帮助清除细胞和胞外碎片,帮助调节突触的可塑性、成熟和移除等,因此,小胶质细胞的功能对于大脑的生理过程至关重要;目前研究人员已经阐明了小胶质细胞在阿尔兹海默病发病过程中扮演的关键角色,然而并不清楚其分子和功能的多样性。
阿尔兹海默病是一种最常见的痴呆症,其特征是大脑中淀粉样斑块的积累,作为大脑中的免疫哨兵,小胶质细胞并不仅仅负责消除外来的入侵者,其还能通过清除诸如淀粉样斑块等毒性废物来帮助维持大脑的平衡。日前,一篇刊登在国际杂志Nature Communications上题为“Transcriptional signature in microglia associated with Aβ plaque phagocytosis”的研究报告中,来自莫纳什大学等机构的科学家们通过研究发现了与淀粉样斑块吞噬作用(即吞噬大脑中的淀粉样β蛋白沉积物)相关的小胶质细胞的基因表达特征,相关研究结果或能提供一种新靶点帮助开发新型干预措施,来解决这种不治之症的潜在疾病机制。
研究人员在阿尔兹海默病临床前模型研究中使用了这种染色剂,随后分析了被染色的小胶质细胞中的基因表达情况,此外他们还调查了小胶质细胞摄取诸如淀粉样斑块的能力背后的基因表达差异,同时还识别出了相关的调节性分子。研究者Jose M. Polo教授指出,理解这一机制非常重要,因为如今我们拥有多个靶点值得深入探究,这些靶点或有望帮助开发治疗诸如阿尔兹海默病等毁灭性疾病的新型疗法。
Hif1a与阿尔兹海默病患者认知功能下降之间的关联目前还并未被完全阐明,后期研究人员将会继续深入研究利用基因编辑工具CRISPR来检测调节Hif1a基因对患者疾病的严重程度和疾病的进展所产生的影响。综上,本文研究结果为阐明小胶质细胞在阿尔兹海默病发病过程中功能多样性背后潜在的分子机制提供了新的线索和思路。
【2】ADDADM:牙龈细菌的生态失衡或与阿尔兹海默病生物标志物直接相关
doi:10.1002/dad2.12172
牙周病(PerioD,Periodontal disease)是一种口腔中发生的慢性炎症性的菌群失调疾病,其影响着50%以上的老年人的健康;同时研究人员发现,牙周病或许与阿尔兹海默病和唐氏综合征的发生均有关联。近日,一篇发表在国际杂志Alzheimer's & Dementia: Diagnosis, Assessment & Disease Monitoring上题为“Periodontal dysbiosis associates with reduced CSF Aβ42 in cognitively normal elderly”的研究报告中,来自纽约大学等机构的科学家们通过研究通过研究发现,牙龈细菌的失衡或许与阿尔兹海默病的生物标志物直接相关。研究者表示,牙龈中有害细菌多于健康细菌的的老年人或许更有可能在其脑脊液中出现β淀粉样蛋白,即阿尔兹海默病的关键生物标志物,然而,口腔菌群的这种失衡或许与另外一种名为tau的阿尔兹海默病生物标志物并无关联。
本文研究增加了证据表明牙周病(牙龈疾病)与阿尔兹海默病之间或存在着非常紧密的关联,据美国CDC数据显示,牙周病在美国影响着70%的65岁及以上的老年人,牙周病的主要特点为机体慢性系统性炎症,主要表现为牙齿和牙龈之间的“小袋结构”不断扩大并会滋养细菌。研究者Angela Kamer博士表示,本文研究中我们在认知功能正常的老年人群中首次发现了,牙龈下不平衡的细菌群罗与阿尔兹海默病脑脊液生物标志物之间存在一定的关联。口腔既是促进炎症的有害细菌生存的场所,也是保护性细菌栖息的地方;研究者发现证据表明,大脑中淀粉样蛋白的存在或与有害细菌的增加及有益细菌水平的下降有关。
综上,本文研究揭示了牙周病患者口腔菌群的生态失衡与淀粉样病变的脑脊液生物标志物之间或许存在一定的选择性关系,后期还需要进一步建模研究来建立口腔菌群与大脑中β淀粉样蛋白之间的直接关联。此外,研究者还指出,本文研究并未发现牙龈细菌与tau蛋白水平之间的关联,他们并不清楚是否tau蛋白病变后期会发生或者受试者后期会出现阿尔兹海默病的症状,这就需要后期研究人员进一步进行纵向研究和临床试验来分析是否改善牙龈健康就能够修饰大脑中的淀粉样蛋白并有效预防阿尔兹海默病的发生,比如深层清除牙龈下的斑块和牙垢沉积物等。
【3】Cell Stem Cell:靶向miR-132有望让阿尔茨海默病患者的大脑返老还童
doi:10.1016/j.stem.2021.05.001
AD是仅次于心脏病、肿瘤和中风而导致死亡的第四大疾病,已成为人类目前和未来所面临的全球公共卫生和社会保健的最大挑战之一。目前的治疗策略不能预防、减缓或治愈这种病理。在一项新的研究中,来自荷兰神经科学研究所的研究人员鉴定出一种称为miR-132的小RNA分子,它可以用来使AD模型动物的大脑返老还童并抵消记忆丧失。相关研究结果于2021年5月24日在线发表在Cell Stem Cell期刊上,论文标题为“Restoring miR-132 expression rescues adult hippocampal neurogenesis and memory deficits in Alzheimer’s disease”。
在这项研究中,这些作者着手解决miR-132是否能调节健康大脑和AD大脑的海马体中的成体神经发生。利用不同的AD小鼠模型、体外培养的人类神经干细胞和死后的人类大脑组织,他们发现这种小RNA分子对成年海马体的神经发生过程是必需的。降低成年小鼠大脑或培养皿中人类神经干细胞中的miR-132水平会损害新神经元的生成。然而,在AD小鼠中恢复miR-132的水平可以拯救神经发生缺陷,并抵消与成体神经发生缺陷有关的记忆损伤。这些作者为开发恢复AD中的成体神经发生的潜在疗法提供了一个概念验证。这些作者的下一个目标是系统地评估靶向miR-132作为AD治疗策略的有效性和安全性。
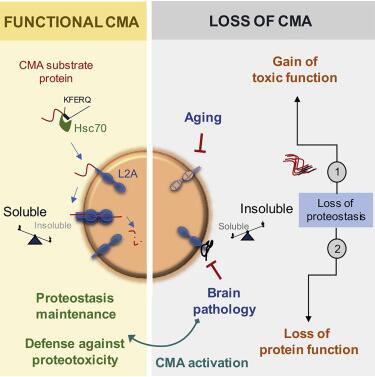
激活CMA可维持蛋白稳态和抵抗蛋白毒性。
图片来源:Cell, 2021, doi:10.1016/j.cell.2021.03.048。
【4】Cell:重大进展!实验性药物CA激活分子伴侣介导的自噬,有潜力治疗阿尔茨海默病
doi:10.1016/j.cell.2021.03.048
在一项新的研究中,来自美国阿尔伯特-爱因斯坦医学院的研究人员设计出一种实验性药物,它可以在小鼠体内逆转阿尔茨海默病的关键症状。该药物通过重新激活一种消化和循环利用不需要的蛋白以去除它们的细胞清理机制而起作用。相关研究结果于2021年4月22日在线发表在Cell期刊上,论文标题为“Chaperone-mediated autophagy prevents collapse of the neuronal metastable proteome”。
这些作者首先研究了CMA受损是否会导致阿尔茨海默病。为此,他们对小鼠进行了基因改造,使之具有缺乏CMA的兴奋性大脑神经元。这种脑细胞中的CMA缺失足以导致短期记忆丧失、行走障碍,以及在阿尔茨海默病的啮齿类动物模型中经常发现的其他问题。此外,CMA的缺失极大地破坏了蛋白稳态(proteostasis)---细胞调节它们所含蛋白的能力。正常情况下可溶性的蛋白已经转变为不可溶性,并有风险形成有毒的聚集物。
重要的是,这两种小鼠模型都已经出现了疾病症状,它们的神经元在用药之前就已经被有毒的蛋白堵塞了。这意味着该药物可能有助于保护神经元的功能,即便在这种疾病的后期阶段。这些作者还感到非常兴奋的是,该药物显著减少了胶质增生(gliosis),即大脑神经元周围细胞的炎症和瘢痕形成。胶质增生与有毒的蛋白有关,并且已知在延续和恶化神经退行性疾病方面起着重要作用。用CA治疗似乎并不损害其他器官,即使在较长长时间内每天给药也是如此。这些作者目前正在开发CA及其相关化合物,用于治疗阿尔茨海默病和其他神经退行性疾病。
【5】Nat Immunol:发现治疗阿尔茨海默病的Tam-ping淀粉样蛋白
doi:10.1038/s41590-021-00918-0
TAM受体激酶Axl和Mer在阿尔茨海默病转基因模型中对小胶质细胞识别和清除积聚的淀粉样蛋白起关键作用。基于此,Katrin I Andreasson 教授团队在Nature Immunology 期刊上发表题为“TAM-ping down amyloid in Alzheimer’s disease”的评论论文,重点解读了小胶质细胞如何在阿尔茨海默病(AD)影响的大脑中导航并与β淀粉样蛋白(Aβ)斑块结合。
Aβ肽是Aβ斑块的主要成分,由淀粉样前体蛋白(app)的连续裂解产生,并释放到细胞外空间,其中其单体以β-折叠构象聚集,形成高阶组装体,如低聚物、原纤维和原纤维。小胶质细胞吞噬Aβ肽,最近有人认为这一过程可能是Aβ作为斑块沉积所必需的。这种反应部分依赖于受体TREM2,它使小胶质细胞包围并压缩Aβ斑块。然而,对小胶质细胞调节Aβ斑块沉积的确切机制的了解还很缺乏。
综上所述,小胶质细胞利用TAM受体酪氨酸激酶Axl和Mer寻找并吞噬Aβ斑块。该研究团队证明,在AD淀粉样沉积的临床前模型中,TAM受体及其配体与修饰aβ斑块的磷脂酰丝氨酸形成桥。TAM受体的基因消融使小胶质细胞检测、吞噬和致密Aβ斑块的能力丧失。
【6】Science子刊:新研究揭示为何APOE4会增加阿尔茨海默病的发病风险
doi:10.1126/scitranslmed.aaz4564
载脂蛋白E基因(APOE)的E4等位基因(APOE4)已被确定为包括心血管疾病和阿尔茨海默病(AD)在内的多种疾病的遗传风险因素,但其作用机制仍不甚明了。APOE是一种脂质运输蛋白,脂质的失调最近已成为包括AD在内的几种神经退行性疾病的主要特征。然而,目前尚不清楚APOE4是如何扰乱细胞内脂质状态的。在一项新的研究中,来自美国麻省理工学院等研究机构的研究人员利用来自APOE4或APOE3携带者的成纤维细胞构建出人诱导性多能干细胞(iPSC),随后诱导人iPSC分化产生星形胶质细胞,基于此发现人ipsC分化产生的星形胶质细胞的细胞脂质组(lipidome)是由APOE4而不是APOE3破坏的,此外表达人APOE异构体的酵母细胞脂质组也是由APOE4而不是APOE3破坏的。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“APOE4 disrupts intracellular lipid homeostasis in human ipsC-derived glia”。
这项研究阐明了脂质代谢中的关键分子干扰,这些干扰可能导致与APOE4基因型相关的疾病风险。这项研究还表明,操纵脂质代谢可能是一种治疗方法,有助于减轻与APOE4等位基因相关的疾病风险。
【7】Hypertension:夜间血压高于白天或会增加个体患阿尔兹海默病的风险
doi:10.1161/HYPERTENSIONAHA.120.16711
近日,一项刊登在国际杂志Hypertension上的研究报告中,来自乌普萨拉大学等机构的科学家们通过研究表明,夜间机体血压高于白天或许是老年男性患阿尔兹海默病的一个风险因素。痴呆症是一类疾病的总称,其用来描述一类以行为改变和认知及社会能力逐渐下降为特征的症状,包括高血压在内的多种因素或会影响这些症状发生的风险。
在健康状况下,血压会在24小时内发生变化,同时夜间血压水平会达到最低值;临床上将这种夜间血压下降称之为“倾斜”(dipping),然而有些人的血压模式正好相反,其夜间血压要比白天高,这种血压模式称之为“反向倾斜”(reverse dipping)。研究者Christian Benedict教授说道,夜晚是大脑健康的关键时期,比如,在动物机体中,此前研究发现,大脑会在睡眠时帮助清除废弃物,而这种清除或会受到异常血压模式的影响;由于夜晚是人类大脑健康的关键时间窗口,研究人员就想通过研究分析机体在夜间血压过高(正如在反向倾斜中观察到的那样)是否与老年人群痴呆症风险增加有关。
本文中的研究对象仅为年龄较大的男性,因此后期研究人员还需要在老年女性群体中重复该项研究;据研究者介绍,下一步他们将会进一步深入研究调查夜间摄入降血压药物是否能够帮助降低老年男性患阿尔兹海默病的风险。
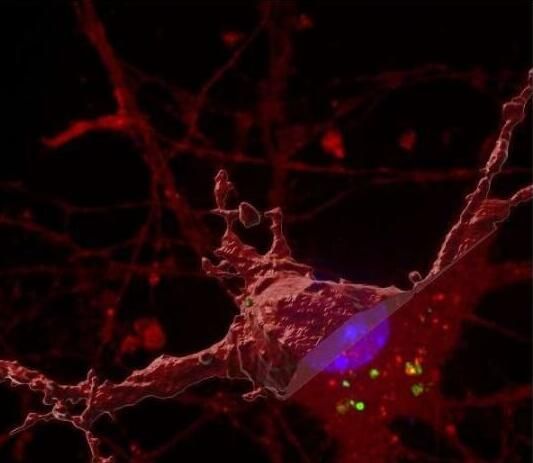
图片来源:Dr. Juan Polanco et. al., The University of Queensland
【8】Acta Neuropathol:揭秘阿尔兹海默病如何通过外泌体来进一步发展?
doi:10.1007/s00401-020-02254-3
日前,一篇刊登在国际杂志Acta Neuropathologica上题为“Exosomes induce endolysosomal permeabilization as a gateway by which exosomal tau seeds escape into the cytosol”的研究报告中,来自昆士兰大学等机构的科学家们通过研究发现,脑细胞中一种新型的“播种”过程或是诱发痴呆症和阿尔兹海默病的原因。研究者表示,作为痴呆症发生的主要标志,缠结的神经元形成的部分原因是因为一种“误入歧途”的细胞过程,其会允许毒性蛋白质tau蛋白渗漏到健康的脑细胞中。这种渗漏会产生一种损伤性的播种过程,其就会促进tau蛋白缠结,最终导致患者记忆缺失和其它损伤。
截至目前为止,科学家们并不理解tau蛋白的种子是如何在进入健康细胞后开始逃逸的;在阿尔兹海默病患者中,似乎细胞内外这种名为外泌体(exosomes)的传递信息的囊状结构能够诱发反应来在自己的细胞膜上穿孔并让有毒的种子逃跑。随着大脑中更多tau蛋白的积累,其最终就会形成缠结结构,聚集在一起就会形成名为淀粉样蛋白的异常配置的蛋白质,最终就会产生这些神经性疾病的关键特征。
最后研究者指出,改善理解阿尔兹海默病和其它疾病通过外泌体扩散的分子机制或能帮助我们开发新方法来治疗并干预这些细胞过程,如今研究人员正在奋力研究观察外泌体和细胞功能障碍是如何作为风险因子在神经变性疾病中扮演关键角色的。
【9】JAD:科学家开发出一种有望有效预防阿尔兹海默病的综合性方法
doi:10.3233/JAD-201059
近日,一项刊登在国际杂志Journal of Alzheimer's Disease上的研究报告中,来自智利大学等机构的科学家们通过研究开发出了一种能有效预防阿尔兹海默病的综合性方法。研究者表示,如今越来越多的研究支持利用综合性的手段来预防阿尔兹海默病,比如将日常锻炼、营养药品、东方实践(比如气功和冥想)和社交生活结合起来的方式。这些健康生活方式元素或能作为早期诊断疾病的可靠生物标志物的补充,从而就能够在疾病症状出现前20年就对人群的阿尔兹海默病尽可能早地发现。
阿尔兹海默病是目前全球医学研究和公共健康系统的主要难题之一,该病在全球影响着近5000万人的健康,其是一种多因素的大脑疾病,以进行性的认知损伤、冷漠和情绪障碍为主要特征,阿尔兹海默病的主要风险因素就是机体衰老。有研究表明,阿尔兹海默病是打破机体正常衰老的一种改变,其还伴随着神经元强大功能及神经元保护机制的变化。衰老过程中功能丧失的决定因素有很多,表观遗传组分就在其中起着重要的作用,因此,通过健康的生活方式、体育锻炼、平衡营养、避免对健康造成伤害的分子和药物,或许就能够减缓介导机体对阿尔兹海默病易感的基因活性;同时在老年期间进行积极性的社会生活和实践活动或许就能实现在老年时获得机体健康。
此外,传统药物疗法治疗的失败和新药的不断寻找刺激了营养化合物在多靶点疗法治疗背景下的出现,同时也证明了非药物治疗方法对改善衰老确实有效,同时还能用于阿尔兹海默病的控制;所有将这些预防性因素与新型多靶点治疗方法结合起来的综合性方法或许都有望为未来控制疾病的发生和进展带来一定希望。
【10】JADR:新发现!肥胖或会加速阿尔兹海默病的疾病效应!
doi:10.3233/ADR-200267
近日,一项刊登在国际杂志Journal of Alzheimer's Disease Reports上的研究报告中,来自谢菲尔德大学等机构的科学家们通过研究发现,过重或许是大脑健康的一种额外负担,其或会加速阿尔兹海默病的发生和影响效应。在这项开创性的多模式神经成像研究中,研究人员发现,肥胖或会导致神经组织的易感性,在轻度阿尔兹海默病患者中维持健康体重或能帮助保护大脑的结构。
本文研究结果还强调了中年时期机体过重对晚年大脑健康所产生的潜在影响;研究者Annalena Venneri说道,目前全球有超过5000万人患有阿尔兹海默病,尽管科学家们进行了几十年的研究,也取得了一定研究成果,但目前全球科学家们依然无法有效治愈这种残酷的疾病。预防措施在抵御这种疾病过程中扮演着关键角色,需要强调的是,本文研究并未标明肥胖会诱发阿尔兹海默病,但其确实表明,处于过重状态是一种大脑健康的额外负担,也会恶化加剧阿尔兹海默病。
能够诱发痴呆症的疾病,比如阿尔兹海默病和血管性痴呆症能够潜伏多年,所以等到60岁时再减肥就已经太晚了;如今我们开始考虑大脑健康了并尽可能早地预防相关疾病的发生。而且教育儿童和青少年关于超重对包括神经变性疾病在内的多种疾病的负担也是至关重要。在阿尔兹海默病的早期阶段,体重减轻往往是最初的症状之一,因为人们容易忘记东西,或者开始吃东西,比如饼干或薯片等易拿的零食,而并非有营养的食物;研究者发现,保持健康的体重或有助于保护那些已经经历轻度阿尔兹海默病痴呆症患者机体的大脑结构,并不像诸如心血管疾病或糖尿病等其它疾病,人们通常并不会考虑营养与神经系统症状之间的关联和重要性,但这些研究结果表明,营养或许有助于保存大脑的结构。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


