Nat Biotechnol:利用改造的锤头状核酶控制AAV病毒载体中的基因表达
来源:本站原创 2020-03-08 23:20
2020年3月8日讯/生物谷BIOON/---使用腺相关病毒(AAV)载体进行瞬时或间歇性基因转移所面临的一种限制是缺乏适合临床表达的遗传开关。特别是,在基因转移出现问题的情况下,在AAV载体中引入关闭开关可以抑制转基因表达。当前的方法基于蛋白开关,这就使得它们可能被免疫系统识别为非自身的,并且它们的尺寸进一步减小了AAV载体中已经有限的可用空间。在一项新的
2020年3月8日讯/生物谷BIOON/---使用腺相关病毒(AAV)载体进行瞬时或间歇性基因转移所面临的一种限制是缺乏适合临床表达的遗传开关。特别是,在基因转移出现问题的情况下,在AAV载体中引入关闭开关可以抑制转基因表达。当前的方法基于蛋白开关,这就使得它们可能被免疫系统识别为非自身的物质,并且它们的尺寸进一步减小了AAV载体中已经有限的可用空间。
在一项新的研究中,来自美国斯克里普斯研究所、中国北京大学深圳研究生院、深圳湾实验室化学生物学研究所和哈尔滨医科大学的研究人员提出了一种替代性方法。他们使用核酶(ribozyme)---一种较小的核糖核酸(RNA),可作为非常特殊的酶发挥作用---来控制AAV基因转移环境中的转基因表达。具体来说,他们对III型锤头状核酶(hammerhead ribozyme)进行改造来改善它的酶活性。当此类核酶包含在RNA链中时,它们会特异性地切割这种RNA链。当这种切割发生在mRNA的3'非翻译区时,它会导致mRNA降解并减少蛋白合成。相关研究结果近期发表在Nature Biotechnology期刊上,论文标题为“A reversible RNA on-switch that controls gene expression of AAV-delivered therapeutics in vivo”。
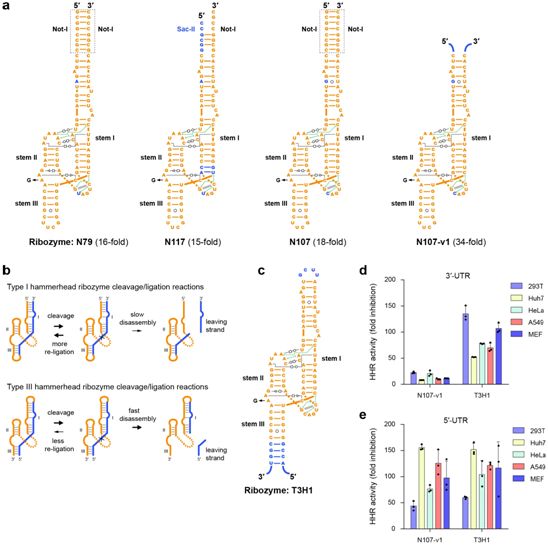
这些研究人员利用这一有趣的特性开发出一种适用于AAV基因转移的关闭开关。他们将原始的锤头状核酶进行改造,使得与其他的核酶(开关开启)相比,它们的改造版本在降低转基因表达方面的活性提高了60~80倍。他们随后开发出一种方法来干扰这种开关并诱导转基因表达(开关关闭)。他们使用了磷酸二氨基酯吗啉代低聚物(phosphorodiamidate morpholino oligomer),即一类已被批准用于治疗神经肌肉疾病的寡核苷酸。在测试了不同的磷酸二氨基酯吗啉代低聚物之后,他们鉴定出一种变体能够将体外培养的细胞中的基因表达提高300倍。重要的是,当他们将这种锤头状核酶与这种磷酸二氨基酯吗啉代低聚物变体的组合使用进行测试时,他们让小鼠腓肠肌中的转基因表达增加了10到100倍。
这项研究报道了一个重要的研究进展,这是因为它为控制基因转移环境中的转基因表达提供了新的分子工具。这种方法的一个可能的局限性是当静脉注射时,这种磷酸二氨基酯吗啉代低聚物变体无法很好地递送至肌肉中。不过,使用不同的吗啉代化学物可能是一种解决此限制的潜在方法。尽管还需开展进一步的测试,但是这种方法极大地增强了锤头状核酶的动态范围,而且当磷酸二氨基酯吗啉代低聚物联合使用时,它们代表着一类开启转基因表达的独特工具。(生物谷 Bioon.com)
参考资料:
1.Guocai Zhong et al. A reversible RNA on-switch that controls gene expression of AAV-delivered therapeutics in vivo. Nature Biotechnology, 2019, doi:10.1038/s41587-019-0357-y.
2.Giuseppe Ronzitti. Let’s switch on AAV!. Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aba9016.
在一项新的研究中,来自美国斯克里普斯研究所、中国北京大学深圳研究生院、深圳湾实验室化学生物学研究所和哈尔滨医科大学的研究人员提出了一种替代性方法。他们使用核酶(ribozyme)---一种较小的核糖核酸(RNA),可作为非常特殊的酶发挥作用---来控制AAV基因转移环境中的转基因表达。具体来说,他们对III型锤头状核酶(hammerhead ribozyme)进行改造来改善它的酶活性。当此类核酶包含在RNA链中时,它们会特异性地切割这种RNA链。当这种切割发生在mRNA的3'非翻译区时,它会导致mRNA降解并减少蛋白合成。相关研究结果近期发表在Nature Biotechnology期刊上,论文标题为“A reversible RNA on-switch that controls gene expression of AAV-delivered therapeutics in vivo”。

图片来自Nature Biotechnology, 2019, doi:10.1038/s41587-019-0357-y。
这些研究人员利用这一有趣的特性开发出一种适用于AAV基因转移的关闭开关。他们将原始的锤头状核酶进行改造,使得与其他的核酶(开关开启)相比,它们的改造版本在降低转基因表达方面的活性提高了60~80倍。他们随后开发出一种方法来干扰这种开关并诱导转基因表达(开关关闭)。他们使用了磷酸二氨基酯吗啉代低聚物(phosphorodiamidate morpholino oligomer),即一类已被批准用于治疗神经肌肉疾病的寡核苷酸。在测试了不同的磷酸二氨基酯吗啉代低聚物之后,他们鉴定出一种变体能够将体外培养的细胞中的基因表达提高300倍。重要的是,当他们将这种锤头状核酶与这种磷酸二氨基酯吗啉代低聚物变体的组合使用进行测试时,他们让小鼠腓肠肌中的转基因表达增加了10到100倍。
这项研究报道了一个重要的研究进展,这是因为它为控制基因转移环境中的转基因表达提供了新的分子工具。这种方法的一个可能的局限性是当静脉注射时,这种磷酸二氨基酯吗啉代低聚物变体无法很好地递送至肌肉中。不过,使用不同的吗啉代化学物可能是一种解决此限制的潜在方法。尽管还需开展进一步的测试,但是这种方法极大地增强了锤头状核酶的动态范围,而且当磷酸二氨基酯吗啉代低聚物联合使用时,它们代表着一类开启转基因表达的独特工具。(生物谷 Bioon.com)
参考资料:
1.Guocai Zhong et al. A reversible RNA on-switch that controls gene expression of AAV-delivered therapeutics in vivo. Nature Biotechnology, 2019, doi:10.1038/s41587-019-0357-y.
2.Giuseppe Ronzitti. Let’s switch on AAV!. Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aba9016.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


