2020年12月Cell期刊不得不看的亮点研究
来源:本站原创 2020-12-31 07:23
2020年12月31日讯/生物谷BIOON/---2020年12月份即将结束了,12月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell论文解读!新方法首次详细揭示核孔复合物的组装过程doi:10.1016/j.cell.2020.11.001在一项新的研究中,来自瑞士苏黎世联邦理工学院和挪威卑尔根大学的研究人员开发出一种
2020年12月31日讯/生物谷BIOON/---2020年12月份即将结束了,12月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell论文解读!新方法首次详细揭示核孔复合物的组装过程
doi:10.1016/j.cell.2020.11.001
在一项新的研究中,来自瑞士苏黎世联邦理工学院和挪威卑尔根大学的研究人员开发出一种方法,使得他们能够首次详细研究大型蛋白复合物的组装过程。作为他们的案例研究,他们选择了最大的细胞复合物之一:酵母细胞中的核孔复合物。相关研究结果近期发表在Cell期刊上,论文标题为“Maturation Kinetics of a Multiprotein Complex Revealed by Metabolic Labeling”。论文通讯作者为苏黎世联邦理工学院的Karsten Weis和Evgeny Onischenko。

这些研究人员将他们的新方法称为KARMA(kinetic analysis of incorporation rates in macromolecular assemblies, 高分子组装中掺入速率的动力学分析),该方法是基于研究代谢过程的方法构建出来的。研究代谢的科学家们长期以来一直在他们的研究工作中使用放射性碳,例如,标记葡萄糖分子,然后细胞吸收并代谢放射性碳。这种放射性标记使得人们能够追踪葡萄糖分子或其代谢物出现的位置和时间点。
2.Cell论文详解!挑战常规!染色质既不是固体也不是液体,而是更像一种凝胶
doi:10.1016/j.cell.2020.11.027
基因组生物学中一个自DNA发现以来一直困扰着科学家们的基本问题:在我们的细胞核内, DNA和蛋白的复杂包裹物(即染色质)是固体还是液体?在一项新的研究中,来自加拿大阿尔伯塔大学和美国科罗拉多州立大学的研究人员找到了这个问题的答案。他们发现染色质既不是固体也不是液体,而是更像一种凝胶。相关研究结果近期发表在Cell期刊上,论文标题为“Condensed Chromatin Behaves like a Solid on the Mesoscale In Vitro and in Living Cells”。论文通讯作者为阿尔伯塔大学肿瘤学系教授Michael Hendzel和科罗拉多州立大学的Jeffrey Hansen。
Hendzel说,以前,生物化学等领域是在染色质和细胞核的其他组分以液体状态运行的假设下进行的。这种对染色质物理特性的新理解挑战了这种观点法,并可能导致对基因组如何编码和解码的更准确理解。
3.Cell:淋巴结受一种独特的具有免疫调节潜能的感觉神经元支配
doi:10.1016/j.cell.2020.11.028
长期以来,神经系统和免疫系统一直被认为是身体中的独立实体,但是一项新的研究发现了这两者之间的直接细胞相互作用。来自哈佛医学院、布罗德研究所和拉根研究所的研究人员发现,痛觉神经元围绕在小鼠淋巴结周围,可以调节这些淋巴结的活动,而淋巴结是免疫系统的关键部分。相关研究结果近期发表在Cell期刊上,论文标题为“Lymph nodes are innervated by a unique population of sensory neurons with immunomodulatory potential”。
这项新研究揭示了介导神经系统和免疫系统之间交谈的细胞。它还为更多关于神经系统如何调节免疫反应的研究铺平了道路。
4.Cell重磅解读!肥胖损伤免疫细胞功能并加速肿瘤生长的分子机制!
doi:10.1016/j.cell.2020.11.009
肥胖与十几种不同类型的癌症风险增加有关,同时也与患者的预后和生存率下降直接相关。多年来,科学家们已经识别出驱动肿瘤生长的肥胖相关的过程,比如代谢改变和慢性炎症等,但他们并未详细阐明肥胖和癌症之间的具体相互作用。近日,一项刊登在国际杂志Cell上题为“Obesity Shapes Metabolism in the Tumor Microenvironment to Suppress Anti-Tumor Immunity”的研究报告中,来自哈佛医学院等机构的科学家们通过研究揭开了这一谜题,研究者发现,肥胖会促进癌细胞在争夺能量的战斗中战胜杀死肿瘤的免疫细胞。
研究者表示,高脂肪饮食会降低肿瘤中的CD8+ T细胞的数量和抗肿瘤活性,之所以出现这种情况,是因为癌细胞为了应对脂肪供应的增加而重编程自身的代谢,从而更好地吞噬富含能量的脂肪分子,并剥夺了T细胞的燃料,并能加速肿瘤的生长。研究者Marcia Haigis说道,将相同的肿瘤放在肥胖和非肥胖的环境中,就能够揭示癌细胞会应对高脂肪饮食而对其细胞代谢重新布线;相关研究结果表明,在某种环境中可能有效的疗法或许在另一种环境中不那么有效,鉴于目前肥胖在人群中的流行,或许就需要科学家们进一步研究理解了。阻断脂肪相关的代谢重编程或能明显减少高脂肪饮食的小鼠机体的肿瘤体积,由于CD8+ T细胞是免疫疗法激活宿主机体免疫系统抵御癌症的主要武器,本文研究中,研究人员提出了改进此类疗法的新型策略。癌症免疫疗法能给癌症患者的生活产生巨大影响,但并非每名患者都能获益。如今研究人员知道随着肥胖改变,T细胞和肿瘤细胞之间存在着新陈代谢的拉锯战, 本文研究或许就提供了探索这种相互作用的路线图,这或能帮助我们开始以新的方式思考癌症免疫疗法和联合疗法的作用机制。
5.Cell论文详解!我的命运我主宰,而细胞中的RNA分子也是如此
doi:10.1016/j.cell.2020.11.030
科学家们对转录是如何开始的有了很好的了解:称为RNA聚合酶的蛋白被招募到DNA分子的特定区域,并开始沿DNA链移动,边走边合成mRNA分子。但是,这个过程的一部分还不太清楚:细胞如何知道何时停止转录?
如今,在一项新的研究中,美国怀特海德生物医学研究所成员、麻省理工学院生物学教授Richard Young及其团队和麻省理工学院化学工程教授Arup K. Chakraborty及其团队发现RNA分子通过反馈回路调节它们自身的形成。RNA分子太少,细胞就会启动转录以产生更多的RNA分子。然后,在某个阈值,过多的RNA分子会导致转录停止。相关研究结果于2020年12月16日在线发表在Cell期刊上,论文标题为“RNA-Mediated Feedback Control of Transcriptional Condensates”。
6.Cell:颠覆传统认知!细胞应激颗粒中的mRNA确实可以表达蛋白
doi:10.1016/j.cell.2020.11.010
就像人一样,细胞也会遭受应激。突然的氧气下降、过热或毒素都会引发一连串的分子变化,导致细胞停止生长,产生应激保护因子,并形成应激颗粒(stress granule)---蛋白和RNA分子挤在一起而形成的无膜细胞器。虽然应激颗粒的功能在很大程度上仍然是未知的,但人们认为它们只含有不被翻译成蛋白的RNA。如今,一项新的研究颠覆了这一长期以来的观点,表明应激颗粒内的信使RNA(mRNA)确实可以制造蛋白。相关研究结果于2020年12月11日在线发表在Cell期刊上,论文标题为“Single-Molecule Imaging Reveals Translation of mRNAs Localized to Stress Granules”。
为了弄清楚这些由应激引起的细胞器内的mRNA会发生什么,论文通讯作者Jeffrey Chao博士、论文第一作者博士后研究员Daniel Mateju及其同事们开始观察单个RNA分子与经历应激的活细胞内的应激颗粒之间的相互作用。为此,他们用荧光标签标记了应激颗粒和单个mRNA分子。多亏了一种名为SunTag的创新抗体标记工具,他们还可以在蛋白产生时以单分子的精度进行可视化观察。
利用这种方法,这些研究人员发现,即使mRNA被稳定地定位在应激颗粒内,它仍然可以被翻译成蛋白。虽然大多数mRNA的翻译在应激期间受到抑制,但是触发应激反应所必需的特定基因(如ATF4)在这些条件下会增加它们的翻译。通过使用ATF4-SunTag作为模型转录本,他们发现它在应激颗粒中的翻译并不是一个罕见的事件,而且完整的翻译周期(起始、延伸、终止)可以在应激颗粒中发生。此外,他们还发现有证据表明,在应激过程中翻译受到抑制的mRNA也可以在应激颗粒中进行翻译。
7.两篇Cell论文揭示强效人类中和抗体有望抵抗东部马脑炎病毒、亨德拉病毒和尼帕病毒攻击
doi:10.1016/j.cell.2020.11.011; doi:10.1016/j.cell.2020.11.023
虽然COVID-19抢占了头条新闻,但是科学家们在对抗其他危险病毒的斗争中正稳步取得进展。其中包括东部马脑炎病毒(Eastern Equine Encephalitis Virus, EEEV)、亨德拉病毒(Hendra virus, HeV)和尼帕病毒(Nipah virus, NiV)。东部马脑炎病毒是北美最具毒性的病毒之一。亨德拉病毒和尼帕病毒在东南亚地区流行。
与COVID-19一样,目前还没有办法阻断这些祸害。不过,在本周发表在Cell期刊上的两篇论文中,美国范德堡大学医学中心的James Crowe Jr.博士及其同事们在开发潜在地治疗和预防这些感染的人类单克隆抗体方面取得新进展。
在第一篇论文中,这些研究人员报告说,从自然遭受东部马脑炎病毒感染的幸存者中分离出的两种强效的中和抗体---EEEV-33(IgG)和EEEV-143(IgA)---保护小鼠免受这种病毒气溶胶的致命性攻击。相关研究结果于2020年12月9日在线发表在Cell期刊上,论文标题为“Human Antibodies Protect against Aerosolized Eastern Equine Encephalitis Virus Infection”。
在第二篇论文中,他们发现了首批天然存在的靶向亨德拉病毒受体结合蛋白的人类单克隆抗体。所有的这些抗体都能中和亨德拉病毒,其中的一些还能中和尼帕病毒,包括两种最为强效的交叉反应性中和抗体:HENV-26和HENV-32。相关研究结果发表在2020年12月10日的Cell期刊上,论文标题为“Potent Henipavirus Neutralization by Antibodies Recognizing Diverse Sites on Hendra and Nipah Virus Receptor Binding Protein”。
8.Cell论文解读!新发现颠覆对杀伤性T细胞的传统认知,有助开发出更好靶向实体瘤的CAR-T细胞
doi:10.1016/j.cell.2020.11.019
一类称为“杀伤性T细胞”的免疫细胞,也被称为细胞毒性或溶细胞性CD8 T细胞。在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院的研究人员发现杀伤性T细胞通常会留在血液中,不会进入器官和其他组织。相关研究结果于2020年12月10日在线发表在Cell期刊上,论文标题为“The Identity of Human Tissue-Emigrant CD8+ T Cells”。
这一发现可能有助于解决免疫学中的许多难题,包括具有医学意义的谜团,比如,为何最近开发的使用经过基因改造的杀伤性T细胞的癌症疗法不能很好地对抗实体瘤,以及为何被认为对杀伤性T细胞非常脆弱的艾滋病致病病毒HIV似乎能够通过躲在血液之外来无限期地逃避这些免疫细胞。
论文共同通讯作者、宾夕法尼亚大学佩雷尔曼医学院微生物学教授Michael Betts博士说,“这一发现告诉我们,杀伤性T细胞通常不会迁移出血液。如今我们知道了这一点,我们就可以开始设计更好的利用这些强大的细胞的治疗方案。”
9.重大进展!两篇Cell论文揭示冠状病毒和黄病毒增殖和传播所必需的宿主因子
doi:10.1016/j.cell.2020.12.005; doi:10.1016/j.cell.2020.12.006
在两项新的研究中,来自美国纽约大学和洛克菲勒大学等研究机构的研究人员发现SARS-CoV-2冠状病毒增殖和传播到其他细胞所必需的一种蛋白是未来疗法可能针对的一个潜在弱点。这种称为跨膜蛋白41 B(transmembrane protein 41 B, TMEM41B)的蛋白被认为在这种病毒在受感染细胞内复制和感染另一个细胞之前,帮助塑造保护病毒遗传物质的脂肪外膜。

这些作者发现TMEM41B对SARS-CoV-2的复制至关重要。在第一项研究中,通过开展一系列实验,他们将导致COVID-19疾病的SARS-CoV-2病毒在受感染细胞中的增殖与二十几种致命的黄病毒(包括黄热病病毒、西尼罗河病毒和寨卡病毒)中的相同过程进行了比较。相关研究结果于2020年12月8日在线发表在Cell期刊上,论文标题为“TMEM41B is a pan-flavivirus host factor”。
在第二项研究中,他们还将SARS-CoV-2在受感染细胞中的增殖方式与已知导致普通感冒的其他三种季节性冠状病毒(HCoV-OC43、HCoV-NL63和HCoV-229E)进行了比较。相关研究结果于2020年12月9日在线发表在Cell期刊上,论文标题为“Genome-scale identification of SARS-CoV-2 and pan-coronavirus host factor networks”。
10.重磅Cell论文详解!利用CRISPR-Cas13a和智能手机摄像头在30分钟内定量检测新冠病毒RNA
doi:10.1016/j.cell.2020.12.001
在一项新的研究中,这些研究人员概述了一种基于CRISPR的COVID-19测试技术,该技术使用智能手机摄像头,可在30分钟内提供准确结果。相关研究结果于2020年12月4日在线发表在Cell期刊上,论文标题为“Amplification-free detection of SARS-CoV-2 with CRISPR-Cas13a and mobile phone microscopy”。
在这种新的测试方法中,Cas13a蛋白与一种在切割时会产生荧光的报告分子结合在一起,然后与来自鼻腔拭子的患者样本混合。混合后的样本被放置在一种连接到智能手机的设备中。如果样本中含有SARS-CoV-2 RNA,Cas13就会被激活,并切割报告分子,导致荧光信号产生。然后,基本上变成了显微镜的智能手机摄像头可以检测到荧光,并报告测试的拭子呈病毒阳性。
论文共同通讯作者、格拉斯通病毒学研究所主任Melanie Ott博士说说,“这种测试方法的真正独特之处在于,它使用一步反应直接测试病毒RNA,而不是传统PCR测试中的两步过程。更简单的化学反应,配合智能手机摄像头,缩短了测试时间,不需要复杂的实验室设备。它还可以让这种测试方法产生定量测量结果,而不是简单的阳性或阴性结果。”
这些研究人员还表示,他们的测试方法可以适用于各种手机,从而使得它易于使用。Fletcher解释说,“我们选择使用手机作为我们检测设备的基础,这是因为它们具有直观的用户界面和高灵敏度的摄像头,让我们可以用来检测荧光。手机也是大规模生产的,而且成本效益高,这表明专门的实验室仪器并不是这种测试方法所必需的。”(生物谷 Bioon.com)
1.Cell论文解读!新方法首次详细揭示核孔复合物的组装过程
doi:10.1016/j.cell.2020.11.001
在一项新的研究中,来自瑞士苏黎世联邦理工学院和挪威卑尔根大学的研究人员开发出一种方法,使得他们能够首次详细研究大型蛋白复合物的组装过程。作为他们的案例研究,他们选择了最大的细胞复合物之一:酵母细胞中的核孔复合物。相关研究结果近期发表在Cell期刊上,论文标题为“Maturation Kinetics of a Multiprotein Complex Revealed by Metabolic Labeling”。论文通讯作者为苏黎世联邦理工学院的Karsten Weis和Evgeny Onischenko。

图片来自Cell, 2020, doi:10.1016/j.cell.2020.11.001。
这些研究人员将他们的新方法称为KARMA(kinetic analysis of incorporation rates in macromolecular assemblies, 高分子组装中掺入速率的动力学分析),该方法是基于研究代谢过程的方法构建出来的。研究代谢的科学家们长期以来一直在他们的研究工作中使用放射性碳,例如,标记葡萄糖分子,然后细胞吸收并代谢放射性碳。这种放射性标记使得人们能够追踪葡萄糖分子或其代谢物出现的位置和时间点。
2.Cell论文详解!挑战常规!染色质既不是固体也不是液体,而是更像一种凝胶
doi:10.1016/j.cell.2020.11.027
基因组生物学中一个自DNA发现以来一直困扰着科学家们的基本问题:在我们的细胞核内, DNA和蛋白的复杂包裹物(即染色质)是固体还是液体?在一项新的研究中,来自加拿大阿尔伯塔大学和美国科罗拉多州立大学的研究人员找到了这个问题的答案。他们发现染色质既不是固体也不是液体,而是更像一种凝胶。相关研究结果近期发表在Cell期刊上,论文标题为“Condensed Chromatin Behaves like a Solid on the Mesoscale In Vitro and in Living Cells”。论文通讯作者为阿尔伯塔大学肿瘤学系教授Michael Hendzel和科罗拉多州立大学的Jeffrey Hansen。
Hendzel说,以前,生物化学等领域是在染色质和细胞核的其他组分以液体状态运行的假设下进行的。这种对染色质物理特性的新理解挑战了这种观点法,并可能导致对基因组如何编码和解码的更准确理解。
3.Cell:淋巴结受一种独特的具有免疫调节潜能的感觉神经元支配
doi:10.1016/j.cell.2020.11.028
长期以来,神经系统和免疫系统一直被认为是身体中的独立实体,但是一项新的研究发现了这两者之间的直接细胞相互作用。来自哈佛医学院、布罗德研究所和拉根研究所的研究人员发现,痛觉神经元围绕在小鼠淋巴结周围,可以调节这些淋巴结的活动,而淋巴结是免疫系统的关键部分。相关研究结果近期发表在Cell期刊上,论文标题为“Lymph nodes are innervated by a unique population of sensory neurons with immunomodulatory potential”。
这项新研究揭示了介导神经系统和免疫系统之间交谈的细胞。它还为更多关于神经系统如何调节免疫反应的研究铺平了道路。
4.Cell重磅解读!肥胖损伤免疫细胞功能并加速肿瘤生长的分子机制!
doi:10.1016/j.cell.2020.11.009
肥胖与十几种不同类型的癌症风险增加有关,同时也与患者的预后和生存率下降直接相关。多年来,科学家们已经识别出驱动肿瘤生长的肥胖相关的过程,比如代谢改变和慢性炎症等,但他们并未详细阐明肥胖和癌症之间的具体相互作用。近日,一项刊登在国际杂志Cell上题为“Obesity Shapes Metabolism in the Tumor Microenvironment to Suppress Anti-Tumor Immunity”的研究报告中,来自哈佛医学院等机构的科学家们通过研究揭开了这一谜题,研究者发现,肥胖会促进癌细胞在争夺能量的战斗中战胜杀死肿瘤的免疫细胞。
研究者表示,高脂肪饮食会降低肿瘤中的CD8+ T细胞的数量和抗肿瘤活性,之所以出现这种情况,是因为癌细胞为了应对脂肪供应的增加而重编程自身的代谢,从而更好地吞噬富含能量的脂肪分子,并剥夺了T细胞的燃料,并能加速肿瘤的生长。研究者Marcia Haigis说道,将相同的肿瘤放在肥胖和非肥胖的环境中,就能够揭示癌细胞会应对高脂肪饮食而对其细胞代谢重新布线;相关研究结果表明,在某种环境中可能有效的疗法或许在另一种环境中不那么有效,鉴于目前肥胖在人群中的流行,或许就需要科学家们进一步研究理解了。阻断脂肪相关的代谢重编程或能明显减少高脂肪饮食的小鼠机体的肿瘤体积,由于CD8+ T细胞是免疫疗法激活宿主机体免疫系统抵御癌症的主要武器,本文研究中,研究人员提出了改进此类疗法的新型策略。癌症免疫疗法能给癌症患者的生活产生巨大影响,但并非每名患者都能获益。如今研究人员知道随着肥胖改变,T细胞和肿瘤细胞之间存在着新陈代谢的拉锯战, 本文研究或许就提供了探索这种相互作用的路线图,这或能帮助我们开始以新的方式思考癌症免疫疗法和联合疗法的作用机制。
5.Cell论文详解!我的命运我主宰,而细胞中的RNA分子也是如此
doi:10.1016/j.cell.2020.11.030
科学家们对转录是如何开始的有了很好的了解:称为RNA聚合酶的蛋白被招募到DNA分子的特定区域,并开始沿DNA链移动,边走边合成mRNA分子。但是,这个过程的一部分还不太清楚:细胞如何知道何时停止转录?

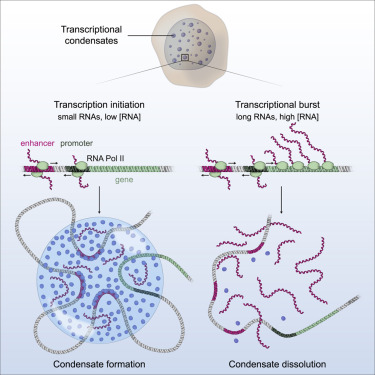
图片来自Cell, 2020, doi:10.1016/j.cell.2020.11.030。
如今,在一项新的研究中,美国怀特海德生物医学研究所成员、麻省理工学院生物学教授Richard Young及其团队和麻省理工学院化学工程教授Arup K. Chakraborty及其团队发现RNA分子通过反馈回路调节它们自身的形成。RNA分子太少,细胞就会启动转录以产生更多的RNA分子。然后,在某个阈值,过多的RNA分子会导致转录停止。相关研究结果于2020年12月16日在线发表在Cell期刊上,论文标题为“RNA-Mediated Feedback Control of Transcriptional Condensates”。
6.Cell:颠覆传统认知!细胞应激颗粒中的mRNA确实可以表达蛋白
doi:10.1016/j.cell.2020.11.010
就像人一样,细胞也会遭受应激。突然的氧气下降、过热或毒素都会引发一连串的分子变化,导致细胞停止生长,产生应激保护因子,并形成应激颗粒(stress granule)---蛋白和RNA分子挤在一起而形成的无膜细胞器。虽然应激颗粒的功能在很大程度上仍然是未知的,但人们认为它们只含有不被翻译成蛋白的RNA。如今,一项新的研究颠覆了这一长期以来的观点,表明应激颗粒内的信使RNA(mRNA)确实可以制造蛋白。相关研究结果于2020年12月11日在线发表在Cell期刊上,论文标题为“Single-Molecule Imaging Reveals Translation of mRNAs Localized to Stress Granules”。
为了弄清楚这些由应激引起的细胞器内的mRNA会发生什么,论文通讯作者Jeffrey Chao博士、论文第一作者博士后研究员Daniel Mateju及其同事们开始观察单个RNA分子与经历应激的活细胞内的应激颗粒之间的相互作用。为此,他们用荧光标签标记了应激颗粒和单个mRNA分子。多亏了一种名为SunTag的创新抗体标记工具,他们还可以在蛋白产生时以单分子的精度进行可视化观察。
利用这种方法,这些研究人员发现,即使mRNA被稳定地定位在应激颗粒内,它仍然可以被翻译成蛋白。虽然大多数mRNA的翻译在应激期间受到抑制,但是触发应激反应所必需的特定基因(如ATF4)在这些条件下会增加它们的翻译。通过使用ATF4-SunTag作为模型转录本,他们发现它在应激颗粒中的翻译并不是一个罕见的事件,而且完整的翻译周期(起始、延伸、终止)可以在应激颗粒中发生。此外,他们还发现有证据表明,在应激过程中翻译受到抑制的mRNA也可以在应激颗粒中进行翻译。
7.两篇Cell论文揭示强效人类中和抗体有望抵抗东部马脑炎病毒、亨德拉病毒和尼帕病毒攻击
doi:10.1016/j.cell.2020.11.011; doi:10.1016/j.cell.2020.11.023
虽然COVID-19抢占了头条新闻,但是科学家们在对抗其他危险病毒的斗争中正稳步取得进展。其中包括东部马脑炎病毒(Eastern Equine Encephalitis Virus, EEEV)、亨德拉病毒(Hendra virus, HeV)和尼帕病毒(Nipah virus, NiV)。东部马脑炎病毒是北美最具毒性的病毒之一。亨德拉病毒和尼帕病毒在东南亚地区流行。
与COVID-19一样,目前还没有办法阻断这些祸害。不过,在本周发表在Cell期刊上的两篇论文中,美国范德堡大学医学中心的James Crowe Jr.博士及其同事们在开发潜在地治疗和预防这些感染的人类单克隆抗体方面取得新进展。
在第一篇论文中,这些研究人员报告说,从自然遭受东部马脑炎病毒感染的幸存者中分离出的两种强效的中和抗体---EEEV-33(IgG)和EEEV-143(IgA)---保护小鼠免受这种病毒气溶胶的致命性攻击。相关研究结果于2020年12月9日在线发表在Cell期刊上,论文标题为“Human Antibodies Protect against Aerosolized Eastern Equine Encephalitis Virus Infection”。
在第二篇论文中,他们发现了首批天然存在的靶向亨德拉病毒受体结合蛋白的人类单克隆抗体。所有的这些抗体都能中和亨德拉病毒,其中的一些还能中和尼帕病毒,包括两种最为强效的交叉反应性中和抗体:HENV-26和HENV-32。相关研究结果发表在2020年12月10日的Cell期刊上,论文标题为“Potent Henipavirus Neutralization by Antibodies Recognizing Diverse Sites on Hendra and Nipah Virus Receptor Binding Protein”。
8.Cell论文解读!新发现颠覆对杀伤性T细胞的传统认知,有助开发出更好靶向实体瘤的CAR-T细胞
doi:10.1016/j.cell.2020.11.019
一类称为“杀伤性T细胞”的免疫细胞,也被称为细胞毒性或溶细胞性CD8 T细胞。在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院的研究人员发现杀伤性T细胞通常会留在血液中,不会进入器官和其他组织。相关研究结果于2020年12月10日在线发表在Cell期刊上,论文标题为“The Identity of Human Tissue-Emigrant CD8+ T Cells”。
这一发现可能有助于解决免疫学中的许多难题,包括具有医学意义的谜团,比如,为何最近开发的使用经过基因改造的杀伤性T细胞的癌症疗法不能很好地对抗实体瘤,以及为何被认为对杀伤性T细胞非常脆弱的艾滋病致病病毒HIV似乎能够通过躲在血液之外来无限期地逃避这些免疫细胞。
论文共同通讯作者、宾夕法尼亚大学佩雷尔曼医学院微生物学教授Michael Betts博士说,“这一发现告诉我们,杀伤性T细胞通常不会迁移出血液。如今我们知道了这一点,我们就可以开始设计更好的利用这些强大的细胞的治疗方案。”
9.重大进展!两篇Cell论文揭示冠状病毒和黄病毒增殖和传播所必需的宿主因子
doi:10.1016/j.cell.2020.12.005; doi:10.1016/j.cell.2020.12.006
在两项新的研究中,来自美国纽约大学和洛克菲勒大学等研究机构的研究人员发现SARS-CoV-2冠状病毒增殖和传播到其他细胞所必需的一种蛋白是未来疗法可能针对的一个潜在弱点。这种称为跨膜蛋白41 B(transmembrane protein 41 B, TMEM41B)的蛋白被认为在这种病毒在受感染细胞内复制和感染另一个细胞之前,帮助塑造保护病毒遗传物质的脂肪外膜。

图片来自Cell, 2020, doi:10.1016/j.cell.2020.12.006。
这些作者发现TMEM41B对SARS-CoV-2的复制至关重要。在第一项研究中,通过开展一系列实验,他们将导致COVID-19疾病的SARS-CoV-2病毒在受感染细胞中的增殖与二十几种致命的黄病毒(包括黄热病病毒、西尼罗河病毒和寨卡病毒)中的相同过程进行了比较。相关研究结果于2020年12月8日在线发表在Cell期刊上,论文标题为“TMEM41B is a pan-flavivirus host factor”。
在第二项研究中,他们还将SARS-CoV-2在受感染细胞中的增殖方式与已知导致普通感冒的其他三种季节性冠状病毒(HCoV-OC43、HCoV-NL63和HCoV-229E)进行了比较。相关研究结果于2020年12月9日在线发表在Cell期刊上,论文标题为“Genome-scale identification of SARS-CoV-2 and pan-coronavirus host factor networks”。
10.重磅Cell论文详解!利用CRISPR-Cas13a和智能手机摄像头在30分钟内定量检测新冠病毒RNA
doi:10.1016/j.cell.2020.12.001
在一项新的研究中,这些研究人员概述了一种基于CRISPR的COVID-19测试技术,该技术使用智能手机摄像头,可在30分钟内提供准确结果。相关研究结果于2020年12月4日在线发表在Cell期刊上,论文标题为“Amplification-free detection of SARS-CoV-2 with CRISPR-Cas13a and mobile phone microscopy”。
在这种新的测试方法中,Cas13a蛋白与一种在切割时会产生荧光的报告分子结合在一起,然后与来自鼻腔拭子的患者样本混合。混合后的样本被放置在一种连接到智能手机的设备中。如果样本中含有SARS-CoV-2 RNA,Cas13就会被激活,并切割报告分子,导致荧光信号产生。然后,基本上变成了显微镜的智能手机摄像头可以检测到荧光,并报告测试的拭子呈病毒阳性。
论文共同通讯作者、格拉斯通病毒学研究所主任Melanie Ott博士说说,“这种测试方法的真正独特之处在于,它使用一步反应直接测试病毒RNA,而不是传统PCR测试中的两步过程。更简单的化学反应,配合智能手机摄像头,缩短了测试时间,不需要复杂的实验室设备。它还可以让这种测试方法产生定量测量结果,而不是简单的阳性或阴性结果。”
这些研究人员还表示,他们的测试方法可以适用于各种手机,从而使得它易于使用。Fletcher解释说,“我们选择使用手机作为我们检测设备的基础,这是因为它们具有直观的用户界面和高灵敏度的摄像头,让我们可以用来检测荧光。手机也是大规模生产的,而且成本效益高,这表明专门的实验室仪器并不是这种测试方法所必需的。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


