多篇文章聚焦科学家们近年来在星形胶质细胞研究上的新进展!
来源:本站原创 2020-09-30 23:47
本文中,小编盘点了多篇文章,共同聚焦科学家们近年来在星形胶质细胞研究上取得的新进展,分享给大家!图片来源:Lucas Cheadle【1】Science子刊:揭示饮酒会导致小胶质细胞吞噬和修剪突触,引发焦虑doi:10.1126/scisignal.aba5754在一项新的研究中,来自葡萄牙波尔图大学的研究人员发现在雄性小鼠中,连续10天饮酒达到暴饮水平(对
本文中,小编盘点了多篇文章,共同聚焦科学家们近年来在星形胶质细胞研究上取得的新进展,分享给大家!
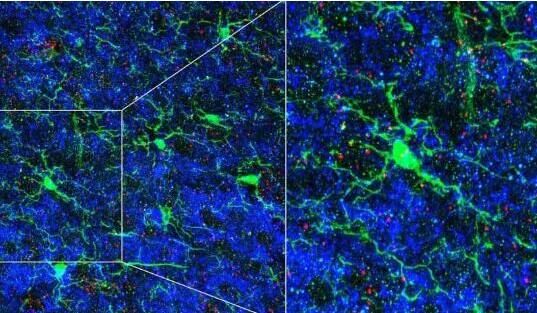
图片来源:Lucas Cheadle
【1】Science子刊:揭示饮酒会导致小胶质细胞吞噬和修剪突触,引发焦虑
doi:10.1126/scisignal.aba5754
在一项新的研究中,来自葡萄牙波尔图大学的研究人员发现在雄性小鼠中,连续10天饮酒达到暴饮水平(对人类而言,平均一个人每天大约喝五次酒)可增强前额叶皮层小胶质细胞中的Src-TNF信号转导,从而增强它们的吞噬能力并导致异常的突触修剪,最终导致突触损失和焦虑样行为。总体而言,这些结果表明小胶质细胞的异常突触修剪可能在酒精滥用引起的突触传递缺陷中起重要作用。相关研究结果发表在Science Signaling期刊上。
神经炎症被认为是酒精引起的大脑损伤的一个主要因素。之前的多项研究(包括5周大的雌性小鼠饮酒持续20周,乙醇浓度大约为140 mg/dl;给6至8周大的雌性小鼠喂食乙醇浓度大约为215 mg/dl的液体饮食,持续5周)已表明,重度饮酒会触发促炎性细胞因子表达特征,并伴有神经胶质增生。然而,尽管暴饮水平的重复性饮酒诱导了神经免疫激活和兴奋性突触丧失,但是在这项新的研究中,这些作者发现在雄性小鼠模型中,这未产生经典的促炎性细胞因子表达特征。相反,他们的数据更符合之前的多项转录组学研究,尤其是一项RNA测序研究:来自小鼠前额叶皮层的小胶质细胞长期暴露于酒精(使用隔日两瓶的选择模式)不会诱发典型的促炎性细胞因子表达特征。同样,在这些作者开发的乙醇暴露模型中,TLR4的转录表达明显下降,这与之前的一项表明体外培养的人外周血单核细胞急性暴露于酒精可抑制TLR4信号转导的研究更为一致。因此,乙醇暴露的剂量和持续时间似乎会不同地影响神经免疫激活和小胶质细胞促炎信号转导。
【2】Neuron:揭秘小胶质细胞在大脑中塑造神经回路的分子机制
doi:10.1016/j.neuron.2020.08.002
日前,一篇发表在国际杂志Neuron上的研究报告中,来自冷泉港实验室等机构的科学家们通过研究表示,免疫细胞在微调大脑神经回路方面或许扮演着意想不到的角色,称之为小胶质细胞的免疫细胞不仅能够保护大脑免于感染和炎症,而且还能帮助塑造发育中的大脑回路,本文研究结果表明,小胶质细胞还能指导神经元对感觉线索产生反应从而修饰自身的连接性。
这项研究中,研究人员深入揭示了生物学和外部世界之间的关联,研究者Lucas Cheadle表示,我们非常感兴趣研究神经回路是如何对感官体验做出反应的;在很大程度上,大脑的总体结构和连接时在出生时就已经完成的,但其确实需要来自环境的强有力的反馈才能够促进大脑成熟,当动物与周围环境相互作用时,一些神经元的连接就会被消除,而另一些连接则会被加强,而对于人类而言,这一过程可能会持续到出生后十年时间。
【3】Cell:小胶质细胞通过吞噬胞外基质为新的突触形成让出空间
doi:10.1016/j.cell.2020.05.050
为了制造新的记忆,我们的脑细胞首先必须找到彼此。从神经元长长的有分支的触角末端伸出的小突起将这些神经元连接在一起,这样它们就可以交谈。这些细胞聊天的端口被称为突触,在整个大脑中发现了数万亿个突触,这让我们能够呈现新的知识。但是,科学家们仍在了解这些连接如何对新的经历和信息作出反应。如今,在一项新的研究中,来自美国加州大学旧金山分校的研究人员令人吃惊地发现了一种大脑免疫细胞帮助解决问题的新方法。相关研究结果发表在Cell期刊上。
【4】Science:浙大科学家揭示小胶质细胞在记忆调节中起着关键作用
doi:10.1126/science.aaz2288
小胶质细胞是大脑中的常驻免疫细胞,它们是第一反应者,总是在寻找发生差错的地方。它们大约占我们脑细胞的10%。在过去,它们被认为是大脑中的被动旁观者,仅在受伤或感染时,它们才起作用。这些细胞最早是由德国医生Rudolf Virchow于1856年观察到的,后来被称为小胶质细胞,意为“小胶水”。如今,在一项新的以小鼠为实验对象的研究中,来自中国浙江大学医学院的研究人员发现小胶质细胞实际上可能是记忆保持的关键因素。如果在人类中发现同样的效果,那么这可能导致人们开发出更好地治疗健忘症、阿尔茨海默病和其他影响记忆力的疾病的方法。相关研究结果发表在Science期刊上。
小胶质细胞有很多功能。当存在损伤或感染时,它们在抑制大脑反应方面起着积极的作用。但是科学家们越来越意识到小胶质细胞有很多功能。我们的大脑混杂着死亡的细胞和堆积的化学物,它们都需要清除。小胶质细胞的任务是保持我们大脑的清洁和健康。科学家们最近还发现,小胶质细胞参与维持神经细胞之间的连接(称为突触)。这些突触是至关重要的通讯枢纽,以便让脑细胞相互交谈并传输脑信号。特别地,在大脑发育过程中,小胶质细胞会主动清除或“修剪”突触,这有助于塑造让大脑有效工作的回路。
【5】Science子刊:阻断星形胶质细胞中的TGF-β受体有望治疗阿尔茨海默病和癫痫
doi:10.1126/scitranslmed.aaw8283 doi:10.1126/scitranslmed.aaw8954
抑制大脑炎症的药物可能能够减缓甚至逆转随着年龄增长而引起的认知能力下降。在第一项新的研究中,美国加州大学伯克利分校整合生物学教授Daniela Kaufer博士和以色列班古里昂大学的Alon Friedman博士及其同事们报道给予一种这样的药物的老年小鼠出现大脑炎症的迹象更少,并且能够更好地学习新的任务,几乎与年龄只有它们一半的小鼠一样熟练。相关研究结果近期发表在Science Translational Medicine期刊上。
研究者表示,我们倾向于用看待神经退化的方式来看待年老的大脑:衰老涉及功能丧失和细胞死亡。但是我们的新数据从一种不同的角度说明年老大脑为何运作不佳:这正是因为这种炎症负荷(inflammatory load)的‘迷雾(fog)’。但是,当移除这种炎症迷雾(inflammatory fog)时,年老的大脑在几天之内就像年轻的大脑一样。就大脑存在的可塑性而言,这是一个非常非常乐观的发现。我们可以逆转大脑衰老。

图片来源:Gong Chen Lab, Penn State
【6】Stem Cell Rep:新型药物混合制剂有望将星形细胞转化为神经元 治疗多种神经变性疾病
doi:10.1016/j.stemcr.2019.01.003
近日,一项刊登在国际杂志Stem Cell Reports上的研究报告中,来自宾夕法尼亚州立大学的科学家们通过研究开发了一种简单的药物混合制剂,其或能将受损神经元附近的细胞转化成为功能性的新型神经元,从而用来治疗中风、阿尔兹海默病和大脑损伤等疾病;研究者表示,一组由四种(甚至三种)分子组成的混合制剂就能将胶质细胞转化为新的神经元细胞。
研究者Gong Chen教授说道,大脑修复的最大问题就是在患者大脑损伤后神经元细胞无法再生,因为神经元细胞不能分裂;相比较而言,聚集在损伤大脑组织附近的胶质细胞则能在大脑损伤后增殖,研究者认为,将这些胶质细胞转化称为新的神经元或许是恢复缺失神经元功能的最佳手段。
【7】Nat Neurosci:科学家成功在小鼠大脑中研究人类小胶质细胞的功能 有望开发阿尔兹海默病新型疗法
doi:10.1038/s41593-019-0525-x
一直以来,人类大脑都是一个非常复杂的研究对象,大脑扫描的分辨率和其所能提供的信息也非常有限,而且研究者也无法利用体外方法来完全复制脑细胞中重要的微环境;近日,一项刊登在国际杂志Nature Neuroscience上的研究报告中,来自Flanders生物技术研究所的科学家们通过研究开发了一种新方法,其开创了将人类大脑小胶质细胞移植到小鼠大脑中的先河。
小胶质细胞是一种主要复杂大脑功能维持的脑细胞,其在阿尔兹海默病的发病过程中扮演着非常重要的角色,但目前研究人员很难对小胶质细胞进行研究;在培养皿中培养小胶质细胞往往会忽略维持细胞功能所需要的复杂环境,而诸如小鼠等模式动物大脑中的小胶质细胞也与人类大脑的小胶质细胞不同。
doi:10.1016/j.cell.2019.04.001
近日,一项刊登在国际杂志Cell上的研究报道了脑细胞收集过度活跃神经元分泌的受损脂质,然后将这些有毒分子回收利用的现象,它是保护神经元免受过度活动的破坏的机制。当神经元快速而激烈地活动时,细胞中的脂质分子会受到损害并且会变得有毒。虽然大多数细胞将多余的脂肪酸隔离开来或将它们运送到自身的线粒体中以防止积聚,但神经元似乎并不依赖这一机制。
研究小组发现,刺激培养皿中的小鼠神经元会导致脂肪酸积聚,最终导致脂质颗粒释放。然后,附近的星形胶质细胞吞噬了颗粒,增强了参与能量产生和解毒的基因的活性。研究者表示,星形胶质细胞将神经元的分泌的脂质转运到自己的线粒体中,将废物转化为能量。小鼠模型显示出类似的现象:在模仿中风的大脑损伤后,神经元增加了参与将脂肪酸运输出细胞的蛋白质的产生,以及星形胶质细胞中的脂肪酸含量也明显上升。
【9】Science:揭示大脑星形胶质细胞在控制昼夜节律中的新作用
doi:10.1126/science.aat4104
在一项新的研究中,来自英国剑桥大学医学研究委员会分子生物学实验室的研究人员发现星形胶质细胞,即包围并支持大脑神经元的“看护”细胞,在昼夜节律(即身体24小时的生物钟)中起着比之前理解的更重要的作用。星形胶质细胞之前被认为仅是支持调节昼夜节律的神经元,但是这项新的研究指出它们实际上能够引导这种体内生物钟的节奏,并且首次证实它们能够控制哺乳动物日常行为的模式。相关研究结果发表在Science期刊上。
当昼夜节律被打乱时,这可能导致时差反应和睡眠障碍,而且还可能导致从精神疾病到痴呆症、糖尿病和癌症的一系列疾病。这项新研究的发现可能为开发新的治疗方法铺平道路。昼夜节律因其在维持人体健康方面的作用而广为人所知,而且虽然已发现身体中的许多不同类型的细胞都有自己的内部时钟,但是这些时钟的定时主要由视交叉上核(suprachiasmatic nucleus, SCN)控制。视交叉上核是下丘脑中的一个小的大脑区域,作为负责调节日常行为的主时钟。
【10】Cell Stem Cell:科学家阐明大脑中神经前体细胞分化为神经胶质细胞的分子机制
doi:10.1016/j.stem.2018.09.008
在大脑中,两种类型的细胞常常会保持活跃状态,即神经细胞和胶质细胞,长期以来科学家们认为胶质细胞是一种支持性的细胞,但如今越来越多的研究发现这种细胞在大脑神经元细胞之间的交流沟通上扮演着非常重要的积极性角色,此外,胶质细胞还参与到了神经变性疾病的发生过程中。近日,一项刊登在国际杂志Cell Stem Cell上的研究报告中,来自德国美茵茨大学医学中心的科学家们通过研究得出了重要发现,这些发现或能帮助研究人员阐明在神经变性疾病发生过程中胶质细胞所发生的变化;文章中,研究人员揭示了神经胶质细胞如何从大脑中的神经前体细胞(neural precursor cells)发育而来,研究者表示,涉及三个阶段及三种转录因子的分化过程在组织细胞核中基因的胶质特异性转录过程中扮演着重要角色。
胶质细胞通常被分为三种基本的类型:星形胶质细胞(astrocytes)、少突胶质细胞(oligodendrocytes)和小胶质细胞(microglia),前两种细胞就是所谓的大胶质细胞;星形胶质细胞是最常见的细胞类型,其在胶质细胞中占到了80%的比例,其是通过放射状胶质细胞或神经前体细胞衍生而来;这项研究中,研究人员应用RNA测序技术对在某一个特定时间点(涉及上述三个过程的分化过程)进行转录的细胞中所有的基因进行分析,在第一阶段,星形胶质前体细胞形成后,会通过细胞分裂进行增殖;在第二阶段,这些星形胶质前体细胞就会发育称为年轻未成熟的星形胶质细胞,但其便不再分裂了,而第三阶段则能促进星形胶质细胞完全成熟并转化为功能性的细胞。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


