2020年液体活检研究进展及其展望
来源:本站原创 2020-12-31 06:34
2020年12月31日讯/生物谷BIOON/---液体活检即肿瘤无创诊断技术,它的出现标志着人类在攻克肿瘤的道路上又前进了一大步。2015年液体活检技术被MIT科技综述杂志(MIT Technology Review)评为年度十大突破技术之一。2017年6月,世界经济论坛与《科学美国人》杂志的专家委员会联合选出了2017年度全球十大新兴技术榜单,其中肿瘤的无
2020年12月31日讯/生物谷BIOON/---液体活检即肿瘤无创诊断技术,它的出现标志着人类在攻克肿瘤的道路上又前进了一大步。2015年液体活检技术被MIT科技综述杂志(MIT Technology Review)评为年度十大突破技术之一。
2017年6月,世界经济论坛与《科学美国人》杂志的专家委员会联合选出了2017年度全球十大新兴技术榜单,其中肿瘤的无创诊断技术成功入选并荣膺榜首。肿瘤无创诊断技术即液体活检(liquid biopsies)的出现,标志着人类在攻克肿瘤的道路上又前进了一大步。与传统的组织活检相比,液体活检具备实时动态检测、克服肿瘤异质性、提供全面检测信息等独特优势。
目前,在临床研究中,液体活检技术主要包括游离循环肿瘤细胞(CTC)检测、循环肿瘤DNA(ctDNA)检测、外泌体及循环RNA(Circulating RNA)检测等。癌症的发生与发展的过程中会释放一系列癌症组分到血液当中。液体活检就是通过分析血液中这些癌症组分,来实现癌症的早期筛查、分子分型、预后、用药指导以及复发监测等临床应用。针对2020年外泌体取得的进展,进行一番梳理,以飨读者。
1.Cell:液体样品检测可用于癌症的诊断
doi:10.1016/j.cell.2020.07.009
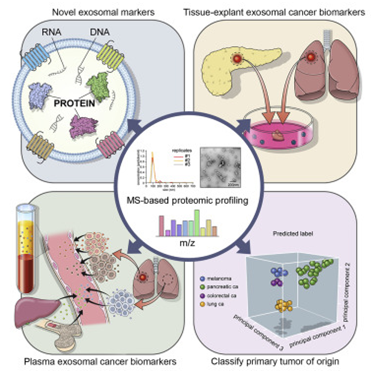
2020年8月,Ayuko Hoshino等人报道,肿瘤释放的细胞外囊泡和颗粒(extracellular vesicle and particle, EVP)可用于在早期阶段检测多种不同类型的癌症。他们使用了来自包括乳腺癌、结肠癌和肺癌在内的18种不同癌症的样本。通过使用计算生物学方法将特定的EVP蛋白特征与某些类型的癌症相匹配,他们发现计算机可以从样本中识别出不同类型的癌症,其灵敏度为95%,特异性为90%。
2.NEJM:NEJM揭示特泊替尼治疗METex14跳跃突变的非小细胞肺癌显示持久的反应
doi:10.1056/NEJMoa2004407
2020年9月,Paul K. Paik等人在一项开放标签的2期临床试验(称为VISION)中发现MET外显子14 (METex14)跳跃突变的晚期非小细胞肺癌(NSCLC)患者对特泊替尼(tepotinib)治疗的客观响应率达到46.5%。
VISION临床试验还表明液体活检是检测突变的可靠方法,可用于可以确定患者对这种药物的反应。51例患者可获得基线和治疗时相匹配的液体活检样本。通过下一代测序,他们发现这些患者中有34人出现分子反应,表现为这种跳跃突变的消失或者大幅减少,射线成像证实68%的患者出现分子反应。
3.Science:血液测试有助于在症状出现之前发现癌症
doi:10.1126/science.abb9601
2020年4月,Anne Marie Lennon等人在数千名没有癌症病史或症状的人中,首次发现血液测试有助于检测多种癌症。这种血液测试仍然是实验性的。即便是它的支持者也说,它还需要改进,而且这些研究结果并不理想。然而,它们显示了在常规护理中使用这些基于基因的测试(称为液体活检)可能会带来哪些好处和不足---在这种情形下,使用PET扫描来确认或排除可疑的肿瘤。但是这种测试方法漏掉的癌症病例比发现的要多得多,而且还发出了一些错误的警报,从而导致不必要的后续程序。它仅在65至75岁的女性中进行研究,还需要在男性、其他年龄段和更加多样化的人群中进行研究。
4.Nature:科学家成功利用机器学习技术对肺癌患者进行早期诊断
doi:10.1038/s41586-020-2140-0
2020年3月,Jacob J. Chabon等人研究利用机器学习系统检测人类患者机体中的早期肺癌,并测试它寻找血液样本中的循环肿瘤DNA(ctDNA)的能力。他们训练机器学习模型,使其能够识别出与非小细胞肺癌相关的数据参数,一旦该机器模型进行了训练,其就能对既定患者的肺癌风险进行有效评估。在测试过程中,这种机器学习系统发现了63%的1期肺癌患者,虽然并不如CT扫描结果好,但其却能足以对高危肺癌患者进行早期筛查。
5.滴血验癌或成真!Science子刊报道个性化血液测试准确检测血液中的肿瘤DNA
doi:10.1126/scitranslmed.aaz8084
2020年6月,Jonathan Wan等人将循环的肿瘤DNA与肿瘤基因组图谱进行比较后,开发出一种计算方法,可以根据患者的肿瘤突变情况来查看血液中的许多DNA片段。通过这种个性化的测序方法,可以从血液中的一百万个DNA片段中检测出一个或几个带有突变的DNA片段。与以前的方法相比,这种方法的灵敏度提高了大约10倍。结合他们最近展示的从干血点中提取DNA序列的方法,他们认为从针扎血液样本中检测血液中的癌症水平是可能的。这在将来甚至可以在家里进行,并且可以在两次就诊之间更频繁地监测病人的病情。它还可以帮助远离癌症专科中心的人扩大癌症诊断的渠道。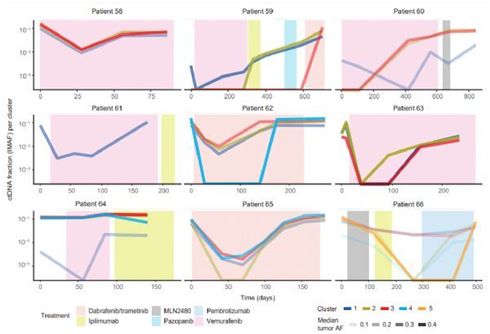
6.Science子刊:新型芯片实验室血液测试有望更早地发现癌症
doi:10.1126/scitranslmed.aaz2878
2020年6月,Peng Zhang等人开发出一种通用的高分辨率胶体喷墨打印方法,从而允许稳健地和可扩展地制造三维纳米图案聚二甲基硅氧烷/玻璃微流体芯片,用于分析血浆中的细胞外囊泡。对临床血浆标本的分析表明,这种微流体芯片平台可以用于癌症检测,包括在一个训练队列(n = 30,96.7%准确率)和一个独立的验证队列(n = 70,92.9%准确率)中,对年龄匹配的对照组和原位导管癌、浸润性导管癌或局部转移性乳腺癌患者的准确分类。通过临床验证,这种技术可以提供一种有用的液体活检工具,以改善癌症诊断和实时监测患者的肿瘤演变,从而为个性化治疗提供信息。
7.Nat Med:重大突破!生物标志物检测准确检测早期肾癌!
doi:10.1038/s41591-020-0933-1
2020年6月,Pier Vitale Nuzzo等人报道一种新的液体活检方法可以高精度地检测出肾癌,包括通常可以治愈但很难早期检测到的小的、局部的肾脏肿瘤。这种称为cfMeDIP-seq(cell-free methylated DNA immunoprecipitation and high-throughput sequencing, 无细胞甲基化DNA免疫沉淀和高通量测序)的方法并不寻找肿瘤脱落DNA的突变,而是检测找肿瘤脱落DNA上存在的异常甲基化。当在血液中利用这种方法区分肾癌患者和无肾癌患者时,它的准确率接近100%。这种方法在检测尿液样本时精确度较低,但是他们相信,性能可以提高。如果该方法在更大规模的试验中得到验证并广泛应用于临床,尿样的侵入性甚至会比抽血更小。
8.Nature子刊深度解读!基于ctDNA的液体活检技术在癌症诊断中的应用进展!
doi:10.1038/s43018-020-0043-5
2020年3月,David W. Cescon等人深入分析了循环肿瘤DNA和肿瘤液体活检的研究进展;如今利用分析循环肿瘤DNA(ctDNA)来检测及监测癌症的技术越来越成熟,而且越来越多的研究证据揭示了该技术在诊断测试中的能力,ctDNA液体活检在实体瘤和恶性血液癌症中的诊断、特性分析及管理中的全部潜力将通过评估临床实用性的介入性临床试验来揭示。
他们从以下几方面进行了阐述,1)转移性实体瘤中的ctDNA;2)免疫疗法反应的基因组关联性;3)从临床试验到临床应用;4)ctDNA的动态变化和疗法反应;5)获得性耐药性的识别和特性分析;6)癌前诊断和筛查;7)引入基于ctDNA的癌症筛查;8)基于ctDNA的临床试验设计等。此外,他们讨论了ctDNA液体活检在癌症检测中的应用以及未来临床应用的前景。
9.Science子刊:预测肺癌是否恶化的新型生物标志物
doi:10.1126/sciadv.aaz6162
2020年3月,Yang Liu等人评估了非小细胞肺癌(NSCLC)脱落的细胞外囊泡所携带的蛋白,以确定哪些蛋白可以作为转移性NSCLC细胞的标志物。他们发现了一种在转移性而非非转移性NSCLC细胞分泌的细胞外囊泡中高表达的蛋白:四次跨膜蛋白8(tetraspanin-8, Tspan8)。这种蛋白可以用作生物标志物,以开发出一种快速,微创的试验,以尽早发现可治愈的癌症。
10.Nat Commun:新型表观基因组平台或有望实现对早期胰腺癌的准确诊断
doi:10.1038/s41467-020-18965-w
2020年10月,Gulfem D. Guler等人纳入了307名40岁及以上的患者(64人患有胰腺导管腺癌,243人未患癌症)进行研究,使用新技术识别出了成千上万个基因中的不同5-羟甲基胞嘧啶(5-hydroxymethylcytosine,5hmC)变化模式,特别是与胰腺发育或功能相关的基因(GATA4、GATA6、PROX1、ONECUT1和MEIS2)以及与癌症发病相关的基因(YAP1、TEAD1、PROX1和IGF1)。
基于此,他们开发出一种新型表观基因组平台,可检测胰腺癌患者血液的循环游离DNA(cfDNA)中的5hmC变化,从而能够较早地实现对疾病的非侵入性精准检测,并能够更加及时地对患者采取治疗措施并提高患者的生存率。
11.Nat Commun:高通量诊断方法可提高癌症诊断效率
doi:10.1038/s41467-020-14381-2
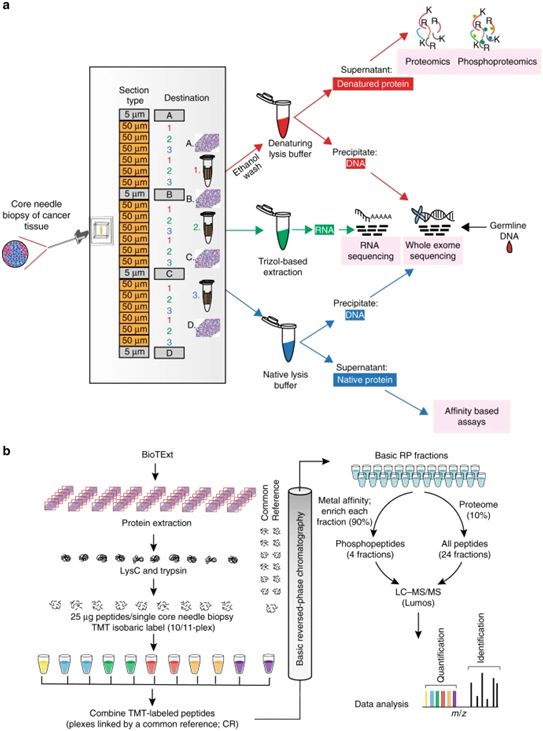
2020年1月,Shankha Satpathy等人开发了单针活检技术用于肿瘤诊断,基于这一技术,研究人员能够对癌症生物学取得更加深入的认识,从而有助于新型疗法的开发。这种新方法结合了基因组学与蛋白质组学的优势:使用来自患者肿瘤的单针核心活检分析了肿瘤遗传物质(基因组学)与深层蛋白质和磷蛋白表征(蛋白质组学)。
通过测试这项新技术,他们首次发现对ErbB2抗体抑制药物有反应的患者中检测到治疗后ERBB2蛋白磷酸化的显著降低,而在没有反应的患者中,没有发现这种蛋白磷酸化的下降。
12.Nat Commun:新技术提早4年诊断癌症!中外科学家开发突破性癌症早期诊断技术!
doi:10.1038/s41467-020-17316-z
2020年7月,Xingdong Chen等人开发出一种非侵入性血液测试,可以检测一个人是否患有五种常见癌症(胃癌、食道癌、结直肠癌、肺癌和肝癌),且可以比目前的癌症诊断方法早四年检测出癌症。这项被称为PanSeer的ctDNA甲基化多癌筛查技术可以在收集样本时无症状且仅在一到四年后被诊断为癌症的个体中检测出91%的癌症样本。此外,在收集样本时已经确诊的113名患者中,该检测准确地检测出了88%的癌症。该测试也识别出95%的无症状癌症样本。
他们强调,PanSeer试验不太可能预测哪些患者将会发展成癌症。相反,它最有可能识别已经出现癌性生长但目前的检测方法仍无法检测的患者。研究小组得出的结论是,还需要进一步的大规模纵向研究来确认该测试在预诊断个体中早期发现癌症的潜力。
13.Clin Cancer Res:一种特殊的新型工具有望帮助抵御黑色素瘤
doi:10.1158/1078-0432.CCR-20-2251
2020年11月,Gabriela Marsavela等人发现了一种癌症关键的血液标志物,它或许能帮助科学家们选择最有效的黑色素瘤疗法。他们发现,携带高水平ctDNA的患者或许会因抵御黑色素瘤的有效疗法而潜在获益,ctDNA是一种指示癌症的重要血液标志物;相关研究发现或许还能帮助临床医生有效开发新型的黑色素瘤疗法。
14.Clin Cancer Res:突破!新型血液检测技术或能更早地实现胰腺癌的诊断!
doi:10.1158/1078-0432.CCR-19-3313
2020年4月,Zijian Yang等人开发出一种新型的血液检测技术,分析了204名受试者(71名健康人,44名患有非PDAC胰腺疾病,89名患有PDAC)的血浆中的下列生物标志物:在他们开发的纳米磁性平台上分离并利用新一代测序或qPCR加以测量的肿瘤相关细胞外囊泡miRNA和mRNA;通过qPCR测量的循环无细胞DNA(cfDNA)浓度;通过液滴数字PCR检测的ccfDNA KRAS G12D/V/R突变,以及通过电化学发光免疫分析测量的CA19-9。他们将机器学习应用于训练集,随后在独立的、用户不知情的测试集中评估模型性能。
在一项包括47名患者(20名PDCA患者和27名无癌患者)的盲测试验中,这种新型检测技术的准确性能够达到92%,这明显优于当前利用CA19-9(准确性为89%)的检测手段;随后研究者利用癌症并未发生转移的25名患者机体的样本进行分析,他们发现,在对疾病分期上新型血液检测手段的准确性能达到84%,这明显高于当前的成像技术(64%)。
15.Open Chem:尿液分子可用于检测黑色素瘤
doi:10.1515/chem-2020-0143
2020年8月,Ivana Špaková等人使用一种简单且便宜的检测方法荧光光谱法对恶性黑色素瘤患者和健康对照者的尿液样本进行了分析,以查看荧光标记物的水平是否存在差异。与健康对照相比,来自恶性黑色素瘤患者的尿液样品含有不同水平的代谢相关荧光分子标志物。令人惊讶的是,尿液中荧光分子的水平与黑色素瘤的阶段以及与黑色素瘤进展相关的基因的表达相关,这表明该分子具有显着的生物标志物潜力,从而为监测该疾病提供了新的可能性。
其实,在过去的十年中,液体活检---利用血液等液体中循环的生物标志物来分析肿瘤---受到了极大的关注。以这种微创和可重复的方式检测和表征肿瘤的能力可能具有相当大的临床意义,而且在开发能够做到这一点的设备方面已经取得了巨大进展。比如,2020年8月8日,Guardant Health公司8日宣布,美国食品药品管理局(FDA)批准该公司开发的液体活检Guardant 360 CDx用于对所有实体瘤类型的综合基因组分析。同时,FDA批准Guardant 360 CDx作为伴随检测,在转移性非小细胞肺癌(NSCLC)患者中,确定携带表皮生长因子受体(EGFR)基因特定类型突变的患者。Guardant360 CDx检测采用新一代测序(NGS)技术可以同时检测55个肿瘤基因的突变,而不是一次检测一个基因。它可以让临床医生更好地评估肿瘤携带的多种基因突变。这是首个FDA批准将NGS和液体活检技术结合在一起,指导治疗决策的诊断测试。再比如,2020年8月26日,Foundation Medicine公司宣布FDA批准了其泛肿瘤液体活检产品FoundationOne Liquid CDx。该产品是一种基于下一代测序(NGS)的定性体外诊断(IVD)测试,利用晚期癌症患者的外周全血中分离的循环游离DNA(cfDNA)分析324个基因,可报告311个基因的短变异,包括BRCA1/2的重排和拷贝数丢失。
大量的工作,包括基于不同原理的各种各样的化验,已经把癌症研究团体弄糊涂了。此外,液体活检检测到的两种最成熟的生物标志物---CTC和cfDNA ---在分析前和分析步骤中存在技术上的差异。为了解决这些问题,并将液体活检交到更多的临床医生手中,研究机构现在必须集中精力证明这些生物标志物的效用。
观察性临床试验已经表明,CTC和cfDNA在不同类型的癌症中具有临床相关性。为了在临床指南中进一步证明它们的实用性和胶结液活检,需要进行介入临床试验。这些项目将利用从PROLipsY等研究项目中收集到的信息,并测试对CTC或cfDNA的检测是否可以用于帮助患者。例如,可以在治疗前采集血样,用于为患者匹配最佳药物。在治疗期间,定期的液体活检可以揭示持续或增加的CTC或cfDNA --这将表明对选择的治疗的耐药性。人们可以得到更有效的治疗,在肿瘤负担变得过度和无法治愈之前。定期的液体活组织检查也可以用来监测有复发风险的人。由于缺乏标准化,目前只能进行少量的介入性临床试验。
仍不清楚液体活检在多大程度上可能最终取代标准的组织活检。对于诊断原发肿瘤或判断组织中难以提取样本的转移病灶,液体活检可能是一个可靠的选择。液体活检还可以帮助避免侵入性组织活检后出现的并发症,如出血、感染和疼痛。
多年来,研究人员已经了解了液体活检的临床潜力。为了推动它们的广泛应用,现在需要更多的介入临床试验,以及开发一种算法来结合合适的循环生物标志物。这是政策制定者和产业界必须介入的领域。只有这样,这些优雅而强大的技术才能实现它们成为快速、可靠和非侵入性决策工具的承诺。(生物谷 Bioon.com)
参考文献:
1.Ayuko Hoshino et al. Extracellular Vesicle and Particle Biomarkers Define Multiple Human Cancers. Cell, 2020, doi:10.1016/j.cell.2020.07.009.
2.Paul K. Paik et al. Tepotinib in Non-Small-Cell Lung Cancer with MET Exon 14 Skipping Mutations. New England Journal of Medicine, 2020, doi:10.1056/NEJMoa2004407.
3.Anne Marie Lennon et al. Feasibility of blood testing combined with PET-CT to screen for cancer and guide intervention. Science, 2020, doi:10.1126/science.abb9601.
4.Jacob J. Chabon et al. Integrating genomic features for non-invasive early lung cancer detection. Nature, 2020, doi:10.1038/s41586-020-2140-0.
5.Jonathan C. M. Wan et al. ctDNA monitoring using patient-specific sequencing and integration of variant reads. Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aaz8084.
6.Peng Zhang et al. Molecular and functional extracellular vesicle analysis using nanopatterned microchips monitors tumor progression and metastasis. Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aaz2878.
7.Pier Vitale Nuzzo et al. Detection of renal cell carcinoma using plasma and urine cell-free DNA methylomes. Nature Medicine, 2020, doi:10.1038/s41591-020-0933-1.
8.David W. Cescon et al. Circulating tumor DNA and liquid biopsy in oncology. Nature Cancer, 2020, doi:10.1038/s43018-020-0043-5.
9.Yang Liu et al. Extracellular vesicle tetraspanin-8 level predicts distant metastasis in non–small cell lung cancer after concurrent chemoradiation. Science Advances, 2020, doi:10.1126/sciadv.aaz6162.
10.Gulfem D. Guler et al. Detection of early stage pancreatic cancer using 5-hydroxymethylcytosine signatures in circulating cell free DNA. Nature Communications, 2020, doi:10.1038/s41467-020-18965-w.
11.Shankha Satpathy et al. Microscaled proteogenomic methods for precision oncology. Nature Communications, 2020, doi:10.1038/s41467-020-14381-2.
12.Xingdong Chen et al. Non-invasive early detection of cancer four years before conventional diagnosis using a blood test. Nature Communications, 2020, doi:10.1038/s41467-020-17316-z.
13.Gabriela Marsavela et al. Circulating Tumor DNA Predicts Outcome from First-, but not Second-line Treatment and Identifies Melanoma Patients Who May Benefit from Combination Immunotherapy. Clinical Cancer Research, 2020, doi:10.1158/1078-0432.CCR-20-2251.
14.Zijian Yang et al. A multi-analyte panel consisting of extracellular vesicle miRNAs and mRNAs, cfDNA, and CA19-9 shows utility for diagnosis and staging of pancreatic adenocarcinoma. Clinical Cancer Research, 2020, doi:10.1158/1078-0432.CCR-19-3313.
15.Ivana Špaková et al. Fluorescence biomarkers of malignant melanoma detectable in urine. Open Chemistry, 2020, doi:10.1515/chem-2020-0143.
16.Catherine Alix-Panabières. The future of liquid biopsy. Nature, 2020, doi:10.1038/d41586-020-00844-5.
2017年6月,世界经济论坛与《科学美国人》杂志的专家委员会联合选出了2017年度全球十大新兴技术榜单,其中肿瘤的无创诊断技术成功入选并荣膺榜首。肿瘤无创诊断技术即液体活检(liquid biopsies)的出现,标志着人类在攻克肿瘤的道路上又前进了一大步。与传统的组织活检相比,液体活检具备实时动态检测、克服肿瘤异质性、提供全面检测信息等独特优势。
目前,在临床研究中,液体活检技术主要包括游离循环肿瘤细胞(CTC)检测、循环肿瘤DNA(ctDNA)检测、外泌体及循环RNA(Circulating RNA)检测等。癌症的发生与发展的过程中会释放一系列癌症组分到血液当中。液体活检就是通过分析血液中这些癌症组分,来实现癌症的早期筛查、分子分型、预后、用药指导以及复发监测等临床应用。针对2020年外泌体取得的进展,进行一番梳理,以飨读者。
1.Cell:液体样品检测可用于癌症的诊断
doi:10.1016/j.cell.2020.07.009
2020年8月,Ayuko Hoshino等人报道,肿瘤释放的细胞外囊泡和颗粒(extracellular vesicle and particle, EVP)可用于在早期阶段检测多种不同类型的癌症。他们使用了来自包括乳腺癌、结肠癌和肺癌在内的18种不同癌症的样本。通过使用计算生物学方法将特定的EVP蛋白特征与某些类型的癌症相匹配,他们发现计算机可以从样本中识别出不同类型的癌症,其灵敏度为95%,特异性为90%。

Cell, 2020, doi:10.1016/j.cell.2020.07.009。
2.NEJM:NEJM揭示特泊替尼治疗METex14跳跃突变的非小细胞肺癌显示持久的反应
doi:10.1056/NEJMoa2004407
2020年9月,Paul K. Paik等人在一项开放标签的2期临床试验(称为VISION)中发现MET外显子14 (METex14)跳跃突变的晚期非小细胞肺癌(NSCLC)患者对特泊替尼(tepotinib)治疗的客观响应率达到46.5%。
VISION临床试验还表明液体活检是检测突变的可靠方法,可用于可以确定患者对这种药物的反应。51例患者可获得基线和治疗时相匹配的液体活检样本。通过下一代测序,他们发现这些患者中有34人出现分子反应,表现为这种跳跃突变的消失或者大幅减少,射线成像证实68%的患者出现分子反应。
3.Science:血液测试有助于在症状出现之前发现癌症
doi:10.1126/science.abb9601
2020年4月,Anne Marie Lennon等人在数千名没有癌症病史或症状的人中,首次发现血液测试有助于检测多种癌症。这种血液测试仍然是实验性的。即便是它的支持者也说,它还需要改进,而且这些研究结果并不理想。然而,它们显示了在常规护理中使用这些基于基因的测试(称为液体活检)可能会带来哪些好处和不足---在这种情形下,使用PET扫描来确认或排除可疑的肿瘤。但是这种测试方法漏掉的癌症病例比发现的要多得多,而且还发出了一些错误的警报,从而导致不必要的后续程序。它仅在65至75岁的女性中进行研究,还需要在男性、其他年龄段和更加多样化的人群中进行研究。
4.Nature:科学家成功利用机器学习技术对肺癌患者进行早期诊断
doi:10.1038/s41586-020-2140-0
2020年3月,Jacob J. Chabon等人研究利用机器学习系统检测人类患者机体中的早期肺癌,并测试它寻找血液样本中的循环肿瘤DNA(ctDNA)的能力。他们训练机器学习模型,使其能够识别出与非小细胞肺癌相关的数据参数,一旦该机器模型进行了训练,其就能对既定患者的肺癌风险进行有效评估。在测试过程中,这种机器学习系统发现了63%的1期肺癌患者,虽然并不如CT扫描结果好,但其却能足以对高危肺癌患者进行早期筛查。
5.滴血验癌或成真!Science子刊报道个性化血液测试准确检测血液中的肿瘤DNA
doi:10.1126/scitranslmed.aaz8084
2020年6月,Jonathan Wan等人将循环的肿瘤DNA与肿瘤基因组图谱进行比较后,开发出一种计算方法,可以根据患者的肿瘤突变情况来查看血液中的许多DNA片段。通过这种个性化的测序方法,可以从血液中的一百万个DNA片段中检测出一个或几个带有突变的DNA片段。与以前的方法相比,这种方法的灵敏度提高了大约10倍。结合他们最近展示的从干血点中提取DNA序列的方法,他们认为从针扎血液样本中检测血液中的癌症水平是可能的。这在将来甚至可以在家里进行,并且可以在两次就诊之间更频繁地监测病人的病情。它还可以帮助远离癌症专科中心的人扩大癌症诊断的渠道。

图片来自Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aaz8084。
6.Science子刊:新型芯片实验室血液测试有望更早地发现癌症
doi:10.1126/scitranslmed.aaz2878
2020年6月,Peng Zhang等人开发出一种通用的高分辨率胶体喷墨打印方法,从而允许稳健地和可扩展地制造三维纳米图案聚二甲基硅氧烷/玻璃微流体芯片,用于分析血浆中的细胞外囊泡。对临床血浆标本的分析表明,这种微流体芯片平台可以用于癌症检测,包括在一个训练队列(n = 30,96.7%准确率)和一个独立的验证队列(n = 70,92.9%准确率)中,对年龄匹配的对照组和原位导管癌、浸润性导管癌或局部转移性乳腺癌患者的准确分类。通过临床验证,这种技术可以提供一种有用的液体活检工具,以改善癌症诊断和实时监测患者的肿瘤演变,从而为个性化治疗提供信息。
7.Nat Med:重大突破!生物标志物检测准确检测早期肾癌!
doi:10.1038/s41591-020-0933-1
2020年6月,Pier Vitale Nuzzo等人报道一种新的液体活检方法可以高精度地检测出肾癌,包括通常可以治愈但很难早期检测到的小的、局部的肾脏肿瘤。这种称为cfMeDIP-seq(cell-free methylated DNA immunoprecipitation and high-throughput sequencing, 无细胞甲基化DNA免疫沉淀和高通量测序)的方法并不寻找肿瘤脱落DNA的突变,而是检测找肿瘤脱落DNA上存在的异常甲基化。当在血液中利用这种方法区分肾癌患者和无肾癌患者时,它的准确率接近100%。这种方法在检测尿液样本时精确度较低,但是他们相信,性能可以提高。如果该方法在更大规模的试验中得到验证并广泛应用于临床,尿样的侵入性甚至会比抽血更小。
8.Nature子刊深度解读!基于ctDNA的液体活检技术在癌症诊断中的应用进展!
doi:10.1038/s43018-020-0043-5
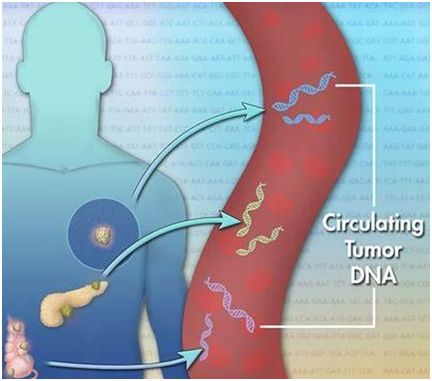
2020年3月,David W. Cescon等人深入分析了循环肿瘤DNA和肿瘤液体活检的研究进展;如今利用分析循环肿瘤DNA(ctDNA)来检测及监测癌症的技术越来越成熟,而且越来越多的研究证据揭示了该技术在诊断测试中的能力,ctDNA液体活检在实体瘤和恶性血液癌症中的诊断、特性分析及管理中的全部潜力将通过评估临床实用性的介入性临床试验来揭示。
他们从以下几方面进行了阐述,1)转移性实体瘤中的ctDNA;2)免疫疗法反应的基因组关联性;3)从临床试验到临床应用;4)ctDNA的动态变化和疗法反应;5)获得性耐药性的识别和特性分析;6)癌前诊断和筛查;7)引入基于ctDNA的癌症筛查;8)基于ctDNA的临床试验设计等。此外,他们讨论了ctDNA液体活检在癌症检测中的应用以及未来临床应用的前景。

图片来源:Wikimedia。
9.Science子刊:预测肺癌是否恶化的新型生物标志物
doi:10.1126/sciadv.aaz6162
2020年3月,Yang Liu等人评估了非小细胞肺癌(NSCLC)脱落的细胞外囊泡所携带的蛋白,以确定哪些蛋白可以作为转移性NSCLC细胞的标志物。他们发现了一种在转移性而非非转移性NSCLC细胞分泌的细胞外囊泡中高表达的蛋白:四次跨膜蛋白8(tetraspanin-8, Tspan8)。这种蛋白可以用作生物标志物,以开发出一种快速,微创的试验,以尽早发现可治愈的癌症。
10.Nat Commun:新型表观基因组平台或有望实现对早期胰腺癌的准确诊断
doi:10.1038/s41467-020-18965-w
2020年10月,Gulfem D. Guler等人纳入了307名40岁及以上的患者(64人患有胰腺导管腺癌,243人未患癌症)进行研究,使用新技术识别出了成千上万个基因中的不同5-羟甲基胞嘧啶(5-hydroxymethylcytosine,5hmC)变化模式,特别是与胰腺发育或功能相关的基因(GATA4、GATA6、PROX1、ONECUT1和MEIS2)以及与癌症发病相关的基因(YAP1、TEAD1、PROX1和IGF1)。
基于此,他们开发出一种新型表观基因组平台,可检测胰腺癌患者血液的循环游离DNA(cfDNA)中的5hmC变化,从而能够较早地实现对疾病的非侵入性精准检测,并能够更加及时地对患者采取治疗措施并提高患者的生存率。
11.Nat Commun:高通量诊断方法可提高癌症诊断效率
doi:10.1038/s41467-020-14381-2
2020年1月,Shankha Satpathy等人开发了单针活检技术用于肿瘤诊断,基于这一技术,研究人员能够对癌症生物学取得更加深入的认识,从而有助于新型疗法的开发。这种新方法结合了基因组学与蛋白质组学的优势:使用来自患者肿瘤的单针核心活检分析了肿瘤遗传物质(基因组学)与深层蛋白质和磷蛋白表征(蛋白质组学)。
通过测试这项新技术,他们首次发现对ErbB2抗体抑制药物有反应的患者中检测到治疗后ERBB2蛋白磷酸化的显著降低,而在没有反应的患者中,没有发现这种蛋白磷酸化的下降。

12.Nat Commun:新技术提早4年诊断癌症!中外科学家开发突破性癌症早期诊断技术!
doi:10.1038/s41467-020-17316-z
2020年7月,Xingdong Chen等人开发出一种非侵入性血液测试,可以检测一个人是否患有五种常见癌症(胃癌、食道癌、结直肠癌、肺癌和肝癌),且可以比目前的癌症诊断方法早四年检测出癌症。这项被称为PanSeer的ctDNA甲基化多癌筛查技术可以在收集样本时无症状且仅在一到四年后被诊断为癌症的个体中检测出91%的癌症样本。此外,在收集样本时已经确诊的113名患者中,该检测准确地检测出了88%的癌症。该测试也识别出95%的无症状癌症样本。
他们强调,PanSeer试验不太可能预测哪些患者将会发展成癌症。相反,它最有可能识别已经出现癌性生长但目前的检测方法仍无法检测的患者。研究小组得出的结论是,还需要进一步的大规模纵向研究来确认该测试在预诊断个体中早期发现癌症的潜力。
13.Clin Cancer Res:一种特殊的新型工具有望帮助抵御黑色素瘤
doi:10.1158/1078-0432.CCR-20-2251
2020年11月,Gabriela Marsavela等人发现了一种癌症关键的血液标志物,它或许能帮助科学家们选择最有效的黑色素瘤疗法。他们发现,携带高水平ctDNA的患者或许会因抵御黑色素瘤的有效疗法而潜在获益,ctDNA是一种指示癌症的重要血液标志物;相关研究发现或许还能帮助临床医生有效开发新型的黑色素瘤疗法。
14.Clin Cancer Res:突破!新型血液检测技术或能更早地实现胰腺癌的诊断!
doi:10.1158/1078-0432.CCR-19-3313
2020年4月,Zijian Yang等人开发出一种新型的血液检测技术,分析了204名受试者(71名健康人,44名患有非PDAC胰腺疾病,89名患有PDAC)的血浆中的下列生物标志物:在他们开发的纳米磁性平台上分离并利用新一代测序或qPCR加以测量的肿瘤相关细胞外囊泡miRNA和mRNA;通过qPCR测量的循环无细胞DNA(cfDNA)浓度;通过液滴数字PCR检测的ccfDNA KRAS G12D/V/R突变,以及通过电化学发光免疫分析测量的CA19-9。他们将机器学习应用于训练集,随后在独立的、用户不知情的测试集中评估模型性能。
在一项包括47名患者(20名PDCA患者和27名无癌患者)的盲测试验中,这种新型检测技术的准确性能够达到92%,这明显优于当前利用CA19-9(准确性为89%)的检测手段;随后研究者利用癌症并未发生转移的25名患者机体的样本进行分析,他们发现,在对疾病分期上新型血液检测手段的准确性能达到84%,这明显高于当前的成像技术(64%)。
15.Open Chem:尿液分子可用于检测黑色素瘤
doi:10.1515/chem-2020-0143
2020年8月,Ivana Špaková等人使用一种简单且便宜的检测方法荧光光谱法对恶性黑色素瘤患者和健康对照者的尿液样本进行了分析,以查看荧光标记物的水平是否存在差异。与健康对照相比,来自恶性黑色素瘤患者的尿液样品含有不同水平的代谢相关荧光分子标志物。令人惊讶的是,尿液中荧光分子的水平与黑色素瘤的阶段以及与黑色素瘤进展相关的基因的表达相关,这表明该分子具有显着的生物标志物潜力,从而为监测该疾病提供了新的可能性。
其实,在过去的十年中,液体活检---利用血液等液体中循环的生物标志物来分析肿瘤---受到了极大的关注。以这种微创和可重复的方式检测和表征肿瘤的能力可能具有相当大的临床意义,而且在开发能够做到这一点的设备方面已经取得了巨大进展。比如,2020年8月8日,Guardant Health公司8日宣布,美国食品药品管理局(FDA)批准该公司开发的液体活检Guardant 360 CDx用于对所有实体瘤类型的综合基因组分析。同时,FDA批准Guardant 360 CDx作为伴随检测,在转移性非小细胞肺癌(NSCLC)患者中,确定携带表皮生长因子受体(EGFR)基因特定类型突变的患者。Guardant360 CDx检测采用新一代测序(NGS)技术可以同时检测55个肿瘤基因的突变,而不是一次检测一个基因。它可以让临床医生更好地评估肿瘤携带的多种基因突变。这是首个FDA批准将NGS和液体活检技术结合在一起,指导治疗决策的诊断测试。再比如,2020年8月26日,Foundation Medicine公司宣布FDA批准了其泛肿瘤液体活检产品FoundationOne Liquid CDx。该产品是一种基于下一代测序(NGS)的定性体外诊断(IVD)测试,利用晚期癌症患者的外周全血中分离的循环游离DNA(cfDNA)分析324个基因,可报告311个基因的短变异,包括BRCA1/2的重排和拷贝数丢失。
大量的工作,包括基于不同原理的各种各样的化验,已经把癌症研究团体弄糊涂了。此外,液体活检检测到的两种最成熟的生物标志物---CTC和cfDNA ---在分析前和分析步骤中存在技术上的差异。为了解决这些问题,并将液体活检交到更多的临床医生手中,研究机构现在必须集中精力证明这些生物标志物的效用。

图片来源:https://cn.bing.com。
观察性临床试验已经表明,CTC和cfDNA在不同类型的癌症中具有临床相关性。为了在临床指南中进一步证明它们的实用性和胶结液活检,需要进行介入临床试验。这些项目将利用从PROLipsY等研究项目中收集到的信息,并测试对CTC或cfDNA的检测是否可以用于帮助患者。例如,可以在治疗前采集血样,用于为患者匹配最佳药物。在治疗期间,定期的液体活检可以揭示持续或增加的CTC或cfDNA --这将表明对选择的治疗的耐药性。人们可以得到更有效的治疗,在肿瘤负担变得过度和无法治愈之前。定期的液体活组织检查也可以用来监测有复发风险的人。由于缺乏标准化,目前只能进行少量的介入性临床试验。
仍不清楚液体活检在多大程度上可能最终取代标准的组织活检。对于诊断原发肿瘤或判断组织中难以提取样本的转移病灶,液体活检可能是一个可靠的选择。液体活检还可以帮助避免侵入性组织活检后出现的并发症,如出血、感染和疼痛。
多年来,研究人员已经了解了液体活检的临床潜力。为了推动它们的广泛应用,现在需要更多的介入临床试验,以及开发一种算法来结合合适的循环生物标志物。这是政策制定者和产业界必须介入的领域。只有这样,这些优雅而强大的技术才能实现它们成为快速、可靠和非侵入性决策工具的承诺。(生物谷 Bioon.com)
参考文献:
1.Ayuko Hoshino et al. Extracellular Vesicle and Particle Biomarkers Define Multiple Human Cancers. Cell, 2020, doi:10.1016/j.cell.2020.07.009.
2.Paul K. Paik et al. Tepotinib in Non-Small-Cell Lung Cancer with MET Exon 14 Skipping Mutations. New England Journal of Medicine, 2020, doi:10.1056/NEJMoa2004407.
3.Anne Marie Lennon et al. Feasibility of blood testing combined with PET-CT to screen for cancer and guide intervention. Science, 2020, doi:10.1126/science.abb9601.
4.Jacob J. Chabon et al. Integrating genomic features for non-invasive early lung cancer detection. Nature, 2020, doi:10.1038/s41586-020-2140-0.
5.Jonathan C. M. Wan et al. ctDNA monitoring using patient-specific sequencing and integration of variant reads. Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aaz8084.
6.Peng Zhang et al. Molecular and functional extracellular vesicle analysis using nanopatterned microchips monitors tumor progression and metastasis. Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aaz2878.
7.Pier Vitale Nuzzo et al. Detection of renal cell carcinoma using plasma and urine cell-free DNA methylomes. Nature Medicine, 2020, doi:10.1038/s41591-020-0933-1.
8.David W. Cescon et al. Circulating tumor DNA and liquid biopsy in oncology. Nature Cancer, 2020, doi:10.1038/s43018-020-0043-5.
9.Yang Liu et al. Extracellular vesicle tetraspanin-8 level predicts distant metastasis in non–small cell lung cancer after concurrent chemoradiation. Science Advances, 2020, doi:10.1126/sciadv.aaz6162.
10.Gulfem D. Guler et al. Detection of early stage pancreatic cancer using 5-hydroxymethylcytosine signatures in circulating cell free DNA. Nature Communications, 2020, doi:10.1038/s41467-020-18965-w.
11.Shankha Satpathy et al. Microscaled proteogenomic methods for precision oncology. Nature Communications, 2020, doi:10.1038/s41467-020-14381-2.
12.Xingdong Chen et al. Non-invasive early detection of cancer four years before conventional diagnosis using a blood test. Nature Communications, 2020, doi:10.1038/s41467-020-17316-z.
13.Gabriela Marsavela et al. Circulating Tumor DNA Predicts Outcome from First-, but not Second-line Treatment and Identifies Melanoma Patients Who May Benefit from Combination Immunotherapy. Clinical Cancer Research, 2020, doi:10.1158/1078-0432.CCR-20-2251.
14.Zijian Yang et al. A multi-analyte panel consisting of extracellular vesicle miRNAs and mRNAs, cfDNA, and CA19-9 shows utility for diagnosis and staging of pancreatic adenocarcinoma. Clinical Cancer Research, 2020, doi:10.1158/1078-0432.CCR-19-3313.
15.Ivana Špaková et al. Fluorescence biomarkers of malignant melanoma detectable in urine. Open Chemistry, 2020, doi:10.1515/chem-2020-0143.
16.Catherine Alix-Panabières. The future of liquid biopsy. Nature, 2020, doi:10.1038/d41586-020-00844-5.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


