Nature:全球近100种在研SARS-CoV-2疫苗,科学家如何找出理想的?
来源:本站原创 2020-05-03 08:23
2020年5月3日讯 /生物谷BIOON /——开发人员和资助者正在为疗效试验奠定基础,但可能只有少数疫苗能达到要求。在世界首次了解到这种新型冠状病毒导致致命肺炎后不到5个月,就有90多种疫苗处于不同的开发阶段,每周都会宣布有更多疫苗的出现。现在至少有6个已经在进行人体安全测试。现在,开发人员、资助者和其他利益相关者正在为他们迄今面临的最大挑战奠定基础:确定
2020年5月3日讯 /生物谷BIOON /——开发人员和资助者正在为疗效试验奠定基础,但可能只有少数疫苗能达到要求。
在世界首次了解到这种新型冠状病毒导致致命肺炎后不到5个月,就有90多种疫苗处于不同的开发阶段,每周都会宣布有更多疫苗的出现。现在至少有6个已经在进行人体安全测试。
现在,开发人员、资助者和其他利益相关者正在为他们迄今面临的最大挑战奠定基础:确定哪些疫苗确实有效。
这通常涉及给数千或数万人疫苗或安慰剂,在几个月甚至几年里观察是两组中有多少人感染、追踪他们的日常生活以检查是否出现安全问题。
但在这次大流行中,科学家必须加快和简化这一过程。疫苗可能是在人群中产生对该病毒免疫的唯一方法:尽管全世界有数百万的冠状病毒病例,一些初步研究表明,即使在疫情严重的地区,也只有一小部分人感染了SARS-CoV-2,而且他们的免疫能力还不清楚。
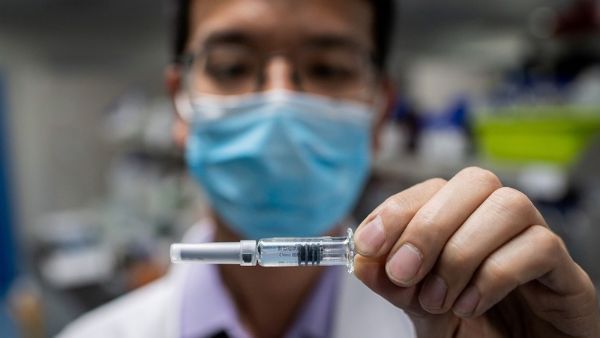
图片来源:Nicolas Asfouri AFP Getty
本月,位于瑞士日内瓦的世界卫生组织(WHO)草拟了一项临床试验计划,将在一项研究中测试多种疫苗。一些开发商和资助者计划进行自己的疗效试验。但是关键的问题仍然存在,比如哪些疫苗将首先进行测试--或者根本不进行测试--以及如何衡量和比较它们的有效性。
纽约市国际艾滋病疫苗行动组织(IAVI)主席兼首席执行官Mark Feinberg说:"这将需要一种以前从未真正发生过的协调水平,以及一种从未真正设想过的时间框架。"设在日内瓦的疫苗联盟Gavi的首席执行官Seth Berkley表示:"你无法将200种疫苗投入有效性试验。"该联盟为中低收入国家的免疫接种提供资金。
联合试验
世界卫生组织提出的团结疫苗试验试图通过适应性设计加快发展。这使得疫苗可以持续添加到试验中。参与者将被持续登记,那些似乎不起作用的疫苗可以从测试中退出。
位于巴黎的法国国立卫生与医学研究所的研究主任Marie-Paule Kieny说,世界卫生组织仍然需要敲定一些细节,比如如何衡量疫苗的有效性。但她认为其整体方法是合理的。她说:"其中一个挑战是确定优先次序--应该首先测试哪种疫苗。"
世界卫生组织已经建立了一个专家小组,将疫苗列入其试验的优先次序,但它不太可能是唯一的组织。Feinberg说:"在这项工作中,一些战略上的联合和协调将是至关重要的,否则将会变得非常混乱。世卫组织的计划只靠WHO本身可能是不够的"。
位于马里兰州贝塞斯达的美国国家卫生研究院(NIH)本月公布了与十多家公司的合作计划,旨在协调研发治疗冠状病毒的药物和疫苗。为疫苗开发提供资金的全球基金会--流行病防备联盟(CEPI)正在支持9种不同的疫苗。该组织的疫苗研发主任Melanie Saville说,该非营利性组织希望筹集20亿美元来支付有效性试验、生产和其他费用。
Kieny说,根据效力对疫苗进行优先排序的标准可能包括疫苗的生产能力、早期人体试验和动物研究中产生的免疫反应,以及监管机构对特定类型疫苗的经验。目前正在开发的一些疫苗,如RNA疫苗,还没有在人体中进行广泛测试,也没有用于获得监管批准的疫苗中。
英国牛津大学詹纳研究所(Jenner Institute)开发的一种疫苗目前正在进行早期试验。"我们很有可能在未来几个月里观察到疫苗的有效性,"领导这项试验的牛津大学传染病研究员Andrew Pollard在网上新闻发布会上说。
IAVI的项目负责人Rip Ballou说,少数有计划和资金获得疫苗批准并扩大生产的开发人员可能会决定如何进行疗效试验。他表示:"如果不与一项计划结合起来,在一些监管机构的授权下进行三期临床试验以证明其有效性,那就毫无意义。只有少数疫苗能达到这个高度。否则,它就只是出版物,而不是疫苗。"
一个公平的机会
另一个挑战是确定不同疫苗之间的相互比较。世卫组织关于有效性试验的建议可能允许直接比较不同疫苗的性能,但Kieny认为,一些开发人员可能不愿意接受这一点,因为这可能会损害疫苗的商业前景。
IAVI的副总裁和新发传染病和科学策略组织领导人Swati Gupta说疫苗开发人员想在进行需要与其他疫苗试验比较的实验之前了解关键决策,以确保他们的疫苗"有公平的机会能够显示其疗效"。
但伦敦惠康基金会(Wellcome Trust)生物医学慈善机构的疫苗负责人Charlie Weller表示,能够比较不同的疫苗至关重要,即使这要求疫苗开发商将短期利益放在一边。"如果他们在商业模式下工作。这对我们现在的情况是行不通的。"
预计全球对冠状病毒疫苗的需求可能会使开发人员更愿意合作。"我们需要不止一种疫苗,"Kieney说。"垄断总是非常糟糕,没有一个疫苗公司可能有足够的生产能力。"
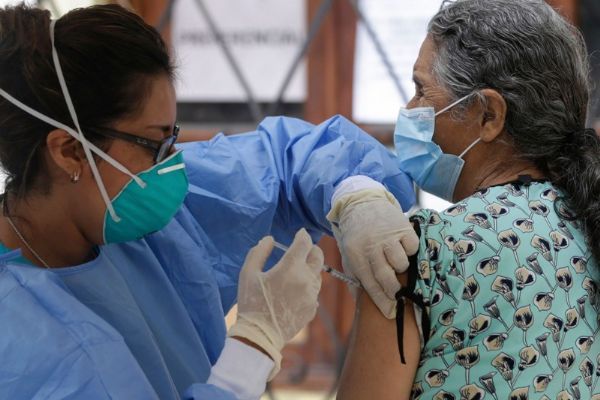
图片来源:Martin Mejia AP Shutterstock
能够鼓励这种合作的一个因素是大流行地域的变化。"如果两个月前在武汉进行疗效试验,中国会是一个很好的地方,"Berkley说。"一个月前,意大利会是一个做这件事的好地方。因此,开发人员有动机加入世界卫生组织或美国国立卫生研究院的项目,因为他们可以利用世界各地的临床试验基础设施,将疫苗带到有冠状病毒病例的地方。我们需要变得灵活。
紧急使用
虽然大多数专家认为大规模试验是确保冠状病毒疫苗安全和有效的必要手段,但一些开发人员正在研究替代方案。
一种选择是确定一种疫苗在涉及数百名参与者的早期试验中是否有效的迹象,然后向监管机构寻求许可,根据"紧急使用"规则在高危人群中部署疫苗,比如医护人员,他们更有可能感染冠状病毒。美国FDA等监管机构可以批准紧急使用,同时收集额外数据以获得疫苗的许可。
中国天津的Cansino Biologics正在开发一种由化学灭活的SARS-CoV-2病毒组成的疫苗。该公司发言人表示,该公司将考虑采用这种方法。而强生公司在一份新闻稿中表示,其疫苗可于2021年初投入紧急使用。
世卫组织免疫、疫苗和生物制品司司长Katherine O'Brien说,从未根据紧急使用规定部署过疫苗。如果冠状病毒疫苗遵循这一途径,监管机构将寻求额外的保证,以确保疫苗是安全的。"在安全问题上没有妥协的余地。"
一项更激进的提议正在形成,以确定哪种疫苗有效:有意让年轻、健康的志愿者感染,从而消除了等待试验参与者自然感染的需要。这些"人类挑战"研究已经被用于研究疟疾和登革热等传染病,一些研究人员说,应该考虑这些研究来加快冠状病毒疫苗的开发。
Berkley说,挑战性试验可以用来迅速确定哪些疫苗可以进行大规模试验。但他认为,如果既没有有效的药物,也没有基因测试来识别那些可能患上严重疾病的罕见的年轻人,这样做的风险可能太大。他说:"在你得到公认的治疗之前,我认为这是一个相当艰难的过程。"(生物谷Bioon.com)
参考资料:
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->