2022年6月Cell期刊精华
来源:生物谷原创 2022-06-30 16:39
2022年6月份即将结束,6月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
2022年6月份即将结束,6月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:从结构上揭示人核外切体靶向复合物的RNA监测机制
doi:10.1016/j.cell.2022.04.016
在生物学中,清除东西可能与制造东西一样重要。细胞、蛋白或其他不再需要的分子的堆积会导致问题,因此生物已经进化出几种清理它们的方法。一个典型的例子是RNA外切体(exosome,注意是外切体,而不是外泌体,虽然这两者的英文单词都是一样的)。RNA分子在细胞中发挥许多作用。它们中的一些被翻译成蛋白;另一些形成了细胞的蛋白构建复合物。RNA外切体是一种细胞分子机器,可以降解有问题、有害或不再需要的RNA分子。如果没有这种微小的分子机器来修剪那些不能激发快乐的东西,我们的细胞将成为功能失调的囤积者,无法发挥作用。
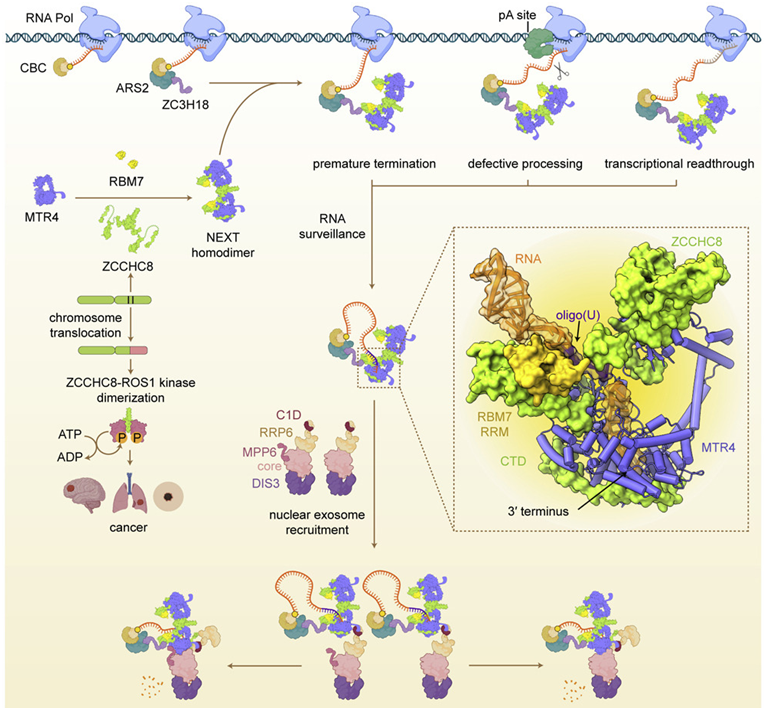
图片来自Cell, 2022, doi:10.1016/j.cell.2022.04.016。
在一项新的研究中,纪念斯隆-凯特琳癌症中心结构生物学项目主席Christopher Lima博士和Lima实验室博士后研究员M. Rhyan Puno提出了有助于解释RNA外切体如何定位需要被降解的RNA的研究结果。在低温电镜(cryo-EM)---一种先进的成像技术---的帮助下,他们能够破译一种名为人核外切体靶向(Nuclear Exosome Targeting, NEXT)复合物的蛋白组装体的结构,这种蛋白组装体是这种降解机制的一个关键部分。相关研究结果发表在2022年6月9日的Cell期刊上,论文标题为“Structural basis for RNA surveillance by the human nuclear exosome targeting (NEXT) complex”。
如今,通过低温电镜,他们获得了NEXT与RNA结合在一起的第一批清晰图片。这些图片,与伴随的生物化学和生物学实验一起,为RNA分子如何被递送给RNA外切体进行降解提供了新线索。
2.Cell:基于CRISPR技术的新型图谱将每个人类基因与其功能关联在一起
doi:10.1016/j.cell.2022.05.013
人类基因组计划(Human Genome Project)是一项雄心勃勃的举措,旨在对人类的每个DNA片段进行测序。该项目吸引了来自世界各地研究机构(包括包括怀特黑德研究所)的合作者,并最终于2003年完成。如今,二十多年过去了,怀特黑德研究所成员Jonathan Weissman及其同事们在一项新的研究中超越了人类基因组序列,首次全面地构建出人类细胞中表达的基因的功能图谱。相关研究结果于2022年6月9日在线发表在Cell期刊上,论文标题为“Mapping information-rich genotype-phenotype landscapes with genome-scale Perturb-seq”。他们将每个基因与它在细胞中的作用联系起来,这是多年来在单细胞测序方法Perturb-seq上合作的成果。
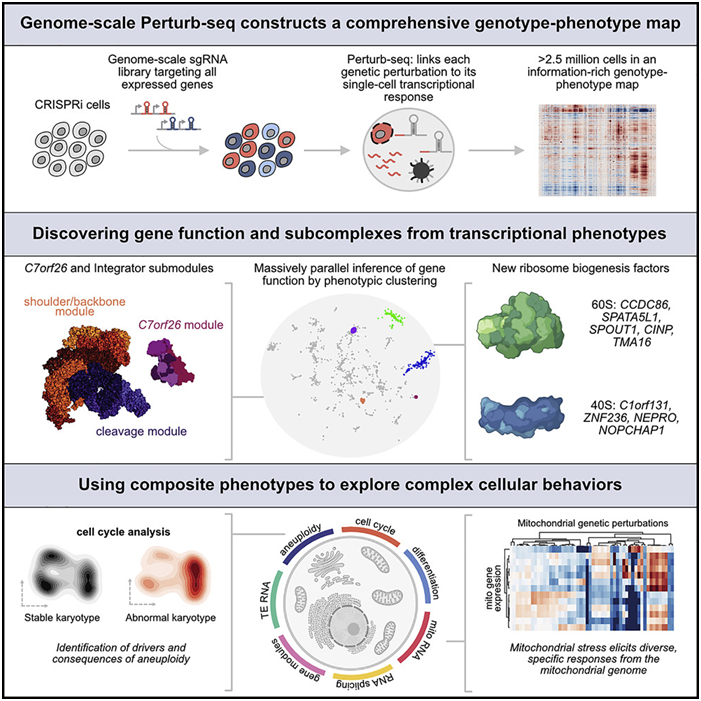
图片来自Cell, 2022, doi:10.1016/j.cell.2022.05.013。
这些数据可以在Weissman实验室的网站上找到,供其他科学家使用。Weissman说,“这是一个大资源,就像人类基因组是一个大资源一样,你可以进去并进行基于发现的研究。与其提前确定你要研究的生物学,不如拥有这张基因型-表型关系图,你可以进去筛选这个数据库,而不必做任何实验。”
这种筛选使得这些作者能够深入研究各种生物学问题。他们用它来探索功能未知的基因对细胞的影响,研究线粒体对应激的反应,并筛选出导致染色体丢失或增加的基因,一种在过去被证明很难研究的表型。论文共同通讯作者、前Weissman实验室博士后Tom Norman说,“我认为这个数据集将使那些来自生物学其他领域的人能够进行各种我们甚至还没有想到的分析,突然之间他们就有了可以利用的数据。”
3.Cell:遗传进化和微环境相互作用导致胶质瘤进展
doi:10.1016/j.cell.2022.04.038
在一项新的研究中,来自荷兰阿姆斯特丹大学、美国杰克逊基因组医学实验室和哥伦比亚大学医学中心等研究机构的研究人员发现作为一种常见的大脑和脊髓肿瘤,浸润性胶质瘤(infiltrating glioma)是由其遗传进化和微环境决定的,这一发现可能导致更有针对性的治疗。相关研究结果发表在2022年6月9日的Cell期刊上,论文标题为“Glioma progression is shaped by genetic evolution and microenvironment interactions”。
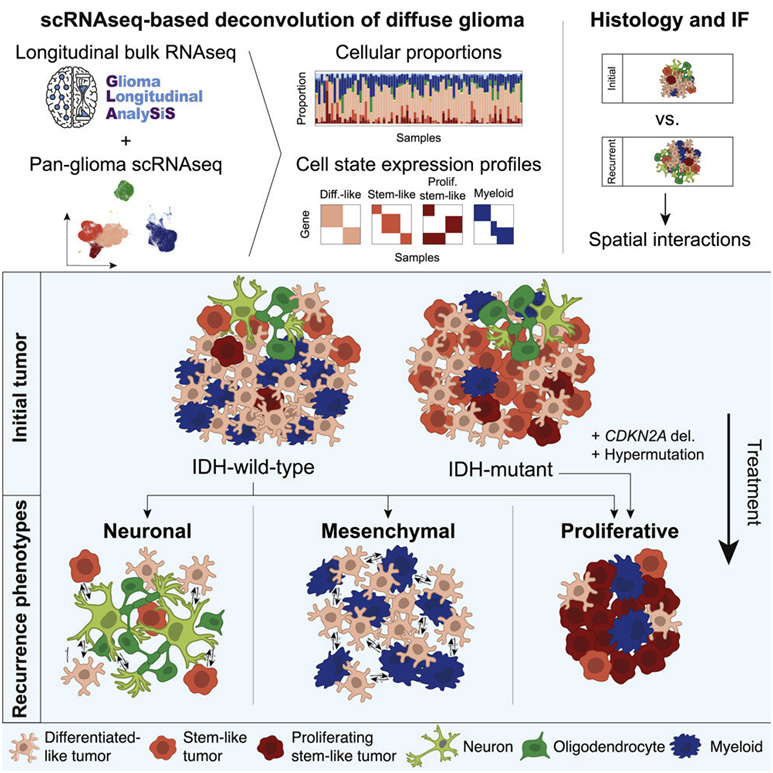
图片来自Cell, 2022, doi:10.1016/j.cell.2022.04.038。
论文共同作者、科罗拉多大学癌症中心成员D.Ryan Ormond博士说,“我们确定了复发时的表观遗传学改变,这些改变不仅在某些病例中具有预后作用,而且可能导致针对不同亚型的不同治疗方案,从而改善长期生存。”
这些作者观察了胶质瘤如何与大脑相互作用,随着时间的推移发生变化,产生治疗抵抗性并变得更具侵袭性。他们确定了胶质瘤复发时的三种不同表型,或者说可观察到的特征---神经元型、间充质型和增殖型。它们中的每一种都细胞、遗传和组织学特征,这些特征在复发时会显现出来。其的一些特征与不太有利的结果有关。
4.Cell:发现α-突触核蛋白的双重功能
doi:10.1016/j.cell.2022.05.008
帕金森病(PD)的特征之一是一种称为α-突触核蛋白(alpha-synuclein, )的蛋白在大脑中的积累。二十多年来,α-突触核蛋白一直是对帕金森病感兴趣的科学家们、临床医生和药物制造商关注的焦点。但是,α-突触核蛋白的功能还没有得到很好的理解。
在一项新的研究中,来自布莱根妇女医院、哈佛干细胞研究所、布罗德研究所的研究人员对α-突触核蛋白的作用有了新的认识,揭示了该蛋白与帕金森病及相关疾病相关的新功能。相关研究结果发表在2022年6月9日的Cell期刊上,论文标题为“The Parkinson’s disease protein alpha-synuclein is a modulator of processing bodies and mRNA stability”。
论文通讯作者、布莱根妇女医院神经病学系运动障碍科主任Vikram Khurana博士说,“我们的研究为α-突触核蛋白提供了新的见解,这种蛋白被认为是帕金森病和相关疾病产生的核心。目前的治疗方法靶向这种蛋白,但是它的功能一直不明确。传统上,α-突触核蛋白被认为在与细胞膜结合和称为囊泡的运输结构中发挥了作用。但我们的研究表明α-突触核蛋白有双重身份。”
Khurana及其同事们的最初线索来自于α-突触核蛋白毒性的酵母和果蝇模型,并通过对人类细胞、患者衍生的神经元和人类遗传学的研究得到证实。他们发现α-突触核蛋白与囊泡相互作用的部分也与称为处理小体(processing body, P-body)的结构结合,其中P-body是细胞中通过信使RNA(mRNA)调节基因表达的分子机器。在由源自携带α-突触核蛋白基因突变的PD患者的诱导性多能干细胞产生的神经元中,P-body的生理结构和功能丧失,mRNA遭受异常调控。同样的情况也发生在来自患者死后大脑的组织样本中。人类基因分析支持了这些发现的疾病相关性:在P-body基因中积累突变的患者似乎有更高的PD风险。
5.Cell:揭示抑制PAAN核酸酶可预防帕金森病中的神经退化
doi:10.1016/j.cell.2022.04.020
在一项新的针对小鼠的研究中,来自约翰霍普金斯大学医学部的研究人员发现一种化合物可以阻止与帕金森病中脑细胞死亡有关的通路中的最后事件。他们说,这一实验结果可能推动一种药物的开发,这种药物可以安全在人体中使同一通路短路,并防止帕金森病、中风和其他神经退行性疾病特有的破坏性影响。相关研究结果发表在2022年5月26日的Cell期刊上,论文标题为“PAAN/MIF nuclease inhibition prevents neurodegeneration in Parkinson’s disease”。
帕金森病的特点是错误折叠的α-突触核蛋白(alpha synuclein)在负责产生一种叫做多巴胺的神经递质的脑细胞中堆积起来。随着更多错误折叠的蛋白聚集在一起,它们通过Dawson和其他约翰霍普金斯大学研究人员确定的所谓“程序化”细胞死亡过程杀死脑细胞。这一过程被称为PARP-1依赖性细胞死亡(parthanatos),可导致运动、情绪调节和思维方面的障碍。
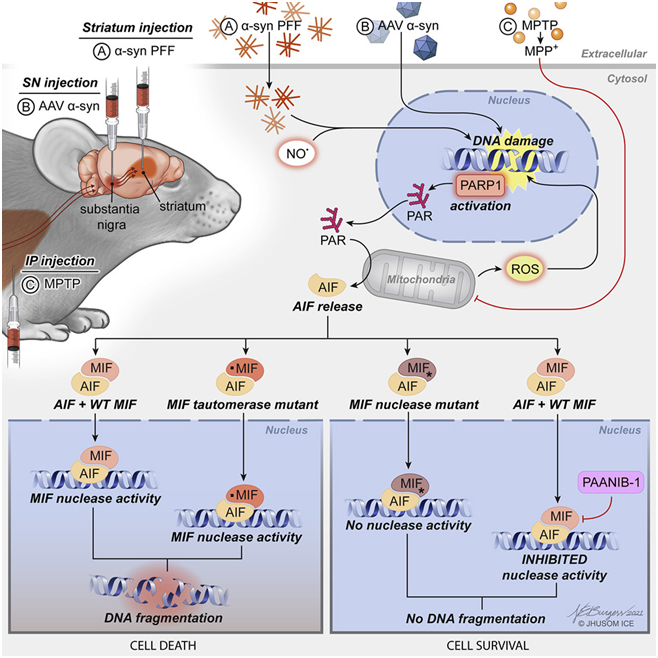
图片来自Cell, 2022, doi:10.1016/j.cell.2022.04.020。
Dawson领导的先前研究已表明一种称为parthanatos相关凋亡诱导因子核酸酶(parthanatos associated apoptosis-inducing factor nuclease, PAAN)的蛋白对受α-突触核蛋白聚集物影响的脑细胞进行最后打击,破坏细胞的DNA。除了帕金森病之外,PAAN蛋白还与中风中的细胞死亡有关。然而,PAAN在大脑中有多种功能,包括在免疫系统中的活性,这些活性需要维持以保持大脑的健康。
利用对PAAN分子结构的了解,这些作者在约翰霍普金斯大学药物文库中筛选了数千种已知的化学物,以寻找那些能特异性阻止PAAN分解DNA分子的化学物。他们通过在这些化学品存在的情况下将一系列的DNA链暴露于PAAN中来完成这一工作。如果加入一种化学物后DNA保持完整,那么他们就认为它有可能阻止PAAN对DNA的破坏。他们在这些测试中发现了一种能阻断PAAN而不影响其他重要PAAN活性的化学物,并将它命名为PAANIB-1(PAAN inhibitor 1, 即PAAN抑制剂1)。
6.Cell:揭示复杂的模式在组织发育过程中如何产生
doi:10.1016/j.cell.2022.04.023
早期发育就像一场精心编排的舞蹈,整齐划一的细胞排列成复杂的模式---这是向形成功能性器官迈出的第一步。例如,一层扁平的皮肤细胞必须在经过转变后布满整齐排列的毛细胞和汗腺。在一项新的研究中,来自洛克菲勒大学的研究人员揭示了发育模式可以从细胞集合体和围绕它们的胞外基质(ECM)之间的物理相互作用中自发产生。这类相互作用产生了类似于流体的特性,允许形成类似于挡风玻璃上的水膜如何缩回成水滴的模式。相关研究结果发表在2022年5月26日的Cell期刊上,论文标题为“Reciprocal cell-ECM dynamics generate supracellular fluidity underlying spontaneous follicle patterning”。论文通讯作者洛克菲勒大学形态发生实验室的Amy Shyer和Alan Rodrigues。
这些作者使用鸡皮作为模型系统,发现细胞之间的机械力打破了这种组织的对称性,促使这些细胞聚集成周期性间隔的细胞束,随后在整个皮肤组织中长出羽毛。这些结构变化引发了次级基因表达变化,导致经典的分子信号传递,从而进一步推动了发育。这些发现使人们对参与器官塑造的物理因素有了更好的了解。
Shyer说,“器官发育涉及机械过程和分子过程之间的持续合作。了解这种反馈回路中各步骤的精确顺序可能有助于我们修复组织或从新的角度研究肿瘤形成。”
7.Cell:首次公布了四种COVID-19疫苗的正面比较结果
doi:10.1016/j.cell.2022.05.022
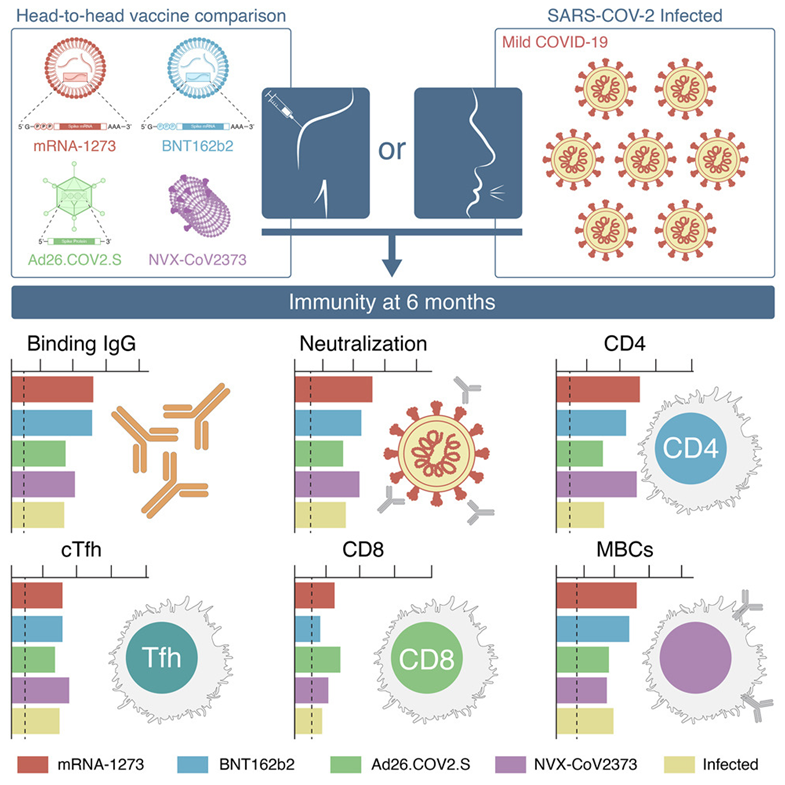
在一项新的研究中,来自拉霍亚免疫学研究所(LJI)的研究人员首次发表了关于四种类型的COVID-19疫苗如何使身体准备好对抗SARS-CoV-2的分析。他们深入研究了T细胞、B细胞、抗体水平在接种疫苗后六个月内的变化情况,这对了解如何在正在进行的COVID-19大流行病期间保护人们至关重要。相关研究结果于2022年5月26日在线发表在Cell期刊上,论文标题为“Humoral and cellular immune memory to four COVID-19 vaccines”。
图片来自Cell, 2022, doi:10.1016/j.cell.2022.05.022。
这项新的研究是历史上首次比较三种不同的疫苗平台如何触发对同一病原体的免疫反应的研究。
这些作者研究了人类对mRNA平台(Pfizer-BioNTech COVID-19疫苗和Moderna COVID-19疫苗)、基于重组蛋白的佐剂疫苗平台(Novavax)和基于病毒载体的平台(Janssen/J&J)的免疫反应。这项新的研究中的所有四种疫苗都是为了让免疫系统准备好对抗同一种靶标,即SARS-CoV-2刺突蛋白。
8.Cell:揭示非编码7S RNA调节人类线粒体中基因表达机制
doi:10.1016/j.cell.2022.05.006
在一项新的研究中,来自瑞典哥德堡大学、卡罗林斯卡学院和德国科隆大学的研究人员发现一种非编码RNA分子调节着人类细胞中的线粒体基因表达。相关研究结果于2022年6月2日在线发表在Cell期刊上,论文标题为“Non-coding 7S RNA inhibits transcription via mitochondrial RNA polymerase dimerization”。论文通讯作者为哥德堡大学教授Maria Falkenberg和卡罗林斯卡医学院的B. Martin Hällberg。论文第一作者为哥德堡大学的Xuefeng Zhu和Xie Xie以及卡罗林斯卡学院的Hrishikesh Das。
人类线粒体7S RNA属于哺乳动物正常发育所必需的一个较大的非编码RNA分子家族。以前人们知道,线粒体7S RNA的水平根据真核细胞的代谢需要而变化,但这些变化的分子基础和功能影响尚不清楚。在这项新的研究中,这些作者开发出研究7S RNA对纯化的蛋白和细胞中线粒体基因活动的影响的方法。
这些作者发现7S RNA具有调节功能,因为它在体外和培养的人类细胞中控制线粒体的转录水平。通过使用低温电镜(cryo-EM)技术,他们发现线粒体RNA聚合酶POLRMT通过与7S RNA相互作用发生二聚化。由此产生的POLRMT二聚体界面封存了启动子识别和线粒体DNA解链所需的结构域,从而阻止了线粒体DNA转录启动。他们提出,非编码7S RNA分子是调节哺乳动物细胞线粒体转录的负反馈回路的一个组成部分。
9.Cell:更为紧凑的靶向RNA的基因编辑工具Cas7-11S问世,有望基于此开发出新型RNA基因疗法
doi:10.1016/j.cell.2022.05.003
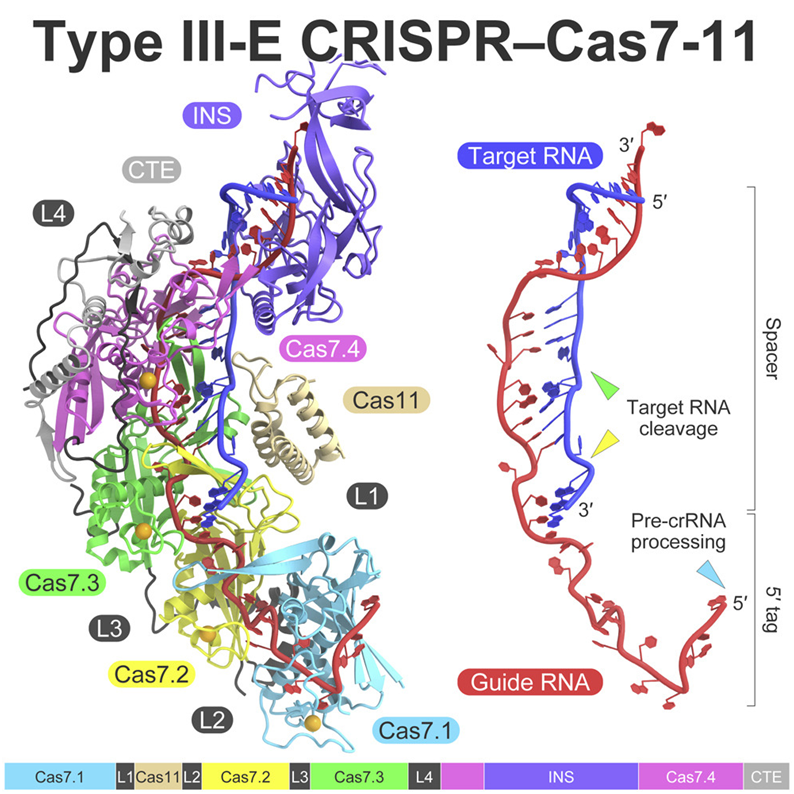
去年,来自麻省理工学院麦戈文脑科研究所的研究人员发现了III-E型CRISPR-Cas效应蛋白Cas7-11并表征了它的特征,它是第一种能够对RNA链进行精确、有指导性的切割而在此过程中不伤害细胞的CRISPR 酶(Nature, 2021, doi:10.1038/s41586-021-03886-5)。如今,在一项新的研究中,他们与东京大学的合作者合作,发现Cas7-11可以缩小到一个更紧凑的版本,使其成为编辑活细胞内RNA的一种更可行的选择。他们描述了这种新的、紧凑的Cas7-11,同时还对原始的Cas7-11进行了详细的结构分析。
相关研究结果于2022年5月27日在线发表在Cell期刊上,论文标题为“Structure and engineering of the type III-E CRISPR-Cas7-11 effector complex”。论文通讯作者为麦戈文脑科研究所研究员Omar Abudayyeh、麦戈文脑科研究所研究员Jonathan Gootenberg和东京大学研究员Hiroshi Nishimasu。论文第一作者为麦戈文脑科研究所前博士后Nathan Zhou和东京大学的Kazuki Kato。
图片来自Cell, 2022, doi:10.1016/j.cell.2022.05.003。
Abudayyeh说,“当我们观察这种结构时,很明显有一些不需要的部分,我们实际上可以去除这些部分。这使得这种酶足够小,以至于可以将它装入在单一的病毒载体中进行治疗应用。”
这些作者认为Cas7-11的新三维结构是一种丰富的资源,可以回答有关这种酶的基本生物学问题,并揭示未来调整它的功能的其他方法。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


