Nature:根据结构对EGFR突变进行分类可更好地为非小细胞肺癌患者匹配靶向疗法
来源:本站原创 2021-09-19 07:39
2021年9月19日讯/生物谷BIOON/---在一项新的研究中,来自美国德克萨斯大学MD安德森癌症中心的研究人员发现,按结构和功能对表皮生长因子受体(EGFR)突变进行分组,为非小细胞肺癌(NSCLC)患者匹配合适的药物提供了一个准确的框架。这一发现确定了四个突变亚群,并介绍了测试酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TK
2021年9月19日讯/生物谷BIOON/---在一项新的研究中,来自美国德克萨斯大学MD安德森癌症中心的研究人员发现,按结构和功能对表皮生长因子受体(EGFR)突变进行分组,为非小细胞肺癌(NSCLC)患者匹配合适的药物提供了一个准确的框架。这一发现确定了四个突变亚群,并介绍了测试酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI)的新策略,以及获得批准的靶向疗法的临床机会。相关研究结果于2021年9月15日在线发表在Nature期刊上,论文标题为“Structure-based classification predicts drug response in EGFR-mutant NSCLC”。

论文通讯作者、德克萨斯大学MD安德森癌症中心胸/头颈肿瘤内科主任John Heymach医学博士说,“70多种不同的EGFR突变已经在患者身上被发现,但只有靶向其中的一些突变的药物被获批上市。我们的研究的直接影响之一是发现我们已有的靶向疗法可能对其中的许多突变有效。对于某些突变,旧的药物实际上可能效果更好,而对于其他突变,新的药物效果更好。眼下,在缺乏指导的情况下,临床医生经常对所有EGFR突变使用最新的治疗方法。这些新的发现可以帮助我们立即为患者挑选更好的疗法,并希望为特定的突变亚群开发更好的药物。”
第一代、第二代和第三代TKI使用不同的机制来靶向EGFR蛋白。Heymach和他的团队发现,根据特定突变亚群中的突变如何影响EGFR蛋白上的药物结合口袋,药物对某些突变亚群的效果更好。
Heymach团队确定的四种EGFR突变NSCLC亚群是:(1)经典类突变,对药物结合几乎没有影响;(2)T790M样突变,在疏水性裂缝中至少含有一个突变,而且往往是在对第一代靶向治疗产生抗药性后获得的;(3)外显子20环插入突变,其特征是在外显子20中αC螺旋的C端之后的环中插入了额外的氨基酸;(4)在ATP结合口袋的内表面或αC螺旋的C端发生的P环αC螺旋压缩(P-loop αC-helix compression, PACC)突变。
目前在EGFR突变的NSCLC中测试新药物的方法是基于外显子编号,这表明突变发生在DNA的线性部分。按外显子对突变进行分组,在临床研究和实验室模型中产生了大部分异质性的结果,这些作者指出,这似乎表明外显子编号和药物敏感性或耐药性之间的相关性很差。
Heymach说,“在一个给定的外显子内,突变的差异很大。我们根据突变如何影响EGFR结构和药物结合来组织突变,这使得我们可以同时在一整组结构相似的突变中测试药物。我们相信这可能成为对突变进行分类和描述的新标准方法,然后将它们与正确的药物配对。”
大数据显示了非典型突变的多样性
在北美约有15%的NSCLC存在EGFR蛋白的突变,在亚洲约有30%至40%的NSCLC是如此。总体而言,存在70多种不同类型的EGFR突变。“经典的”EGFR突变往往对美国食品药品管理局(FDA)批准的靶向疗法反应良好,但对于其余的“非典型的”EGFR突变,一直缺乏有效的治疗方法和指南。
在这项新的研究中,Heymach团队分析了来自五个不同患者数据库的16175名EGFR突变NSCLC患者的数据。11619名患者的主要和共同发生的突变被记录下来,其中,67.1%的人有经典的EGFR突变,30.8%的人有非典型的EGFR突变,2.2%的人两者都有。
为该研究提供详细的分子和结果信息的关键数据库之一是基因组标志物指导治疗计划(Genomic Marker-Guided Therapy Initiative, GEMINI),这是肺癌登月计划(MD安德森登月计划的一部分)的一个大数据项目。MD安德森登月计划旨在加速将科学发现发展为拯救患者生命的临床进展。
对于经典和非典型的EGFR突变,Heymach团队分析了治疗失败的时间(time to treatment failure, TTF),这是癌症对靶向疗法产生抗性的速度的一个指标。他们发现,无论治疗类型如何,非典型突变患者的TTF较短,总生存期较短。用第一代和第三代TKI治疗的经典突变患者的TTF更长。
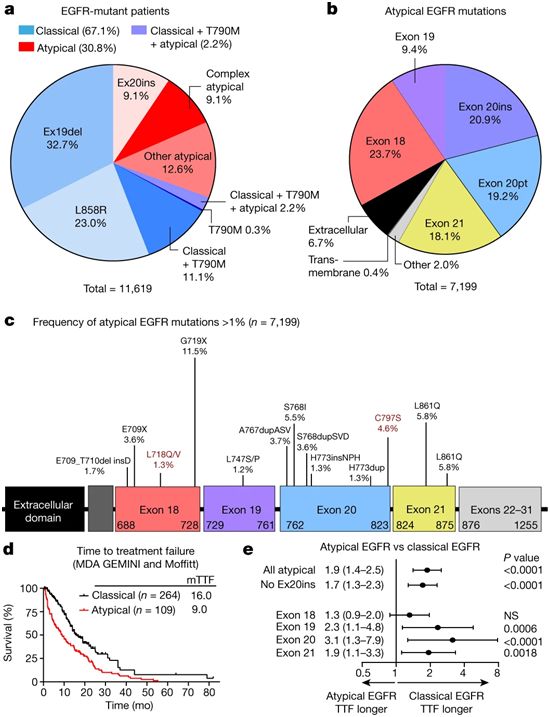
非典型EGFR突变与较差的患者预后相关,图片来自Nature, 2021, doi:10.1038/s41586-021-03898-1。
Heymach团队随后创建了76个具有EGFR突变的细胞系,并针对18种EGFR抑制剂对这些细胞系进行了筛选,从而发现了四种不同的EGFR突变亚群。比较不同亚群与外显子的药物敏感性的相关性,显示基于结构的亚群比基于外显子的亚群更具预测性。通过分类和回归树分析数据,机器学习进一步验证了这种基于结构的亚群方法的有效性。
经典类突变对所有类别的TKI都很敏感,特别是第三代TKI。外显子20环插入突变仍然是最异质的亚群,其中的某些突变对第二代TKI反应最好。T790M样突变对ALK抑制剂和PKC抑制剂敏感,其中的一些突变对第三代TKI保持敏感。PACC突变对第二代TKI最敏感。
论文第一作者、德克萨斯大学MD安德森癌症中心胸/头颈肿瘤内科助理教授Jacqulyne Robichaux博士说,“蛋白质不是线性的,所以当我开始考虑如何将正确的药物与患者身上的正确突变相匹配时,按外显子对突变进行分组似乎不是一种直观的方法。蛋白质是三维的,这促使我们调查EGFR蛋白质中是否有与发生突变时的药物敏感性相关的区域,这就是我们如今所发现的。这些亚群在结构上有共同的属性,与它们的功能直接相关,并比传统方法更好地回顾性预测了患者的结果。”
进一步强调下一代测序的作用和未来的研究
这项新的研究还强调了对所有新诊断或复发的NSCLC患者进行生物标志物检测的重要性。目前的下一代测序方法有能力检测已知致癌驱动EGFR突变的全部范围,几乎所有的突变都属于这四种基于结构的亚群之一。这些作者指出,这对罕见的突变尤其重要,因为这些罕见的突变更难通过基于单个突变的传统临床试验方法来研究。未来的前瞻性研究将有助于完善这个亚群框架并为其提供信息。
Heymach说,“这对患者来说是一个重要的进展,因为目前FDA还没有批准靶向大多数EGFR突变的靶向治疗,这让临床医生对针对哪种突变使用哪种药物一无所知。如今,根据突变所处的结构亚群,我们可以更好地为特定突变匹配最佳药物。展望未来,这也可能有助于集中药物开发工作,通过对结构相似的整组突变进行药物测试,而不是针对单个突变。”(生物谷 Bioon.com)
参考资料:
Jacqulyne P. Robichaux et al. Structure-based classification predicts drug response in EGFR-mutant NSCLC. Nature, 2021, doi:10.1038/s41586-021-03898-1.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


